Clear Sky Science · pl
Usunięcie DUSP6 przywraca wydolność limfocytów CAR T osłabioną przez utratę CD58 w nowotworze poprzez pobudzenie sygnalizacji AP-1
Dlaczego wzmocnienie komórek walczących z rakiem ma znaczenie
Zmodyfikowane komórki układu odpornościowego zwane komórkami CAR T zrewolucjonizowały leczenie niektórych nowotworów krwi, jednak wiele osób i tak doświadcza nawrotów, ponieważ guzy uczą się unikać ataku. W tym badaniu odkryto ukrytą słabość niektórych nowotworów, która po cichu dezaktywuje komórki CAR T od środka — oraz pokazano, jak precyzyjna modyfikacja genetyczna może przywrócić wytrzymałość tych komórek, ich źródła energii i zdolność do zabijania. Dla czytelnika to wgląd w to, jak terapie komórkowe następnej generacji mogą stać się trwalsze i skuteczniejsze dla większej liczby pacjentów.
Brakujący uchwyt na komórkach nowotworowych
Aby dobrze działać, komórki CAR T potrzebują pewnego «uścisku dłoni» z celem. Wiele komórek nowotworowych eksponuje na powierzchni cząsteczkę zwaną CD58, która pełni rolę „uchwytu” dla komórek odpornościowych, pomagając im się przyczepić i utworzyć szczelny kontakt. Wcześniejsze prace wykazały, że gdy nowotwory tracą CD58, komórkom CAR T trudniej jest nawiązać ten kontakt i stają się mniej skuteczne. W tym badaniu naukowcy zadali bardziej szczegółowe pytanie: poza tym mechanicznym problemem z „uściskiem dłoni”, jak utrata CD58 przeprogramowuje wewnętrzną biologię komórek CAR T, by stopniowo tłumić ich funkcję?
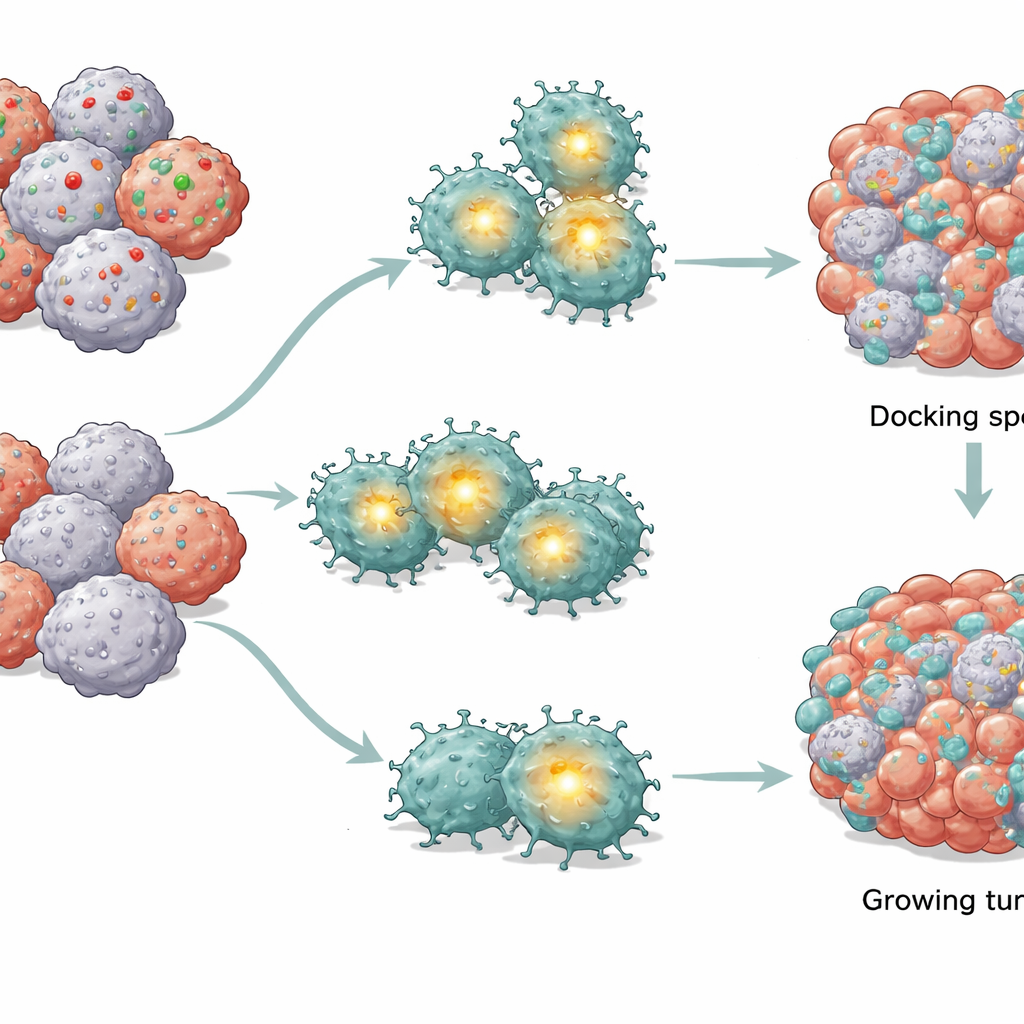
Przerwany przewód wewnątrz komórek CAR T
Porównując komórki CAR T wystawione na kontakt z normalnymi guzami z tymi stykającymi się z nowotworami pozbawionymi CD58, zespół odkrył, że kluczowe centrum kontroli w komórkach T — zwane AP-1 — było selektywnie osłabione, podczas gdy inne główne szlaki sygnałowe pozostały w dużej mierze nienaruszone. AP-1 to grupa białek uruchamiających geny zaangażowane w aktywację i przetrwanie. Gdy aktywność AP-1 malała, komórki CAR T wykazywały typowe objawy wewnętrznego kryzysu energetycznego: mniej i mniejsze mitochondria (ich elektrownie), obniżoną zdolność do zużywania tlenu i metabolizowania cukru oraz utratę potencjału elektrycznego przez błony mitochondrialne. Jednocześnie narastały szkodliwe reaktywne formy tlenu. Te zmiany razem skłaniały komórki CAR T ku programowi autodestrukcji wynikającemu z uszkodzeń mitochondriów, nawet bez zewnętrznych sygnałów śmierci.
Wyłączenie wewnętrznego hamulca
Aby zrozumieć, dlaczego AP-1 był tak stłumiony, badacze zajrzeli w górę szlaku w poszukiwaniu molekularnych „hamulców”, które mogły być nadaktywne. Stwierdzili, że komórki CAR T konfrontowane z guzami CD58‑ujemnymi zwiększały ekspresję kilku fosfataz — enzymów wyłączających szlaki sygnałowe — w szczególności jednej zwanej DUSP6. Używając najpierw leków, a następnie precyzyjnego edytowania genów, by zablokować te enzymy, odkryli, że usunięcie DUSP6 najsilniej przywracało aktywność AP-1. Komórki CAR T z edytowanym DUSP6 lepiej się namnażały, tworzyły więcej mitochondriów, sprawniej spalały paliwo, produkowały więcej cząsteczek zabijających nowotwór i były mniej skłonne do apoptozy, zwłaszcza przy wielokrotnym wyzwaniu przez komórki nowotworowe pozbawione CD58.
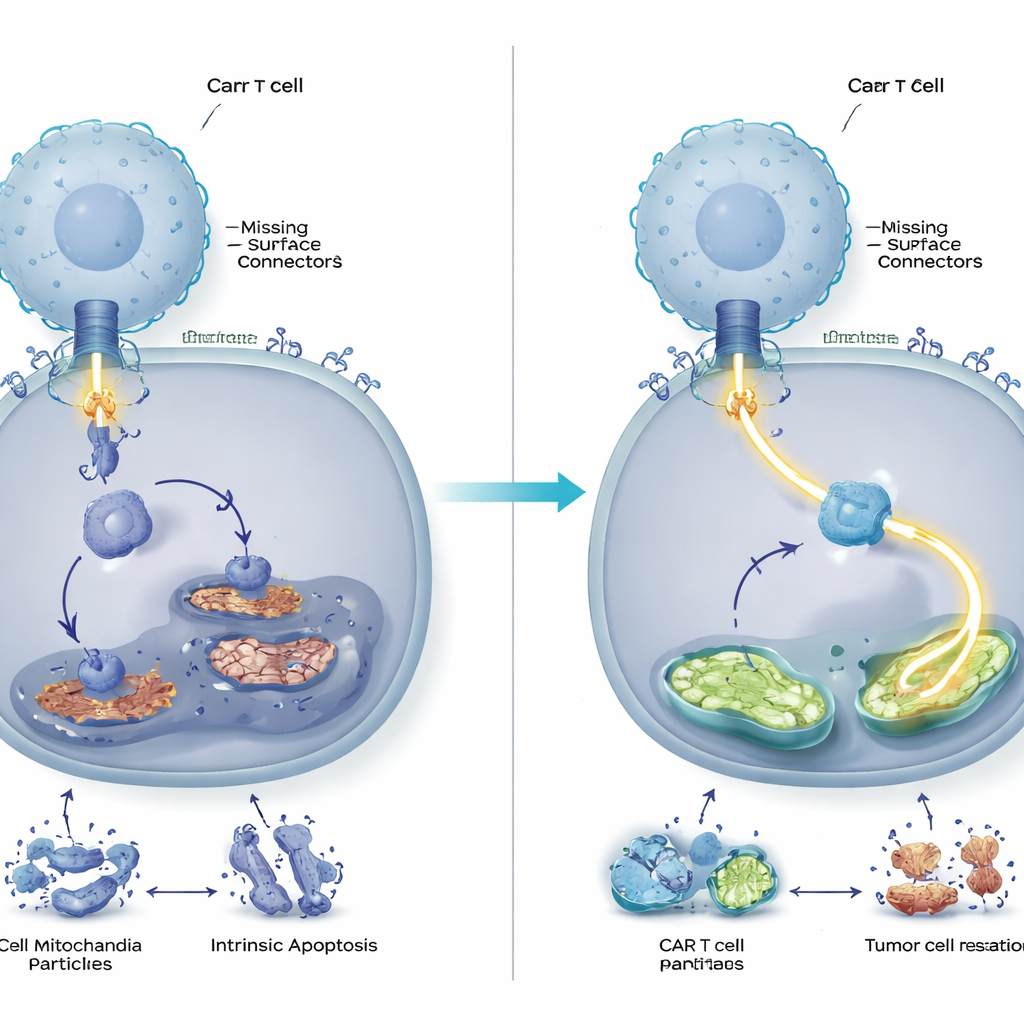
Mocniejsza, dłużej utrzymująca się kontrola guza u zwierząt
Zespół sprawdził następnie, czy to molekularne „strojenie” ma znaczenie w żywych organizmach. U myszy noszących ludzkie komórki nowotworu krwi, które miały lub nie miały CD58, komórki CAR T pozbawione DUSP6 skuteczniej usuwały guzy i dłużej je powstrzymywały niż konwencjonalne komórki CAR T. Zmodyfikowane komórki namnażały się silniej, wykazywały mniej markerów wyczerpania i wydzielały wyższe poziomy kluczowych przekaźników odpornościowych. Co istotne, korzyści z usunięcia DUSP6 obserwowano nie tylko przy guzach pozbawionych CD58, lecz także gdy guzy go zachowywały, co sugeruje, że ta modyfikacja mogłaby szerzej wzmocnić terapie CAR T zamiast być wąskim rozwiązaniem dla rzadkiego podtypu guza.
Wskazówki z danych pacjentów
Aby sprawdzić znaczenie u ludzi, badacze przeanalizowali dane ekspresji genów u osób leczonych komórkami CAR T lub lekami blokującymi punkty kontrolne odporności. U pacjentów z rozlanym chłoniakiem dużych komórek B otrzymujących terapię CAR T o podwójnym ukierunkowaniu niższe poziomy DUSP6 w komórkach CD8 przed lub krótko po infuzji wiązały się z wyższymi wskaźnikami całkowitej odpowiedzi. W oddzielnej kohorcie chorych na raka skóry leczonych przeciwciałami anty-PD-1, wyczerpane komórki CD8 od pacjentów‑nieodpowiadających miały skłonność do wyższej ekspresji DUSP6 niż komórki od osób odpowiadających. Razem te obserwacje sugerują, że DUSP6 działa jako negatywny marker sprawności limfocytów T w różnych immunoterapiach i że jego obniżenie mogłoby poprawić wyniki leczenia.
Co to oznacza dla przyszłych terapii przeciwnowotworowych
Dla czytelnika nieprofesjonalnego przekaz jest taki, że niektóre nowotwory uciekają przed atakiem komórek CAR T nie tylko przez ukrywanie się przed rozpoznaniem, lecz także przez sabotowanie wewnętrznych „silników” tych komórek. Utrata „uchwytu” CD58 na komórkach nowotworowych cicho obniża sygnalizację AP-1 w komórkach CAR T, osłabiając ich mitochondria, zwiększając toksyczne produkty uboczne i skłaniając je do przedwczesnej śmierci. Poprzez usunięcie hamulca DUSP6 naukowcy mogą przywrócić tę utraconą sygnalizację, naprawić kondycję mitochondriów i dać komórkom CAR T większą wytrzymałość i siłę zabijania, nawet wobec opornych guzów. Chociaż potrzebne są dalsze testy bezpieczeństwa i badania kliniczne, ablacja DUSP6 jawi się jako obiecująca strategia inżynieryjna, by uczynić żywe leki przeciwnowotworowe silniejszymi, dłużej działającymi i potencjalnie skutecznymi dla szerszej grupy pacjentów.
Cytowanie: Ma, X., Zhang, Y., Wang, Y. et al. DUSP6 ablation restores CAR T-cell fitness impaired by tumor CD58 loss through invigoration of AP-1 signaling. Sig Transduct Target Ther 11, 100 (2026). https://doi.org/10.1038/s41392-026-02597-5
Słowa kluczowe: komórki CAR T, CD58, DUSP6, immunoterapia nowotworów, metabolizm limfocytów T