Clear Sky Science · pl
Uwolnienie potencjału bimetalicznego nanobomu aktywującego szlak STING w celu wzmocnienia bispecyficznego aktywatora limfocytów T wobec foto-immunoterapii raka jelita grubego
Odwracanie układu odpornościowego przeciw rakowi jelita
Raki jelita grubego i odbytnicy są powszechne i często śmiertelne, częściowo dlatego, że guzy uczą się ukrywać przed układem odpornościowym. W tym badaniu przedstawiono nową strategię, która łączy kilka metod zwalczania nowotworu w jednej maleńkiej „nanobombie”, aby obudzić obronę organizmu, pomóc komórkom odpornościowym odnaleźć guz i zapobiec nawrotom lub przerzutom.
Dlaczego współczesne leki immunologiczne wymagają ulepszeń
Jedna obiecująca klasa leków przeciwnowotworowych, zwana bispecyficznymi aktywatorami limfocytów T, działa jak biologiczni swatowie: jeden koniec wiąże limfocyt T (kluczowego „żołnierza” odporności), a drugi przyczepia się do markera na komórce nowotworowej, zmuszając je do zbliżenia, by limfocyt mógł zabić. Choć skuteczne w nowotworach krwi, te leki mają trudności w guzach litych, takich jak rak jelita grubego. Szybko są usuwane z organizmu, mogą atakować zdrowe tkanki, które mają ten sam marker, i często napotykają „zimne” guzy, pozbawione wystarczającej liczby komórek odpornościowych, by terapia zadziałała. Lekarze i naukowcy szukają więc sposobów bezpieczniejszego dostarczania tych leków i przełączania zimnych guzów w „gorące”, nasycone aktywowanymi komórkami odpornościowymi.
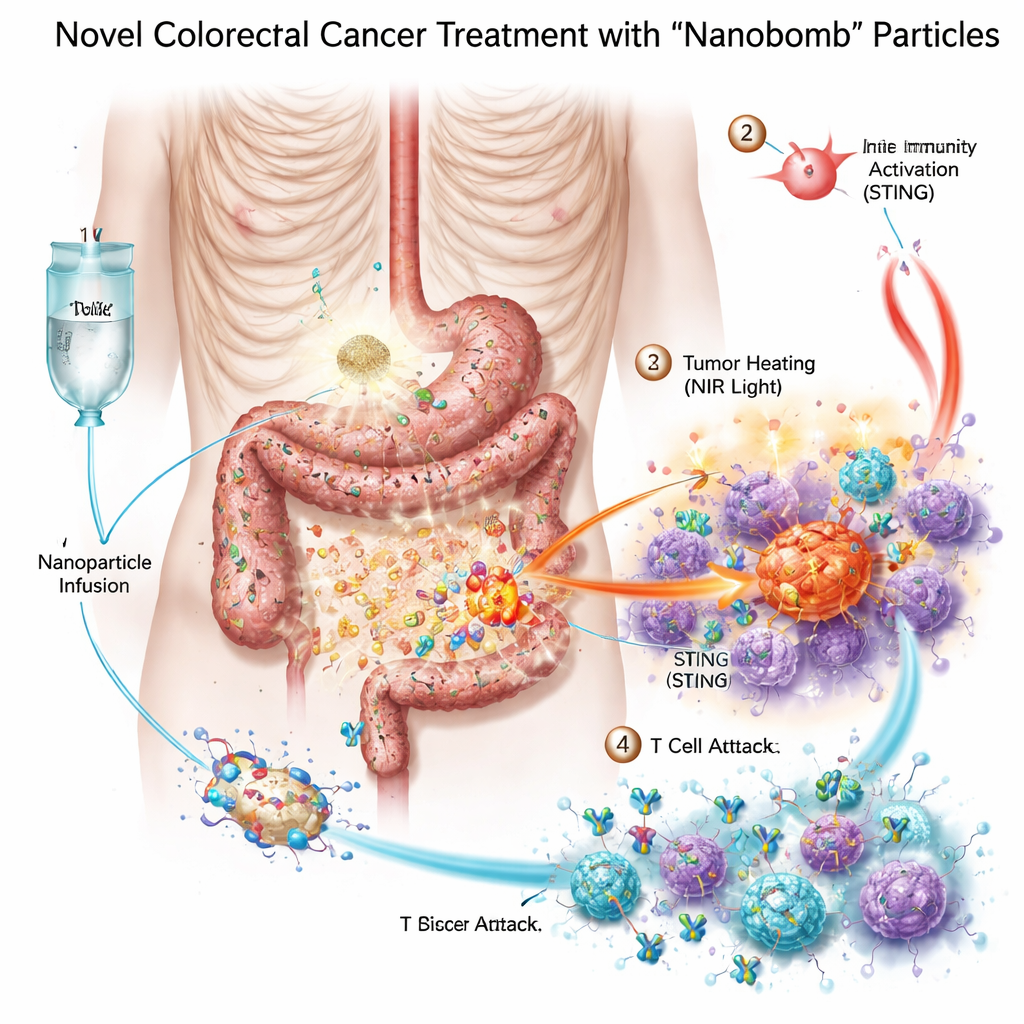
Zapakowanie trzech broni w jedną maleńką „nanobombę”
Naukowcy zaprojektowali bimetaliczną nanobombę — naukowo nazwaną MnO2/Co‑DA@BiTE/HPT — która łączy trzy tryby leczenia w jednej cząstce. Po pierwsze, rdzeń zawiera mangan i kobalt, metale zdolne do aktywacji komórkowego systemu alarmowego zwanego szlakiem STING, który pomaga organizmowi rozpoznawać niebezpieczeństwo i przywoływać komórki odpornościowe. Po drugie, powierzchnia cząstki jest pokryta bispecyficznym aktywatorem limfocytów T, który łączy limfocyty T z komórkami nowotworowymi. Po trzecie, materiał pochłania promieniowanie bliskiej podczerwieni, co pozwala lekarzom podgrzewać guz od zewnątrz w formie terapii fototermalnej. Aby nanobomby kierowały się do komórek raka jelita grubego, zespół dodał krótki fragment DNA — aptamer — rozpoznający PD‑L1, cząsteczkę często obfitującą na tych guzach. Gdy cząstki docierają do guza, naturalne enzymy w tkance nowotworowej pomagają je rozbić i uwolnić ładunek dokładnie tam, gdzie jest potrzebny.
Podgrzewanie, alarmowanie i rekrutacja armii odpornościowej
W badaniach in vitro nanobomby zabijały komórki raka jelita grubego skuteczniej niż jakikolwiek pojedynczy składnik. Po naświetleniu bliską podczerwienią cząstki się nagrzewały, stresowały i uszkadzały komórki nowotworowe oraz przyczyniały się do powstawania reaktywnych form tlenu — wysoce reaktywnych cząsteczek, które dalej uszkadzają komórki guza. Ten stres łamał DNA komórek i prowadził je do szczególnie widocznej formy śmierci, która wysyła sygnały „zagrożenia”. Sąsiadujące komórki odpornościowe, zwłaszcza komórki dendrytyczne, pochłaniały umierające fragmenty guza i aktywowały szlak STING przy udziale uwolnionego manganu i kobaltu. Następnie produkowały interferony i inne zapalne przekaźniki, które dojrzewają i przyciągają limfocyty T. Równocześnie bispecyficzny aktywator na nanobombie fizycznie łączył limfocyty T z komórkami PD‑L1 dodatnimi, poprawiając aktywację limfocytów T i zabijanie guza nawet w wcześniej zimnych nowotworach.
Od kurczenia się guza do trwałej pamięci odpornościowej
W kilku modelach mysich — w tym w podskórnych guzach jelita grubego, guzach na obu stronach ciała, przerzutach do płuc oraz w modelu nawrotu po operacji — nanobomby wraz ze światłem silnie spowalniały lub niemal zatrzymywały wzrost guza. Leczone guzy zawierały znacznie więcej niszczących nowotwór limfocytów CD8 i mniej regulatorowych limfocytów T, które zwykle tłumią odpowiedzi immunologiczne. Komórki dendrytyczne w guzach i w węzłach chłonnych wykazywały cechy dojrzewania, a badania krwi ujawniły podwyższone poziomy cytokin stymulujących układ odpornościowy. Co ważne, myszy, które oczyściły guzy po leczeniu nanobombami, były lepiej chronione, gdy nowotwór został ponownie wprowadzony, i rozwijały mniej przerzutów do płuc, co pokazuje, że terapia pomogła zbudować długotrwałą pamięć odpornościową, a nie tylko spowodować jednorazowe zmniejszenie guza.
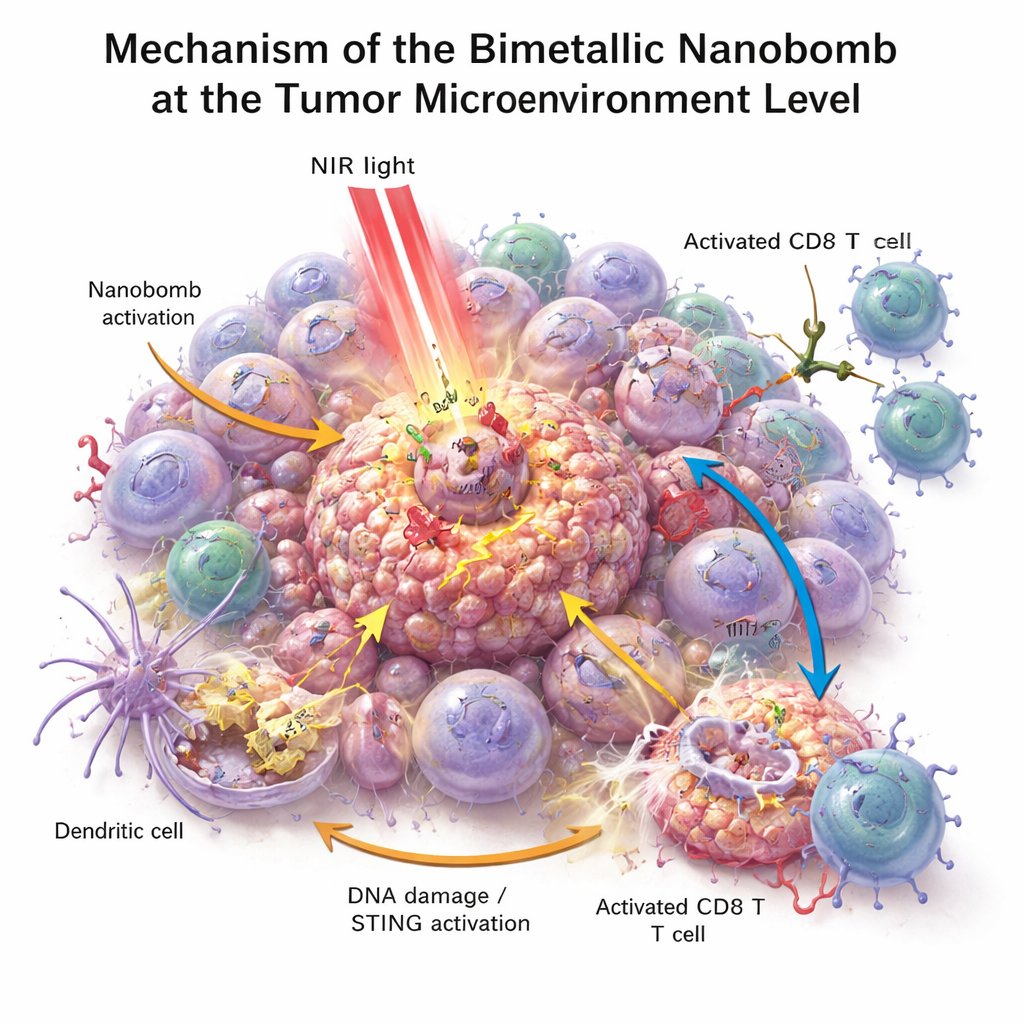
Co to może znaczyć dla przyszłej opieki onkologicznej
Ta praca przedstawia nanomedycynę „potrójnego uderzenia”, która podgrzewa guzy, włącza wewnętrzny alarm zagrożenia i kieruje limfocyty T bezpośrednio do komórek nowotworowych — wszystko w jednej celowanej cząstce. U myszy podejście to nie tylko przemieniło zimne guzy jelita grubego w gorące, zapalne ogniska, ale także pomogło zapobiec nawrotom i rozprzestrzenianiu się choroby. Choć technologia wciąż jest daleka od zastosowań klinicznych — skalowanie, długoterminowe bezpieczeństwo i badania u ludzi pozostają poważnymi wyzwaniami — daje plan działania dla przyszłych terapii łączących inteligentne materiały z lekami immunologicznymi, by zapewnić pacjentom silniejszą i trwalszą odpowiedź przeciwnowotworową.
Cytowanie: Mu, M., Li, H., Chen, B. et al. Unleashing the potential of bimetallic nanobomb-mediated STING pathway to enhance bispecific T-cell engager against colorectal cancer photo-immunotherapy. Sig Transduct Target Ther 11, 80 (2026). https://doi.org/10.1038/s41392-026-02596-6
Słowa kluczowe: rak jelita grubego, immunoterapia, nanocząstki, szlak STING, bispecyficzny aktywator limfocytów T