Clear Sky Science · pl
Spersonalizowana terapia kierowana PK–PD za pomocą platformy wielo-organoidowej pochodzącej z komórek iPS u pacjentów z rakiem piersi z mutacją NF1
Dlaczego te badania mają znaczenie dla pacjentów
Wiele osób z rakiem otrzymuje leki, które działają dobrze u niektórych pacjentów, ale u innych zawodzą i często wywołują dotkliwe działania niepożądane. W tym badaniu opisano nowy sposób testowania terapii przeciwnowotworowych poza organizmem, wykorzystując mini‑organy hodowane w laboratorium z komórek pobranych od pacjenta. Praca koncentruje się na trudnej do leczenia postaci raka piersi spowodowanej zmianami w genie NF1 i pokazuje, jak połączenie strategii naprawy genu z lekiem celowanym może prowadzić do bezpieczniejszej, skuteczniejszej i naprawdę spersonalizowanej terapii.
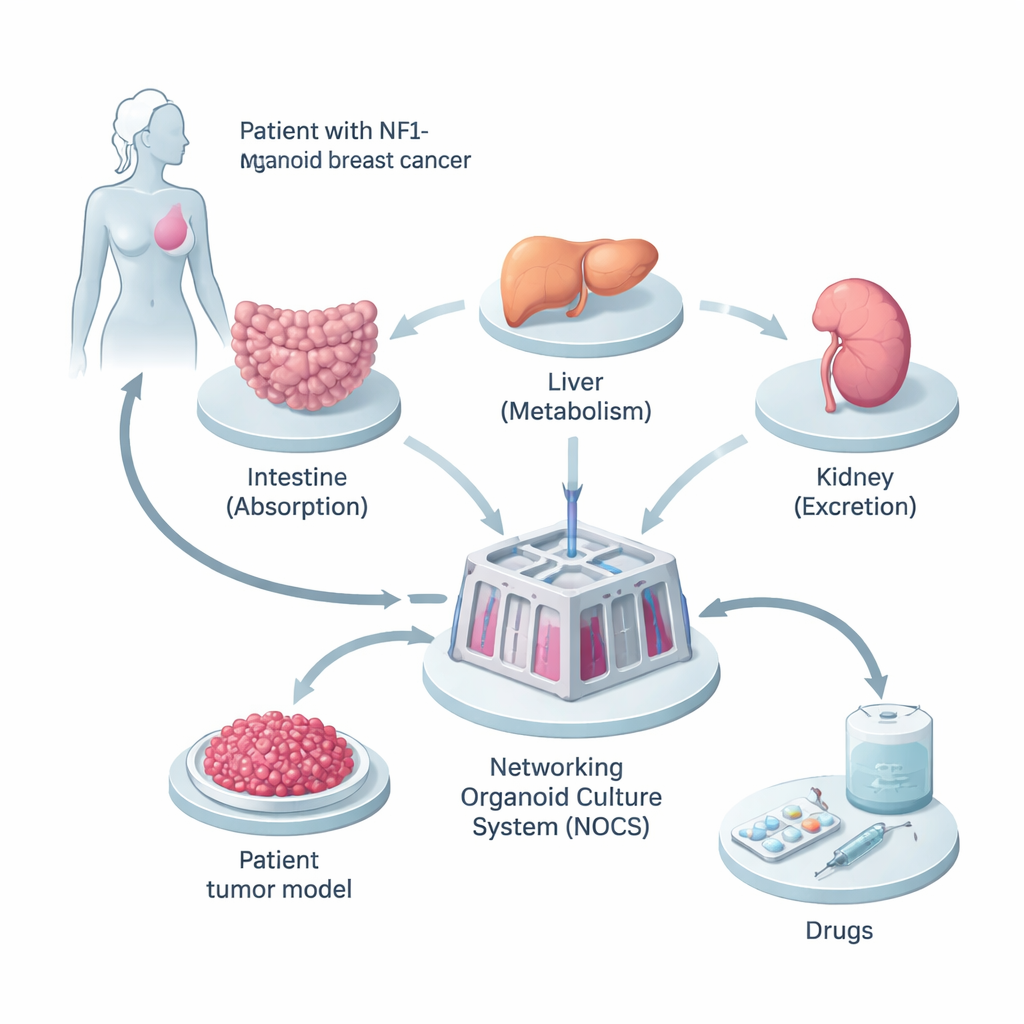
Budowa miniaturowej wersji organizmu pacjenta
Naukowcy zaczęli od tkanki pobranej od kobiety, u której rak piersi miał dziedziczną mutację w genie NF1. Przeprogramowali jej normalne komórki przypominające skórę w indukowane pluripotentne komórki macierzyste (iPS), które mogą przekształcić się niemal w każdy typ komórki w organizmie. Z tych komórek wyhodowali trzy rodzaje miniaturowych organów — jelito cienkie, wątrobę i nerkę — ponieważ to w tych miejscach leki są wchłaniane, przetwarzane i usuwane. Równolegle stworzyli trójwymiarowe „sferoidy” nowotworowe z komórek jej guza, zachowując układ typów komórek i zmiany genetyczne występujące w pierwotnym nowotworze.
Żywy obwód do testowania leków
Aby mini‑organy zachowywały się bardziej jak prawdziwe ciało, zespół połączył je w urządzeniu wypełnionym płynem zwanym Networking Organoid Culture System (NOCS). W takim układzie płyn hodowlany krążył między przedziałami jelita, wątroby, nerki i guza, naśladując krążenie krwi. Leki można było podawać w sposób przypominający połknięcie tabletki lub otrzymanie zastrzyku, a czujniki i pompy kontrolowały prędkość przepływu „krwi” oraz częstotliwość jej odświeżania. Dzięki temu naukowcy mogli śledzić, ile leku jest wchłanianych, jak szybko jest rozkładany i jak mocno działa na guz — wszystko w modelu opartym na tkankach pacjenta i człowieka.
Naprawa uszkodzonego genu przez wycinanie eksonu
Nowotwór pacjentki nosił szkodliwą mutację NF1, która utrzymuje włączone szlaki wzrostu i sprawia, że wiele standardowych leków jest nieskutecznych. Zespół zaprojektował krótkie fragmenty materiału genetycznego, zwane antysensownymi oligonukleotydami, które kierują maszynerię przetwarzania RNA do pominięcia wadliwego fragmentu (eksonu 2) genu NF1. Używając systemu dostarczania opartego na wektorze wirusowym, działającego przez kilka dni, wywołali stabilne „pomijanie eksonu” w komórkach nowotworowych pacjentki. Powstał krótszy, ale funkcjonalny białkowy produkt NF1, osłabiono nadaktywne sygnały wzrostu i zwiększono wrażliwość komórek nowotworowych na leczenie.
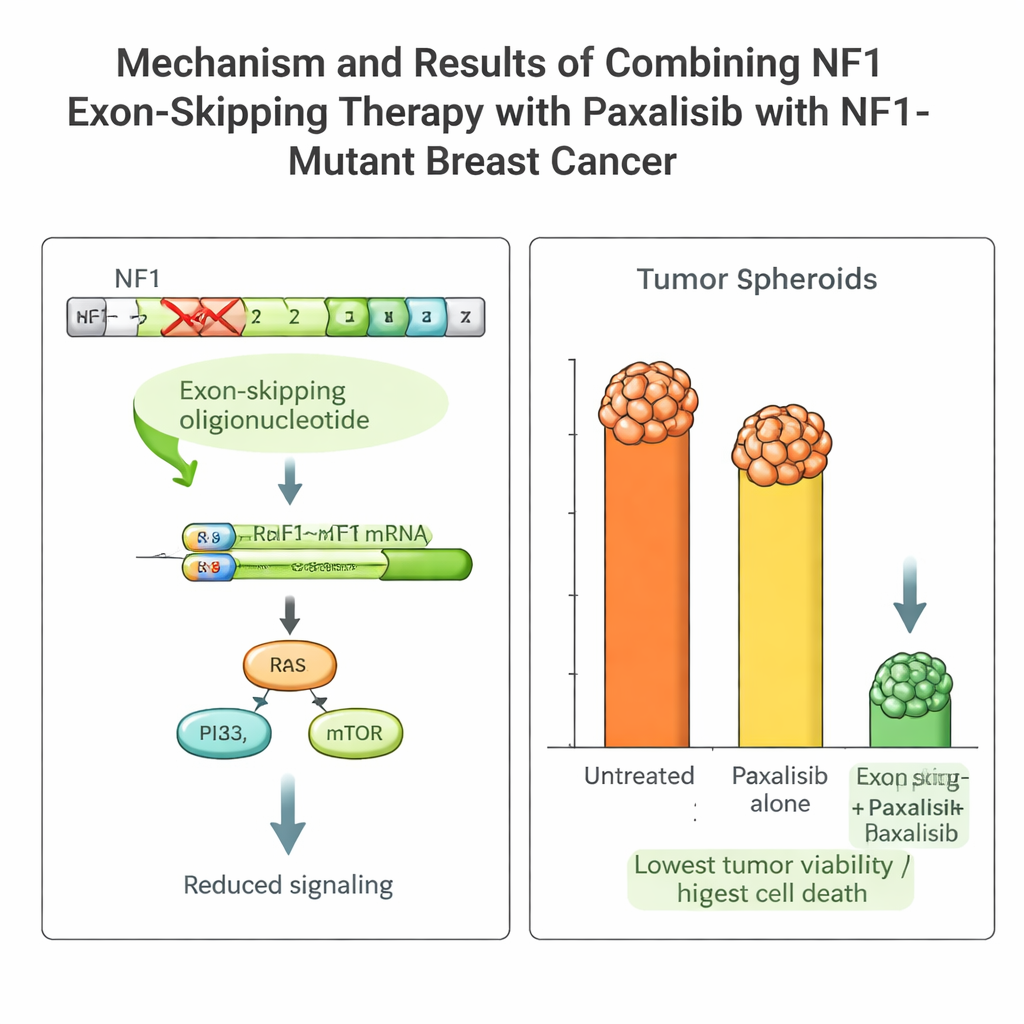
Wybór właściwego leku celowanego z wykorzystaniem wytycznych PK/PD
Dysponując tą platformą, zespół porównał kilka zaawansowanych leków blokujących szlak PI3K–mTOR, który działa poniżej NF1. Mierzyli farmakokinetykę (jak organizm radzi sobie z lekiem) i farmakodynamikę (jak lek działa na guz) zarówno u myszy, jak i w systemie NOCS. Jeden z leków, Paxalisib, wyróżnił się: był dobrze wchłaniany w jelicie, utrzymywał się w systemie na użytecznych poziomach i zachowywał się podobnie u zwierząt i w urządzeniu organoidowym. W połączeniu z pomijaniem eksonu NF1, skuteczność Paxalisibu wobec komórek guza pacjentki wzrosła dramatycznie, z silnym zahamowaniem wzrostu i wyraźnymi oznakami programowanej śmierci komórek, zarówno w NOCS, jak i u myszy niosących guz pacjentki.
Równoważenie korzyści i ryzyka między organami
Ponieważ modele jelita, wątroby i nerki były częścią tego samego obwodu, badacze mogli także obserwować wczesne oznaki uszkodzenia narządów. Paxalisib wywoływał reakcje stresowe i subtelne osłabienie bariery w modelach jelitowych i nerkowych oraz oznaki przeciążenia w wątrobie, ale bez istotnej utraty żywotności komórek przy testowanej dawce. Taki widok całego „ciała”, oparty na ludzkich tkankach, daje możliwość porównania opcji terapeutycznych nie tylko pod kątem zmniejszania guzów, lecz także potencjalnego wpływu na zdrowe organy, zanim lek trafi do pacjenta.
Co to może znaczyć dla przyszłej opieki onkologicznej
Mówiąc prosto, badanie pokazuje, że obecnie możliwe jest wyhodowanie uproszczonego, specyficznego dla pacjenta „mini‑ciała na chipie”, które może testować, jak różne leki — a nawet podejścia naprawcze genu — będą się zachowywać i wchodzić ze sobą w interakcje. Dla tej pacjentki z rakiem piersi z mutacją NF1 optymalną strategią okazało się połączenie terapii pomijającej ekson NF1 i doustnego leku Paxalisib, które razem hamowały wzrost guza znacznie bardziej niż każde z nich osobno. Jeśli metoda zostanie dalej rozwinięta i sprawdzona u większej liczby pacjentów, takie platformy mogłyby kierować lekarzy ku planom leczenia dopasowanym do genów i biologii konkretnej osoby, zwiększając szanse powodzenia przy zmniejszeniu niepotrzebnej toksyczności.
Cytowanie: Lim, J.H., Mun, S.J., Kang, H.M. et al. Personalized pharmacokinetic–pharmacodynamic guided therapy via an induced pluripotent stem cell–derived multi-organoid platform in NF1-mutant breast cancer. Sig Transduct Target Ther 11, 79 (2026). https://doi.org/10.1038/s41392-026-02595-7
Słowa kluczowe: spersonalizowana onkologia, rak piersi, organoidy, mutacja NF1, terapia celowana