Clear Sky Science · pl
Wykorzystanie lipidowo napędzanych ścieżek immunometabolicznych w przerzutach do sieci większej w celu zwiększenia skuteczności immunoterapii u pacjentek z rakiem jajnika
Dlaczego tłuszcz w jamie brzusznej ma znaczenie w raku jajnika
Rak jajnika często rozprzestrzenia się do tłuszczowej fałdy w jamie brzusznej zwanej siecią większą. Miejsce to jest bogate w komórki tłuszczowe i komórki układu odpornościowego i okazuje się być czymś więcej niż biernym obserwatorem. Podsumowane tutaj badanie pokazuje, że sposób, w jaki komórki odpornościowe wykorzystują i przetwarzają tłuszcz w tych przerzutach do sieci może pomóc wyjaśnić, dlaczego tylko niewielka część pacjentek korzysta z nowoczesnych immunoterapii. Sugeruje też nowe kombinacje leków i testy obrazowe, które mogłyby uczynić te terapie skuteczniejszymi dla większej liczby osób.
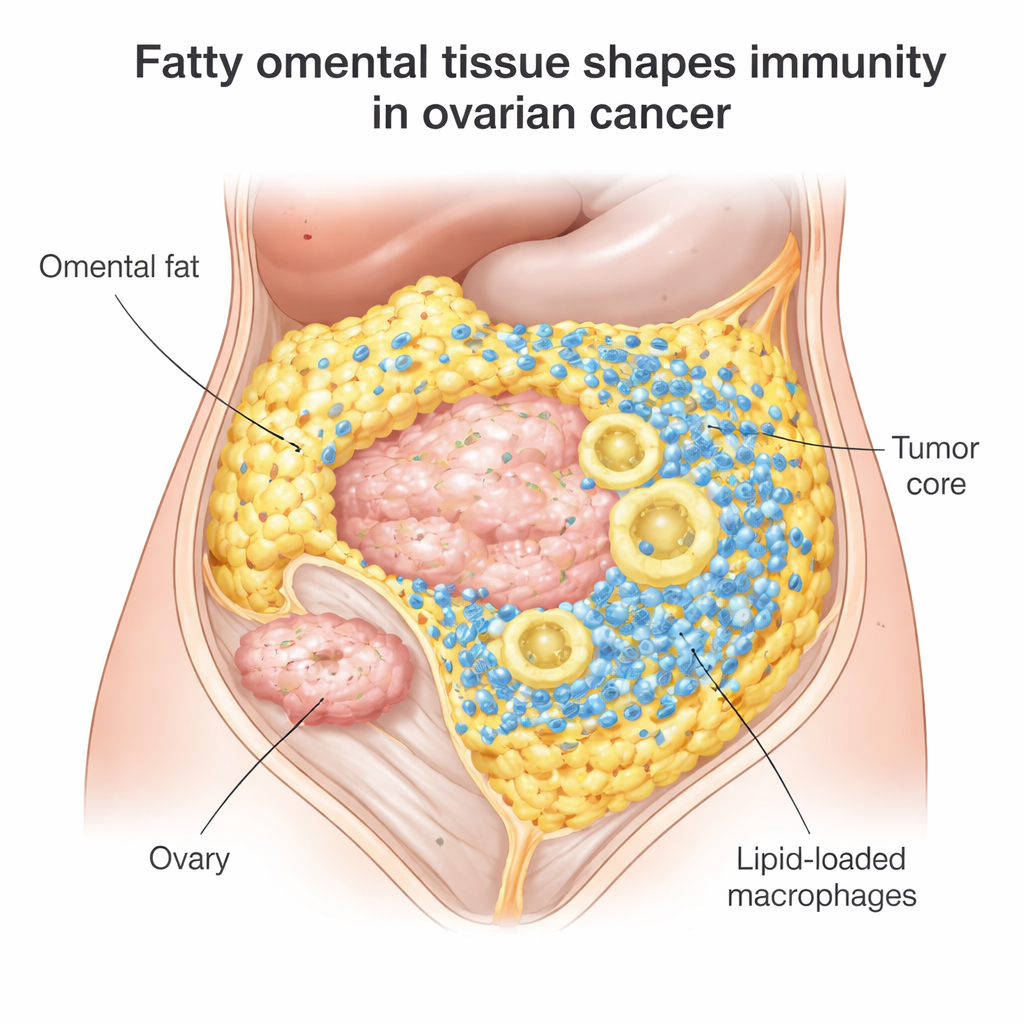
Ukryte pole bitwy w tłuszczu brzusznym
Większość kobiet z rakiem nabłonkowym jajnika początkowo reaguje na zabieg chirurgiczny i chemioterapię, ale u 70–80% choroba nawraca, a leki blokujące punkty kontrolne odporności, takie jak niwolumab czy pembrolizumab, pomagają tylko u około 10–15%. Naukowcy skupili się na przerzutach do sieci większej, częstym miejscu rozsiewu raka jajnika wśród komórek tłuszczowych. Analizując ponad 100 próbek guza, odkryli, że guzy w sieci były pełne komórek odpornościowych: cytotoksycznych limfocytów T, które mogą atakować nowotwór, oraz dużych komórek żernych zwanych makrofagami. Był jednak haczyk. Te limfocyty T miały tendencję do gromadzenia się na granicy między guzem a tłuszczem, zamiast penetrować rdzeń guza, gdzie są najbardziej potrzebne.
Tłuszcz, który zasila niektóre komórki odpornościowe, a inne przytłacza
Szczegółowe analizy wykazały, że limfocyty T w tych tłustych guzach adaptują się do lokalnego środowiska poprzez pobieranie lipidów, czyli tłuszczów, z pobliskich komórek tłuszczowych. Wygląda na to, że to utrzymuje ich sprawność metaboliczną: ich aktywność genowa i testy laboratoryjne pokazywały, że potrafią rozpoznawać i zabijać własne komórki nowotworowe pacjentki. Jednocześnie wiele makrofagów związanych z guzem w sieci było silnie naładowanych kroplami tłuszczu. Te „napakowane lipidami” makrofagi wykazywały oznaki wysokiego stresu oksydacyjnego — chemicznego zużycia związanego z reaktywnymi formami tlenu — i przestawiały się w kierunku stanu immunosupresyjnego wspierającego guz. Innymi słowy, to samo bogate w tłuszcz środowisko, które może odżywiać efektywne limfocyty T, jednocześnie popycha makrofagi w szkodliwy tryb, tłumiąc ogólną odpowiedź immunologiczną.
Przeprogramowanie przekarmionych makrofagów dostępnymi lekami
Naukowcy pytali następnie, czy można odwrócić ten stan i uczynić z tych zestresowanych makrofagów sojuszników. Korzystając ze świeżych fragmentów guza hodowanych w laboratorium, przetestowali dwa podejścia. Pierwsze obejmowało maravirok — lek przeciw HIV blokujący CCR5, receptor dla sygnału immunologicznego CCL5, który jest obfity na granicy guz–tłuszcz. Drugie polegało na blokowaniu CD36, kluczowego receptora „żerującego”, który pozwala makrofagom importować kwasy tłuszczowe. Obie terapie zmniejszały ładunek tłuszczu wewnątrz makrofagów, obniżały markery stresu oksydacyjnego i szkodliwej peroksydacji lipidów oraz wyzwalały fale sygnałów zapalnych. Co istotne, pozwalały one cytotoksycznym limfocytom T namnażać się i przesuwać z tłustego obrzeża do rdzenia guza, wzmacniając lokalną aktywność immunologiczną bez dodawania zewnętrznych komórek odpornościowych.
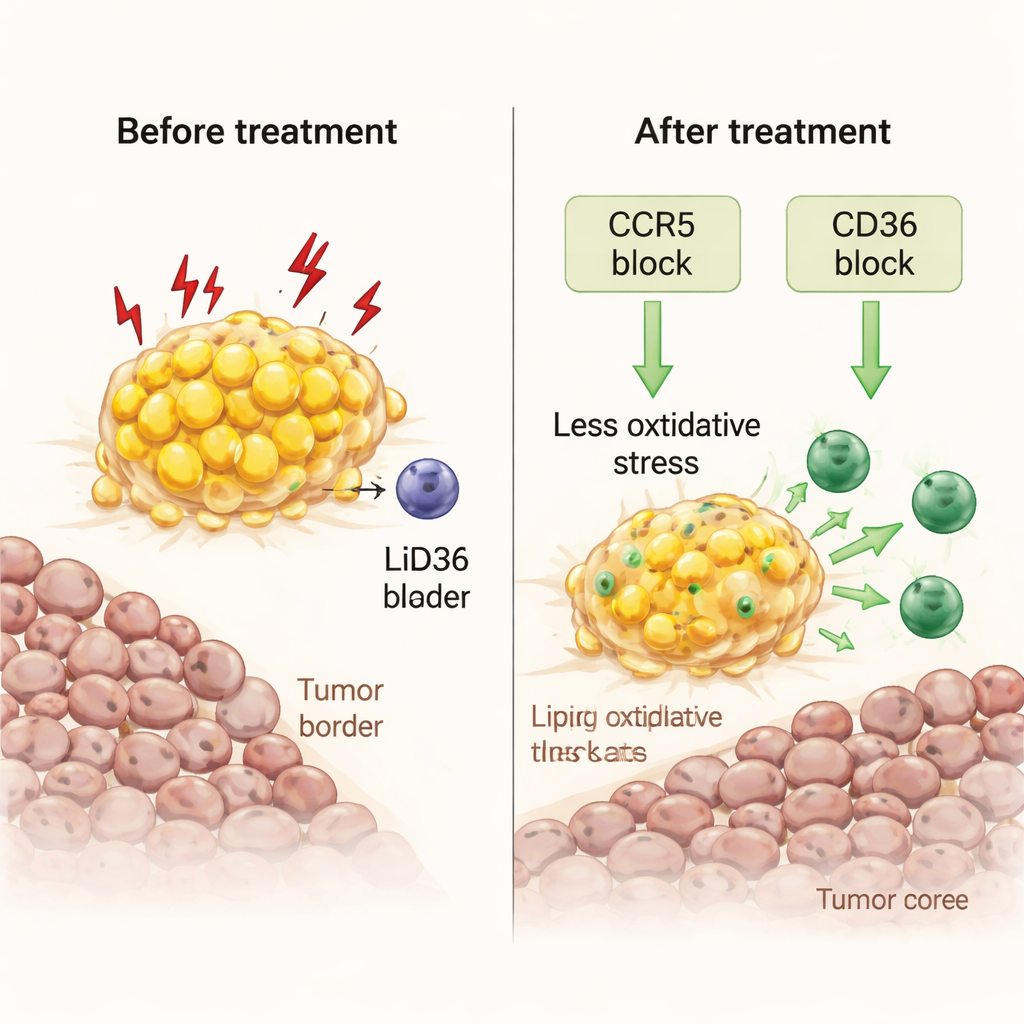
Od ścieżek komórkowych do modeli i pacjentów
Aby sprawdzić te koncepcje w bardziej realistycznym kontekście, zespół użył wysterylizowanych myszy „humanizowanych”, wyposażonych w podobny do ludzkiego układ odpornościowy, i wszczepił im ludzki rak piersi w tkankę bogatą w tłuszcz. Leczenie maravirokiem przeprogramowało ludzkie makrofagi u tych zwierząt w sposób odzwierciedlający próbki pochodzące od pacjentów: zmniejszenie sygnatur lipidowych i stresu, zwiększona produkcja cytokin i silniejsze wsparcie szlaków związanych z limfocytami T. W warunkach klinicznych badacze ponownie przeanalizowali japońskie badanie niwolumabu u pacjentek z rakiem jajnika opornym na chemioterapię. Każda pacjentka, która odniosła korzyść z leku, miała przerzuty w sieci widoczne w materiałach chirurgicznych. Korzystając z tomografii komputerowej lub rezonansu magnetycznego wraz z analizą uczenia maszynowego rozkładu tkanki tłuszczowej, zbudowali drzewo decyzyjne, które mogło nieinwazyjnie wskazać pacjentki, których guzy prawdopodobnie znajdują się blisko trzewnej tkanki tłuszczowej — i w jednym prospektywnym przypadku metoda ta prawidłowo przewidziała pacjentkę, która później odpowiedziała na niwolumab.
Co to może oznaczać dla przyszłego leczenia
Dla czytelnika niebędącego specjalistą kluczowy wniosek jest taki, że „gdzie” rak jajnika rośnie w organizmie i jak pobliski tłuszcz przebudowuje komórki odpornościowe, może silnie wpływać na to, czy immunoterapia zadziała. Tłuszczowe przerzuty do sieci większej wydają się kryć energiczne limfocyty T, ale także przekarmione, zestresowane makrofagi, które osłabiają atak. Ulżąć ładunkowi lipidowemu tych makrofagów i zmniejszyć ich stres oksydacyjny — stosując blokery CCR5, takie jak maravirok, środki celujące w CD36 lub powiązane strategie — może być możliwe przekształcenie częściowo zablokowanej odpowiedzi immunologicznej w pełnoskalowy atak na guz. Równocześnie miary obrazowe zaangażowania sieci większej mogłyby pomóc lekarzom wybrać pacjentki, które najprawdopodobniej skorzystają z leków blokujących punkty kontrolne odporności, wprowadzając bardziej spersonalizowane i potencjalnie skuteczniejsze podejście do leczenia raka jajnika.
Cytowanie: Suarez-Carmona, M., Hampel, M., Zhang, XW. et al. Harnessing lipid-driven immunometabolic pathways in omental metastases to enhance immunotherapy in patients with ovarian cancer. Sig Transduct Target Ther 11, 78 (2026). https://doi.org/10.1038/s41392-026-02594-8
Słowa kluczowe: rak jajnika, tłuszcz sieci większej, immunoterapia, makrofagi związane z guzem, metabolizm lipidów