Clear Sky Science · pl
Aktywacja receptora tromboksanu w komórkach dendrytycznych łagodzi sepsę przez hamowanie rekrutacji neutrofili zależnej od S100a8/a9
Dlaczego powstrzymanie wymykających się infekcji ma znaczenie
Sepsa to zagrażająca życiu nadmierna reakcja organizmu na zakażenie, często zaczynająca się w płucach lub jelitach i prowadząca do niewydolności wielu narządów. Nawet przy współczesnej intensywnej opiece medycznej sepsa zabija miliony ludzi rocznie, ponieważ standardowe terapie głównie wspierają zawodzące organy, zamiast precyzyjnie uspokajać nieprawidłowo pracujący układ odpornościowy. W tym badaniu odkryto wcześniej ukrytą „hamulcową” funkcję w kluczowym typie komórek odpornościowych — komórkach dendrytycznych — która potrafi przyciszyć szkodliwe zapalenie bez wyłączania zdolności organizmu do zwalczania drobnoustrojów.
Stróże odporności pod presją
Komórki dendrytyczne pełnią rolę strażników układu odpornościowego: wykrywają zagrożenie, alarmują inne komórki odpornościowe i pomagają zdecydować, jak silna ma być odpowiedź. W próbkach krwi od pacjentów z sepsą autorzy stwierdzili, że komórek dendrytycznych było nie tylko mniej, lecz także wykazywały znacząco obniżone poziomy receptora o nazwie TP, który normalnie reaguje na lipidowy związek zwany tromboksanem A₂. Pacjenci, których komórki dendrytyczne miały najniższe poziomy TP, mieli tendencję do większej liczby krążących neutrofili — pierwszej linii obrony przeciw infekcjom — oraz cięższy przebieg choroby, co sugeruje, że gdy ten hamulec w komórkach dendrytycznych zawodzi, zapalenie może wymknąć się spod kontroli.
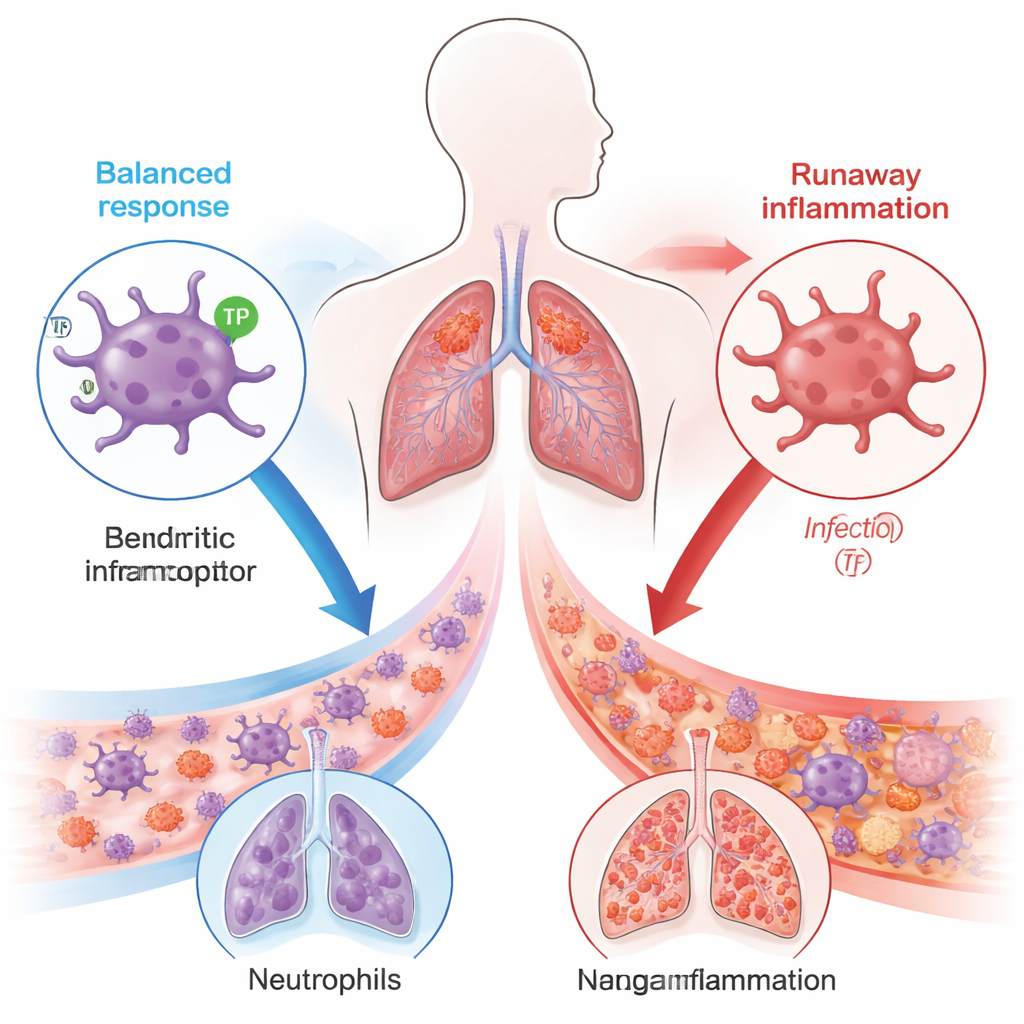
Gdy hamulec zawodzi, neutrofile zalewają płuca
Aby sprawdzić związek przyczynowo-skutkowy, zespół użył modeli mysich sepsy wywołanej albo przez przebicie jelita (zabieg uwalniający bakterię z jelita do jamy brzusznej), albo przez podanie toksyn bakteryjnych. Myszy zmodyfikowane tak, by pozbawione były TP tylko w komórkach dendrytycznych, miały znacznie gorsze rokowanie: częściej umierały, miały bardziej przepuszczalne płuca wypełnione płynem oraz wykazywały duże napływy neutrofili i uszkodzenia tkanek. Gdy komórki dendrytyczne pobrane od zwierząt pozbawionych TP przeniesiono do zdrowych myszy, biorcy także rozwijali cięższą sepsę, co potwierdza, że wadliwe sygnalizowanie w samych komórkach dendrytycznych może przesunąć równowagę w stronę śmiertelnego zapalenia.
Sygnał niebezpieczeństwa, który przywołuje zbyt wielu obrońców
Dalej badacze przeanalizowali, które geny zmieniały ekspresję w komórkach dendrytycznych przy braku TP. Dwa białka związane z sygnałem niebezpieczeństwa, S100A8 i S100A9, wyróżniały się silnie podwyższonymi poziomami. Te cząsteczki działają jak race przyciągające neutrofile do zapalonych tkanek. Zespół wykazał, że komórki dendrytyczne z septycznych myszy w testach laboratoryjnych przyciągały więcej neutrofili, a zablokowanie S100A8/A9 lekiem ostro zmniejszało to przyciąganie. Zarówno u myszy, jak i u pacjentów, wyższe poziomy S100A8/A9 szły w parze z niższymi poziomami TP. In vivo usunięcie S100A9 specyficznie w komórkach dendrytycznych — albo zablokowanie jego głównego receptora, czujnika odpornościowego TLR4 — ograniczało napływ neutrofili, zmniejszało powstawanie lepkościowych sieci DNA-białko zwanych zewnątrzkomórkowymi pułapkami neutrofili (NET) i chroniło płuca przed uszkodzeniem.
Obwód sygnałowy stojący za precyzyjnym hamulcem
Autorzy zmapowali następnie, jak TP kontroluje produkcję S100A8/A9 w komórkach dendrytycznych. Aktywacja TP uruchamiała wewnętrzny szereg zdarzeń obejmujący kinazę białkową (PKCδ) oraz czynnik transkrypcyjny STAT1, który przemieszcza się do jądra komórkowego, by wpływać na aktywność genów. Gdy ta ścieżka była nienaruszona, STAT1 pomagał utrzymać S100A8/A9 pod kontrolą, ograniczając rekrutację neutrofili. Zablokowanie PKCδ lub STAT1 przerwało ten ochronny obwód, pozwalając na wzrost S100A8/A9. Wreszcie zespół zbudował nanolek, łącząc związek aktywujący TP z peptydem ukierunkowującym konkretnie do komórek dendrytycznych. U septycznych myszy to celowane leczenie przywracało sygnał TP tylko w komórkach dendrytycznych, obniżało S100A8/A9, zmniejszało nagromadzenie neutrofili i NET w płucach oraz poprawiało przeżywalność — wszystko to bez szerokiego tłumienia układu odpornościowego.
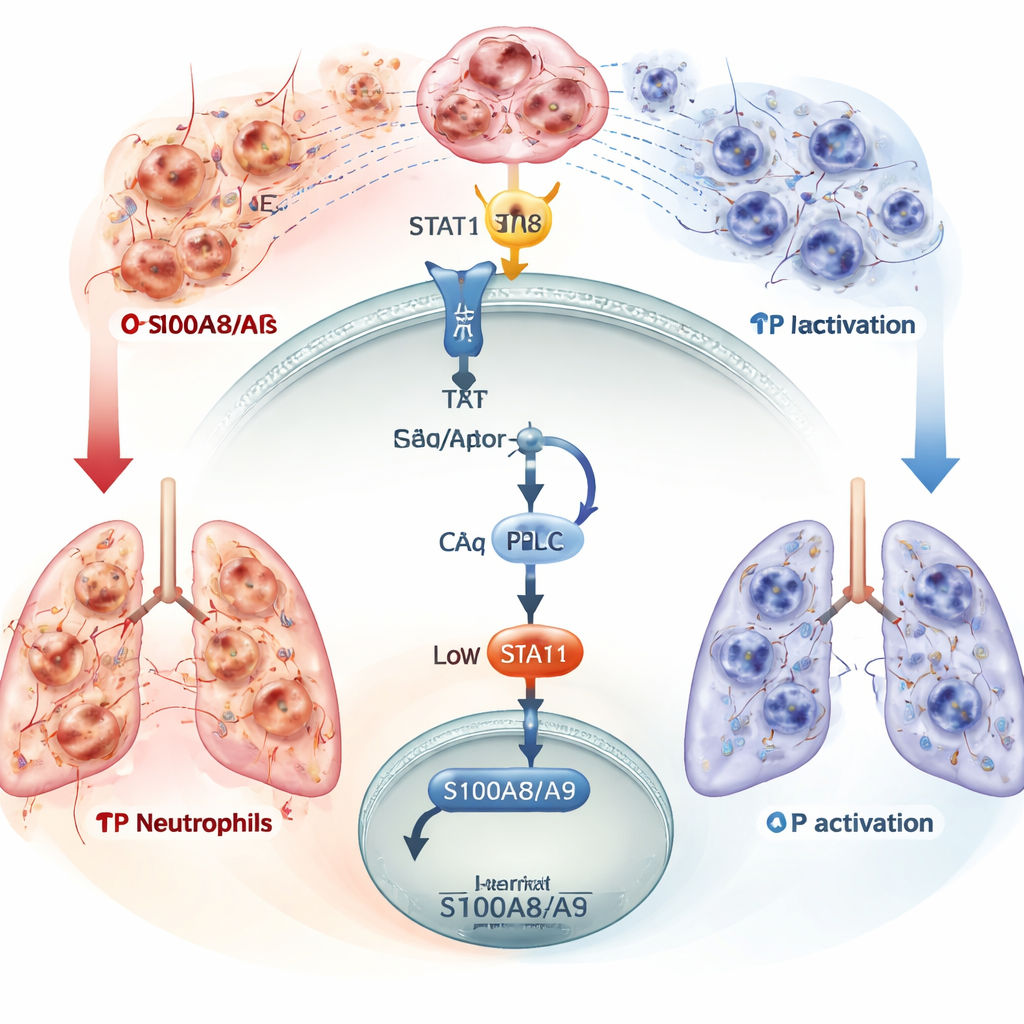
Przekształcanie odkrycia w przyszłe terapie sepsy
Dla czytelnika niebędącego specjalistą główne przesłanie jest takie, że nie każde zapalenie jest złe — ale zbyt intensywne, w niewłaściwym miejscu, może być śmiertelne. Ta praca identyfikuje precyzyjny obwód w komórkach dendrytycznych, który normalnie zapobiega zalewaniu płuc przez neutrofile podczas ciężkiej infekcji. Gdy sygnalizacja TP ustaje, komórki dendrytyczne nadprodukują alarm S100A8/A9, przywołując fale neutrofili, które uszkadzają tkanki zamiast pomagać. Ponowne uruchomienie TP jedynie w komórkach dendrytycznych — lub zablokowanie ścieżki S100A8/A9 — może pozwolić wychłodzić szkodliwą stronę zapalenia, zachowując jednocześnie dużą część zdolności organizmu do walki z infekcją. Choć na razie w modelach zwierzęcych, ta ukierunkowana strategia otwiera obiecujący kierunek dla przyszłych, bardziej precyzyjnych terapii sepsy.
Cytowanie: Du, R., Pan, T., Wang, Y. et al. Thromboxane receptor activation in dendritic cells mitigates sepsis by suppressing S100a8/a9-mediated neutrophil recruitment. Sig Transduct Target Ther 11, 75 (2026). https://doi.org/10.1038/s41392-026-02592-w
Słowa kluczowe: sepsa, komórki dendrytyczne, neutrofile, zapalanie, regulacja odporności