Clear Sky Science · pl
GPR54 reguluje rozwój niedrobnokomórkowego raka płuca poprzez dekarboksylazę dopy (DDC)
Dlaczego ta historia o raku płuca ma znaczenie
Rak płuca pozostaje jednym z najbardziej śmiertelnych nowotworów, a większość przypadków to tzw. niedrobnokomórkowy rak płuca (NSCLC). Wielu pacjentów ostatecznie traci dostęp do skutecznych opcji leczenia, ponieważ guzy adaptują się lub stają się oporne na stosowane leki. W badaniu odkryto wcześniej niedoceniany system kontroli wewnątrz komórek raka płuca, skupiony wokół receptora nazwanego GPR54 oraz enzymu dekarboksylazy dopy (DDC). Zrozumienie, w jaki sposób te molekuły wspierają wzrost i „napędzanie” guzów, wskazuje nowe sposoby spowolnienia lub nawet zmniejszenia NSCLC.
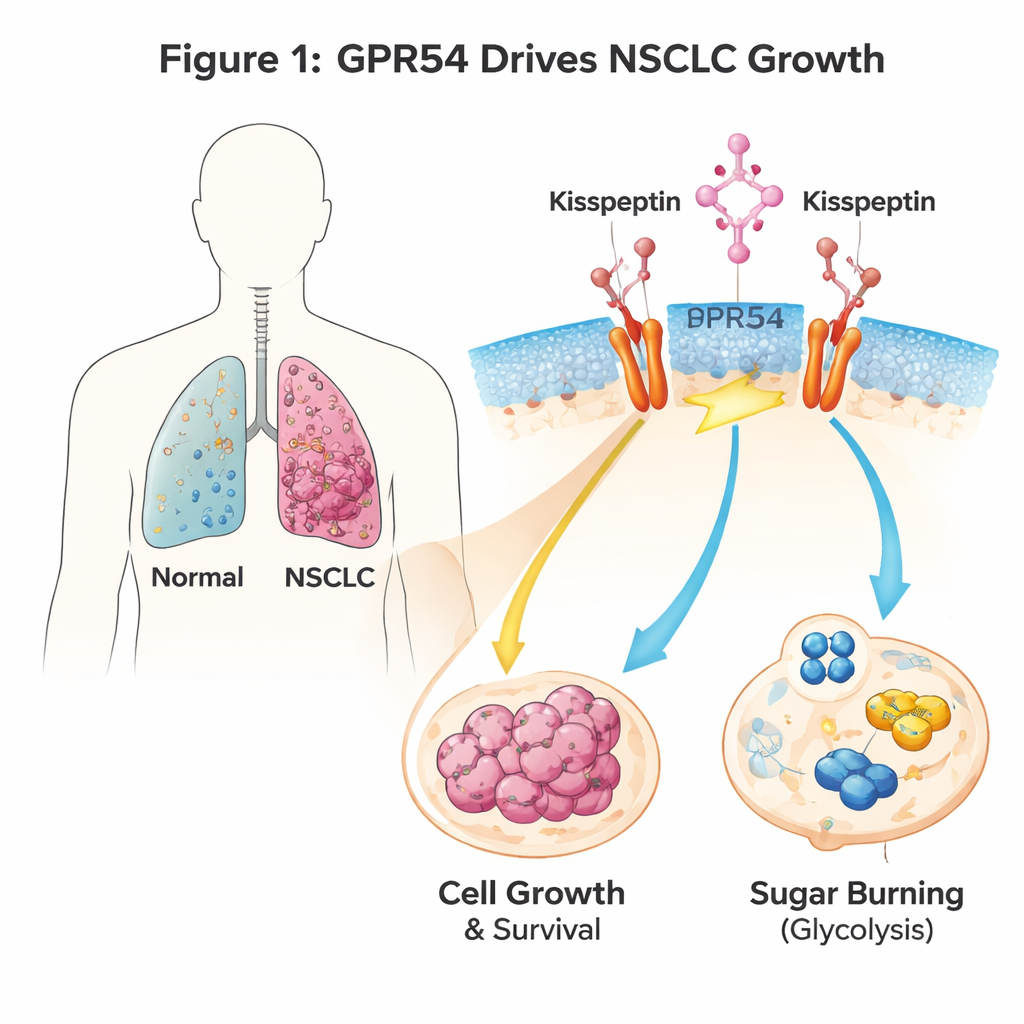
Przełącznik sygnału na komórkach raka płuca
GPR54 to czujnik umieszczony na powierzchni komórek, który reaguje na naturalny sygnał zwany kisspeptyną. Receptor jest najlepiej znany z roli w dojrzewaniu płciowym i rozrodczości, ale pojawia się też w wielu nowotworach. Autorzy użyli genetycznie zmodyfikowanych myszy, które rozwijają NSCLC po aktywacji onkogenu Kras w komórkach płuc. Gdy usunęli gen Gpr54 u tych myszy, zwierzęta żyły dłużej, miały mniej i mniejsze guzy płuc, a komórki nowotworowe wykazywały wyraźne cechy autodestrukcji (apoptozy). Badania na ludzkich liniach komórkowych NSCLC potwierdziły te obserwacje: przy obniżeniu poziomu GPR54 komórki nowotworowe rosły wolniej, tworzyły mniej kolonii i łatwiej ulegały śmierci, niezależnie od ich konkretnych mutacji genetycznych.
Jak GPR54 utrzymuje komórki guza przy życiu
Pogłębiając analizę, badacze sprawdzili, które wewnętrzne obwody wykorzystuje GPR54. Stwierdzili, że GPR54 napędza dwie główne ścieżki wzrostu w komórce, znane jako AKT i ERK. Obie są powszechnymi „węzłami” sygnałowymi, które nakazują komórkom nowotworowym dzielić się i opierać śmierci. Gdy GPR54 był blokowany lub usuwany, aktywność AKT i ERK spadała, a komórki stawały się bardziej podatne na apoptozę. Przywrócenie silnych sygnałów AKT lub ERK mogło częściowo uratować komórki, co potwierdza, że GPR54 pomaga komórkom NSCLC przetrwać, opierając się na tych obwodach wzrostu.
Ponowne okablowanie wykorzystania cukru przez nowotwór
Komórki nowotworowe często przeprogramowują sposób używania składników odżywczych, preferując szybkie rozkładanie cukru (glikolizę) do zasilania wzrostu. Profilowanie aktywności genów w guzach myszy pozbawionych Gpr54 wykazało, że wiele genów zaangażowanych w obsługę cukru i produkcję energii było wyciszonych. W komórkach raka płuca traktowanych kisspeptyną w celu aktywacji GPR54, pomiary zużycia tlenu i produkcji kwasów — będące wskaźnikami metabolizmu energetycznego — ujawniły, że GPR54 zwiększa glikolizę. Blokowanie ścieżki GPR54 na różnych etapach (przełącznik Gαq/11, PI3K, AKT czy mTOR) zmniejszało zużycie glukozy i produkcję mleczanu oraz skłaniało komórki ku apoptozie. Mówiąc wprost, GPR54 pomaga komórkom NSCLC szybciej i wydajniej spalać cukier, wspierając ich szybki wzrost.
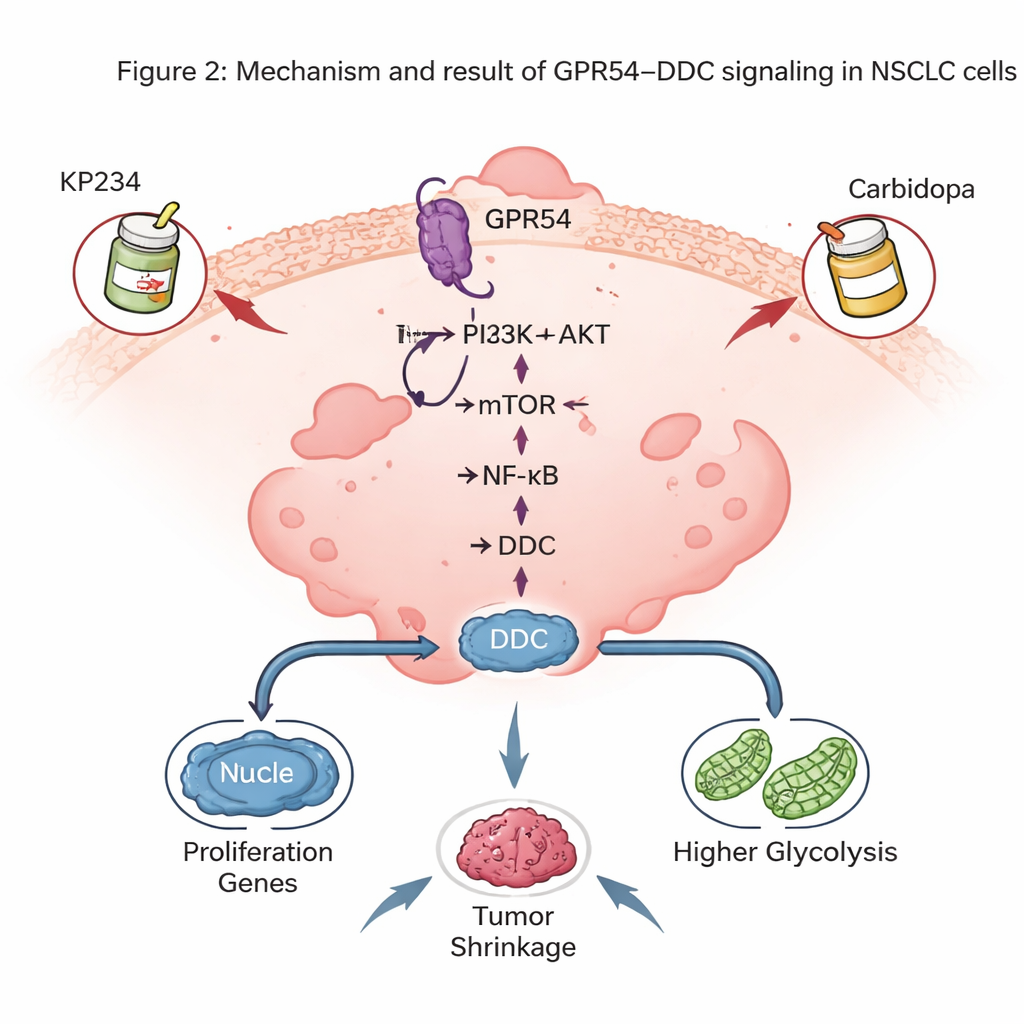
Zaskakująca rola enzymu kojarzonego z mózgiem
Jedno z najbardziej uderzających odkryć to fakt, że GPR54 kontroluje poziomy DDC — enzymu najlepiej znanego z produkcji w mózgu neuroprzekaźników dopaminy i serotoniny. W guzach myszy poziomy DDC ściśle korelowały z ilością GPR54: mniej GPR54 oznaczało mniej DDC. Ludzkie guzy NSCLC i linie komórkowe również wykazywały wyższe poziomy DDC niż normalne komórki płuc, a pacjenci z większą ilością DDC mieli gorsze przeżycia. Obniżenie DDC w komórkach raka płuca spowolniło wzrost guza u myszy, zmniejszyło podziały komórkowe w hodowlach i wywołało więcej apoptozy. Na poziomie molekularnym DDC pomagał utrzymać aktywność ścieżki NF-κB — głównego regulatora promującego przeżycie komórek nowotworowych i stan zapalny — a także wspierał wysoki stan glikolizy komórek nowotworowych.
Testowanie strategii łączenia leków
Ponieważ DDC jest już celem terapii w chorobie Parkinsona w kontekście leku karbidopy, autorzy sprawdzili, czy połączenie blokeru GPR54 (KP234) z karbidopą może zaatakować NSCLC z dwóch stron. W hodowlach komórkowych i w modelach mysich, gdzie ludzkie komórki NSCLC rosły w płucach, podwójne leczenie hamowało wzrost guzów bardziej niż każdy z leków osobno i zwiększało śmierć komórek nowotworowych, bez wyraźnej utraty wagi zwierząt. Te kombinacje wykazywały też obiecujące efekty w zestawieniu z niektórymi nowoczesnymi lekami celowanymi przeciwko zmutowanym genom RAS, co sugeruje, że sygnalizacja GPR54–DDC może zostać nałożona na istniejące terapie precyzyjne.
Co to oznacza dla przyszłej opieki nad rakiem płuca
Dla osoby niebędącej specjalistą kluczowy przekaz jest taki, że komórki NSCLC polegają na wcześniej niedocenianym partnerstwie między powierzchniowym przełącznikiem (GPR54) a enzymem metabolicznym (DDC), aby pozostać przy życiu i szybko spalać paliwo. Zakłócenie tego partnerstwa osłabia guzy, sprawiając, że rosną wolniej i łatwiej ulegają śmierci w modelach eksperymentalnych. Choć przed wprowadzeniem takich strategii do kliniki wciąż wiele pracy, badanie wskazuje GPR54 i DDC jako potencjalne markery biologiczne do identyfikacji agresywnego NSCLC oraz jako obiecujące cele do nowych terapii łącznych, które mogłyby poprawić wyniki u pacjentów, których nowotwory obecnie unikają standardowych terapii.
Cytowanie: Hwang, HH., Lee, S.Y., Lee, C. et al. GPR54 regulates non-small cell lung cancer development via dopa decarboxylase. Sig Transduct Target Ther 11, 74 (2026). https://doi.org/10.1038/s41392-026-02591-x
Słowa kluczowe: niedrobnokomórkowy rak płuca, GPR54, dekarboksylaza dopy, metabolizm nowotworu, terapia celowana