Clear Sky Science · pl
Reaktywne formy tlenu (ROS) w nowotworach: od mechanizmu do implikacji terapeutycznych
Kiedy pomocne molekuły stają się niebezpieczne
W każdej komórce nieustannie powstają maleńkie chemiczne iskry nazywane reaktywnymi formami tlenu, czyli ROS, jako część normalnych procesów życiowych. W odpowiednich stężeniach pomagają komórkom rosnąć, komunikować się i bronić przed drobnoustrojami. Niniejszy przegląd wyjaśnia jednak, jak te same cząsteczki mogą uszkadzać DNA, zniekształcać wewnętrzne połączenia komórkowe i napędzać rozwój nowotworu, jego rozsiew oraz oporność na leczenie. Zrozumienie tej „podwójnej natury” ROS pomaga naukowcom projektować nowe terapie przeciwnowotworowe, które albo łagodzą szkodliwy stres oksydacyjny, albo celowo go zwiększają, by zabić komórki guza.
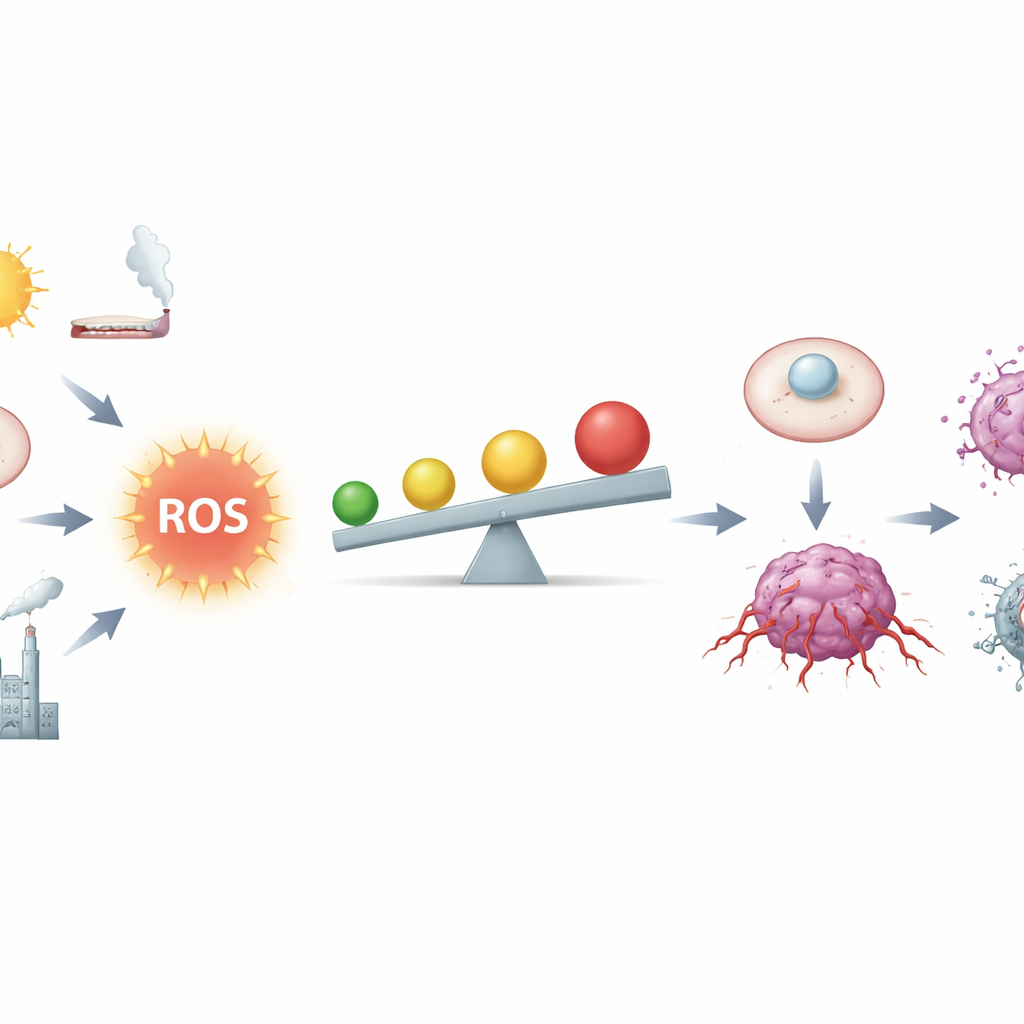
Cienka granica między paliwem a ogniem
Autorzy opisują ROS jako produkty uboczne oddychania i metabolizmu, a jednocześnie jako potężne przekaźniki sygnałowe. W zdrowych tkankach niskie ilości ROS pomagają kontrolować cykl komórkowy, naprawiać uszkodzenia i regulować odporność. Komórki utrzymują tę równowagę dzięki złożonej sieci antyoksydantów, w tym cząsteczek takich jak glutation oraz enzymów kontrolowanych przez główny przełącznik o nazwie Nrf2. Komórki nowotworowe żyją jednak bliżej strefy zagrożenia: uszkodzone geny, nadmiernie pracujące mitochondria, przewlekłe zapalenie, dym tytoniowy, promieniowanie i niektóre metale zwiększają poziom ROS. Przy umiarkowanie podwyższonych stężeniach ROS mogą naciąć DNA, destabilizować chromosomy i przewlekle włączać obwody wzrostu i przeżycia, ułatwiając przemianę komórki prawidłowej w komórkę nowotworową.
Jak stres oksydacyjny kształtuje zachowanie guza
Gdy guz się już uformuje, ROS nadal kształtują jego biologię. Umiarkowany stres oksydacyjny aktywuje liczne szlaki wzrostu, które zachęcają komórki do podziału, pobudzają tworzenie naczyń krwionośnych, inwazję pobliskich tkanek i zwiększają odporność na chemioterapię. ROS mogą przeprogramowywać sposób, w jaki komórki nowotworowe wykorzystują cukry, tłuszcze i aminokwasy, kierując paliwo w szlaki, które produkują dodatkową moc antyoksydacyjną i elementy budulcowe nowych komórek. Wpływają również na decyzje dotyczące losu komórki: w zależności od natężenia i kontekstu ROS mogą przechylić równowagę w stronę sygnałów przeżycia lub w stronę jednego z kilku rodzajów programowanej śmierci komórkowej, w tym klasycznej apoptozy oraz nowszych form, takich jak ferroptoza, nekroptoza i cuproptoza. To sprawia, że ROS są zarówno współwinne postępowi guza, jak i potencjalnymi wyzwalaczami jego autodestrukcji.
Przestawienie układu odpornościowego i odpowiedzi na leki
Przegląd podkreśla, że ROS nie działają wyłącznie wewnątrz komórek nowotworowych — przebudowują też ich otoczenie. Wysoki stres oksydacyjny może wyczerpywać lub zabijać komórki T i komórki NK walczące z rakiem, jednocześnie sprzyjając komórkom supresyjnym, które osłaniają guz przed atakiem. ROS pomagają też guzom zwiększać ekspresję sygnałów „nie zabijaj mnie”, takich jak białka punktów kontrolnych, osłabiając skuteczność immunoterapii. Równocześnie umiarkowane ROS mogą napędzać oporność na leki, zwiększając pompki wypompowujące leki i odpowiedzi na stres, co pozwala komórkom nowotworowym usuwać chemioterapeutyk lub naprawiać wywołane przez niego uszkodzenia. Jednak w innych warunkach przekroczenie krytycznego progu ROS może rozmontować te obrony i ponownie uczulić guzy na leczenie.
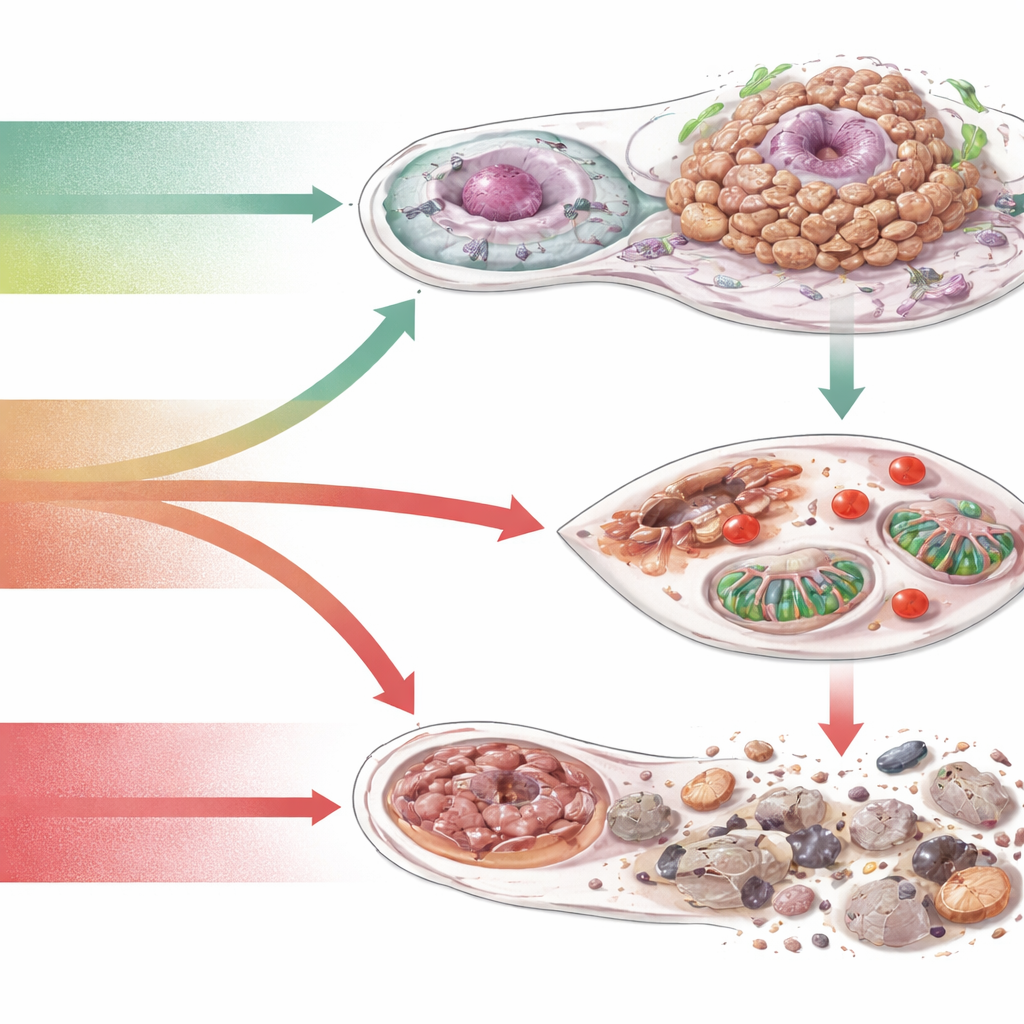
Wykorzystanie słabości redoks jako strategii terapeutycznej
Ponieważ komórki nowotworowe chodzą po cienkiej linie między użytecznością ROS a ich toksycznością, autorzy postrzegają równowagę ROS jako dźwignię terapeutyczną. Jedna szeroka strategia polega na obniżaniu szkodliwych ROS lub wzmacnianiu antyoksydantów — głównie w profilaktyce lub w celu ochrony zdrowych tkanek podczas leczenia. Inna polega na działaniu odwrotnym w guzie: hamowaniu systemów antyoksydacyjnych lub zwiększaniu produkcji ROS aż do momentu, gdy komórki nowotworowe przekroczą śmiertelny próg, szczególnie w połączeniu z radioterapią, lekami ukierunkowanymi lub immunoterapią. Trzecie podejście to pozostawienie poziomów ROS bez zmian, ale zablokowanie konkretnych ROS-czułych przełączników — białek sygnałowych, enzymów metabolicznych czy szlaków śmierci — na których guz polega. Przewija się tu motyw personalizacji: różne nowotwory niosą odmienne „podpisy redoksowe”, więc przyszłe terapie mogą wymagać badań krwi lub tkanki oceniających uszkodzenia oksydacyjne, zdolność antyoksydacyjną i geny związane z ROS, aby dobrać właściwe leczenie ukierunkowane na redoks dla każdego pacjenta.
Co to oznacza dla pacjentów
Mówiąc prosto, artykuł argumentuje, że ROS nie są ani wyłącznie złe, ani wyłącznie dobre; to potężne narzędzia, z których korzystają komórki, w tym komórki nowotworowe. Komórki nowotworowe zwykle funkcjonują bliżej punktu krytycznego stresu oksydacyjnego niż komórki zdrowe, co może tworzyć okno terapeutyczne. Jednak dlatego, że antyoksydanty i prooksydanty mogą pomagać lub szkodzić w zależności od dawki, czasu podania i rodzaju guza, rutynowe stosowanie suplementów lub leków zwiększających ROS jest ryzykowne. Autorzy konkludują, że przyszłość leży w starannie zaprojektowanych terapiach i diagnostyce, które ocenią stan redoksowy każdego guza, a następnie odpowiednio nim pokierują — albo obniżając ROS, aby chronić tkanki zdrowe, albo podnosząc je, by przepchnąć komórki nowotworowe za ich punkt załamania.
Cytowanie: Akter, S., Madhuvilakku, R., Kar, A.K. et al. Reactive oxygen species (ROS) in cancer: from mechanism to therapeutic implications. Sig Transduct Target Ther 11, 111 (2026). https://doi.org/10.1038/s41392-026-02583-x
Słowa kluczowe: reaktywne formy tlenu, stres oksydacyjny, metabolizm nowotworu, terapia redoks, mikrośrodowisko guza