Clear Sky Science · pl
Białko podobne do parathormonu jest celem terapeutycznym w idiopatycznym włóknieniu płuc
Dlaczego bliznowacenie płuc ma znaczenie
Idiopatyczne włóknienie płuc (IPF) to wyniszczająca choroba płuc, w której delikatne pęcherzyki oddechowe stopniowo przekształcają się w sztywne blizny, przez co każdy oddech staje się trudniejszy. Obecne leki mogą spowalniać to bliznowacenie, ale nie potrafią go zatrzymać ani odwrócić. W badaniu tym ujawniono wcześniej niedoceniany czynnik tego procesu: niewielkie, przypominające hormon białko wytwarzane przez komórki wyściełające drogi oddechowe, zwane białkiem podobnym do parathormonu (PTHrP), i wykazano, że blokowanie jego działania może oferować nową drogę leczenia IPF.
Ukryty przekaźnik w drogach oddechowych
IPF od dawna wiązano z nadmiernie aktywnymi fibroblastami — komórkami, które normalnie pomagają w naprawie tkanek, lecz w tej chorobie przechodzą w stan nadmiernej aktywności i odkładają nadmiar kolagenu, głównego składnika blizny. Wiele badań skupiało się na sygnałach pochodzących od komórek układu odpornościowego i z głębszych komórek pęcherzykowych, ale ta praca patrzy wyżej w drzewie oskrzelowym, na przewody, które doprowadzają powietrze do płuc. Ponowna analiza dużych zbiorów danych genetycznych od osób z IPF i bez tej choroby wykazała, że gen o nazwie PTHLH, kodujący PTHrP, był konsekwentnie aktywowany na wyższym poziomie w płucach chorych na IPF. Obrazowanie mikroskopowe próbek ludzkich płuc potwierdziło, że białko PTHrP było znacznie bardziej obfite u pacjentów z IPF i koncentrowało się w komórkach nabłonka oskrzelowego wyściełających drogi oddechowe.
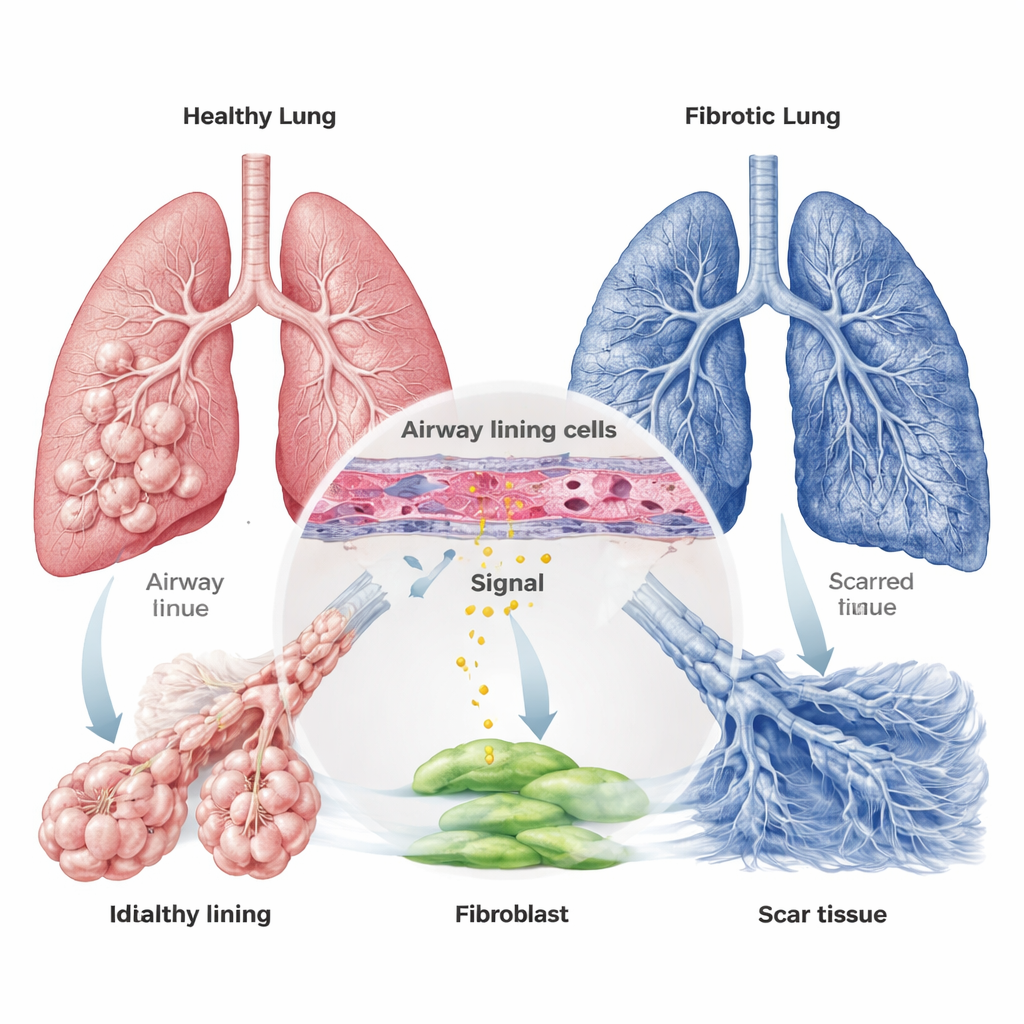
Z sygnału z dróg oddechowych do komórek budujących bliznę
PTHrP powstaje jako większe białko, które może być pocięte na kilka mniejszych fragmentów. Zespół skupił się na jednym fragmencie, PTHrP1-34, znanym z aktywacji receptora na niektórych komórkach. Wykazali, że komórki nabłonka oskrzelowego poddane stresowi — takim jak niskie stężenie tlenu lub ekspozycja na bleomycynę, lek o działaniu podobnym do chemioterapii, często używany do modelowania uszkodzeń płuc u zwierząt — wydzielają do otoczenia więcej PTHrP1-34. Jednocześnie odkryli, że dopasowany receptor, zwany PTH1R, występuje przede wszystkim nie na komórkach wyściełających pęcherzyki, lecz na fibroblastach i komórkach mięśni gładkich. Tworzy to linię komunikacyjną: uszkodzone komórki dróg oddechowych wysyłają PTHrP1-34, a pobliskie fibroblasty są „nastrojone”, by go odbierać.
Jak sygnał zmienia fibroblasty w agresywne
W hodowlach dodanie PTHrP1-34 do ludzkich i mysich fibroblastów płucnych sprawiło, że przyjmowały one bardziej agresywny, sprzyjający bliznowaceniu stan. Zwiększyła się u nich produkcja alfa-aktyny mięśni gładkich (cecha charakterystyczna tzw. miofibroblastów) oraz kluczowych genów kolagenu, a także ich zdolność do migracji — cechy powiązane z postępującym włóknieniem. Testy molekularne wykazały, że dzieje się to przez specyficzną wewnątrzkomórkową drogę: PTHrP1-34 wiąże się z PTH1R na powierzchni fibroblastu, podnosi poziom cząsteczki przekaźnikowej cAMP i aktywuje enzym o nazwie PKA, który następnie włącza „geny włóknienia” w jądrze komórkowym. Zablokowanie receptora lub zahamowanie PKA znacznie zmniejszało tę odpowiedź. Co istotne, komórki nabłonka oskrzelowego i pęcherzykowego nie reagowały w ten sam sposób, co podkreśla, że ten fragment hormonu działa bardzo selektywnie na fibroblasty.
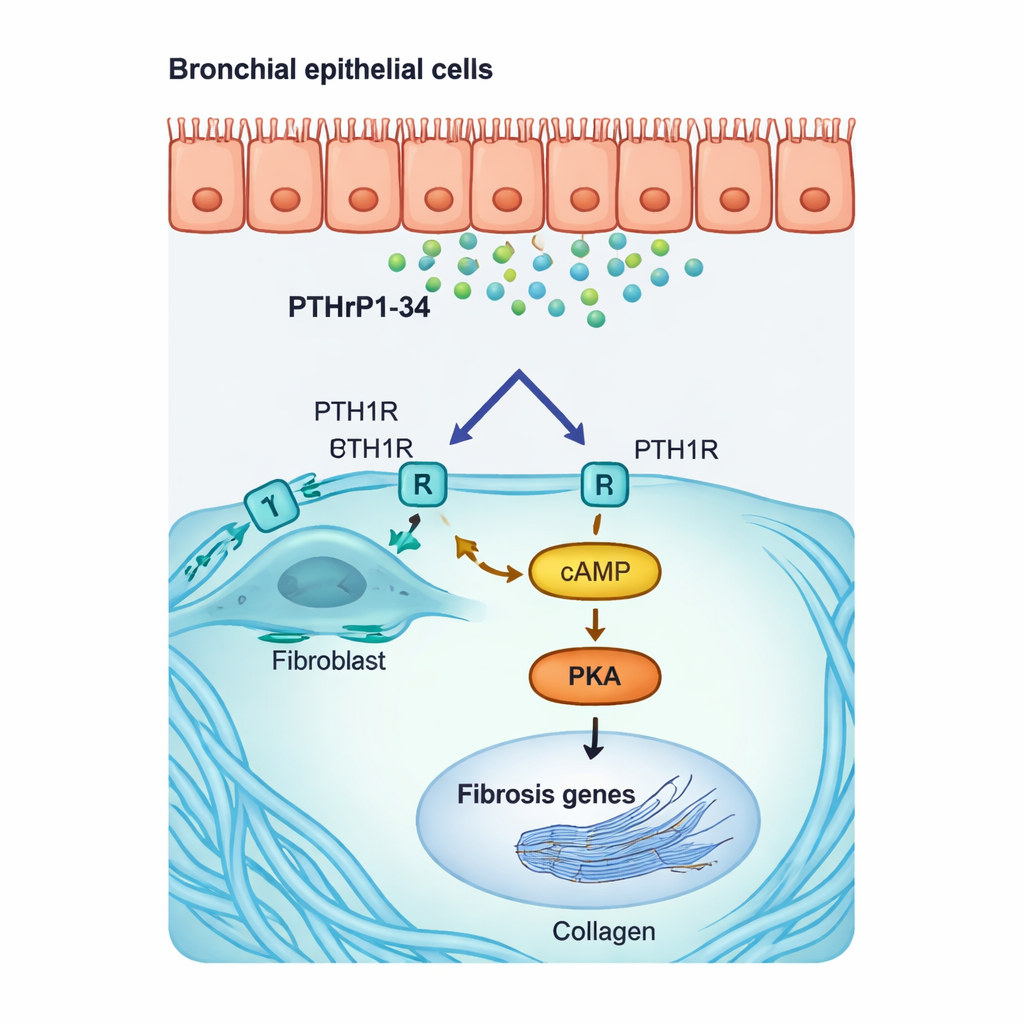
Dowód w chorych płucach i nowe kierunki terapeutyczne
Aby sprawdzić, czy ta droga ma znaczenie w całych płucach, badacze sięgnęli po modele mysie uszkodzenia płuc wywołane bleomycyną. W miarę jak płuca zwierząt przechodziły od wczesnego zapalenia do gęstego włóknienia, poziomy PTHrP1-34 znacznie wzrastały w drogach oddechowych i tkance płucnej, ale nie we krwi, co sugeruje lokalny, specyficzny dla płuc wzrost. Bezpośrednie podanie PTHrP1-34 do dróg oddechowych skłaniało płuca w kierunku stanu włóknienia, a w połączeniu z bleomycyną znacznie pogarszało bliznowacenie i odkładanie kolagenu. Zespół przetestował następnie trzy sposoby przerwania tego szkodliwego sygnału: przeciwciało neutralizujące, które wyłapuje PTHrP1-34, krótki peptyd blokujący jego receptor (PTHrP7-34) oraz podejście wyciszające gen, które obniża produkcję PTHrP w komórkach dróg oddechowych. W każdym z tych przypadków myszy rozwijały mniej włóknienia płuc, miały niższe poziomy kolagenu i utrzymywały lepszą masę ciała, z efektami porównywalnymi lub przewyższającymi działanie nintedanibu, zarejestrowanego leku na IPF.
Co to oznacza dla przyszłej opieki
Dla osób niezajmujących się specjalistycznie medycyną kluczowy wniosek jest taki, że nabłonek oskrzelowy nie jest tylko biernym przewodem dla powietrza; może aktywnie napędzać bliznowacenie płuc, wysyłając silne sygnały chemiczne. Badanie identyfikuje PTHrP1-34 jako jeden z takich komunikatów i wykazuje, że blokowanie jego „rozmowy” z fibroblastami może spowolnić, a nawet odwrócić włóknienie w modelach zwierzęcych. Choć potrzeba więcej badań, by potwierdzić bezpieczeństwo i skuteczność u ludzi, celowanie w ścieżkę PTHrP1-34/PTH1R mogłoby dodać całkowicie nową klasę terapii dla IPF, mającą na celu nie tylko spowolnienie choroby, lecz także atakowanie jednego z jej istotnych mechanizmów.
Cytowanie: Fang, XQ., Lim, S., Lee, YM. et al. Parathyroid hormone–related protein is a therapeutic target in idiopathic pulmonary fibrosis. Sig Transduct Target Ther 11, 67 (2026). https://doi.org/10.1038/s41392-026-02578-8
Słowa kluczowe: idiopatyczne włóknienie płuc, włóknienie płuc, białko podobne do parathormonu, aktywacja fibroblastów, nabłonek oskrzelowy