Clear Sky Science · pl
Konsensusowe molekularne podtypy raka płaskonabłonkowego przełyku
Dlaczego te badania są ważne dla pacjentów
Rak płaskonabłonkowy przełyku to śmiertelny nowotwór gardełkowy o ograniczonych możliwościach leczenia ukierunkowanego i zwykle złym rokowaniu. Lekarze wiedzą, że nie wszystkie guzy zachowują się tak samo, lecz dotychczas brakowało przejrzystego, ujednoliconego sposobu podziału tych nowotworów na biologicznie sensowne grupy. Badanie to łączy wiele rodzajów danych genetycznych i obrazowych, aby zdefiniować cztery główne typy tego raka i pokazuje, że prosty obraz ze szkiełka mikroskopowego często potrafi ujawnić, do którego typu należy pacjent. To otwiera drogę do bardziej precyzyjnego leczenia, zamiast metod prób i błędów.
Porządkowanie skomplikowanego krajobrazu choroby
W ciągu ostatniej dekady różne zespoły badawcze zaproponowały co najmniej siedem sposobów podziału tego nowotworu w oparciu o mutacje DNA, zmiany liczby kopii, aktywność genów czy inne pomiary molekularne. Każdy system wykorzystywał inne dane i metody, co prowadziło do pokrywających się, lecz nieidentycznych podtypów i utrudniało stosowanie ich w praktyce klinicznej. Autorzy najpierw ponownie przeanalizowali dobrze scharakteryzowaną grupę 152 chińskich pacjentów, dla których dostępne były wielowarstwowe dane, w tym sekwencjonowanie całego genomu, aktywność genów, metylacja DNA i profile mikroRNA. Przy użyciu metody zwanej similarity network fusion połączyli wszystkie te dane w jedną całość i zidentyfikowali cztery podtypy multi‑omics. Następnie zbudowali statystyczną „sieć podtypów”, która powiązała ich nowe grupy z 21 wcześniej opublikowanymi, ujawniając silne powiązania między studiami.
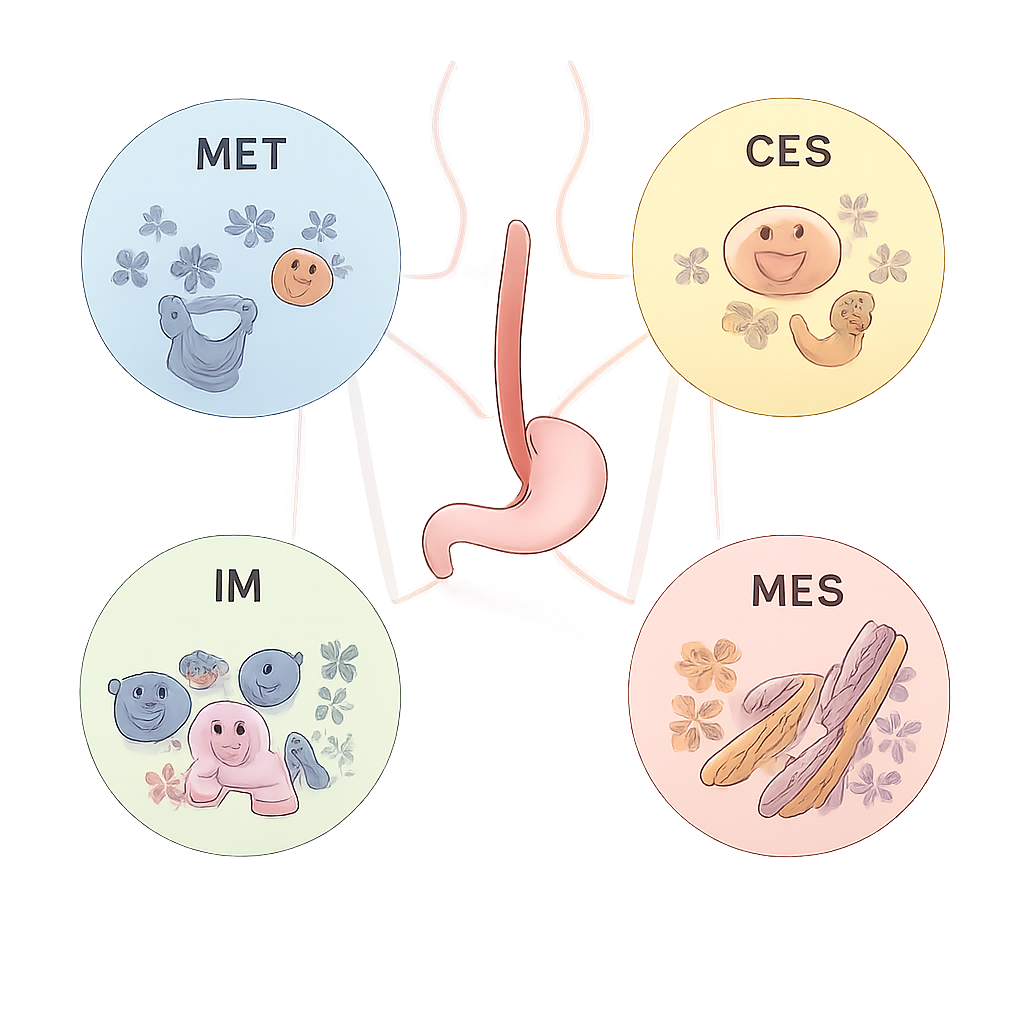
Cztery główne biologiczne „osobowości” guza
Z tej sieci zespół wyodrębnił cztery konsensusowe molekularne podtypy nazwane ECMS1 do ECMS4, z wyraźnie odmiennym zachowaniem. ECMS1, typ metaboliczny (MET), wykazuje silną aktywność szlaków przetwarzających leki i substancje odżywcze oraz częstą aktywację genu NFE2L2, co może napędzać oporność na chemioterapię i radioterapię. ECMS2, typ klasyczny (CLS), charakteryzuje się dominującą aktywnością cyklu komórkowego i sygnałów wzrostu, często z dodatkowymi kopiami genu ERBB2 (HER2). ECMS3, typ immunologiczny (IM), ma niższe ogólne obciążenie mutacjami, ale silnie aktywowany układ odpornościowy, w tym wysoki poziom ścieżki kontroli immunologicznej PD‑1. ECMS4, typ mezenchymalny (MES), wykazuje cechy przebudowy tkanki, tworzenia naczyń krwionośnych oraz zwiększonej ruchliwości i inwazyjności komórek — cechy powiązane z gorszymi wynikami.
Powiązanie podtypów z rokowaniem i wyborem leczenia
Porównanie tych czterech grup z danymi klinicznymi pacjentów ujawniło wyraźne wzorce. Pacjenci z guzami mezenchymalnymi ECMS4 mieli najwyższe ryzyko nawrotu oraz najgorsze przeżycia ogólne i wolne od choroby. Grupa immunologiczna ECMS3, mimo aktywnego środowiska odpornościowego, słabo reagowała na standardową chemioradioterapię, ale wykazywała wyższy odsetek korzyści z leków przeciw PD‑1. Guzy klasyczne ECMS2 wydawały się bardziej wrażliwe na powszechnie stosowane chemioterapeutyki, takie jak cisplatyna i taksany, a częsta amplifikacja HER2 sugeruje, że mogą skorzystać z leków ukierunkowanych na HER2. Guzy metaboliczne ECMS1, wzbogacone w aktywność NFE2L2 i niektóre receptory czynników wzrostu, mogą lepiej reagować na leki celowane w ścieżki metaboliczne i sygnałowe. Krótko mówiąc, cztery podtypy wskazują na różne słabe punkty i różne prawdopodobne odpowiedzi na terapię.
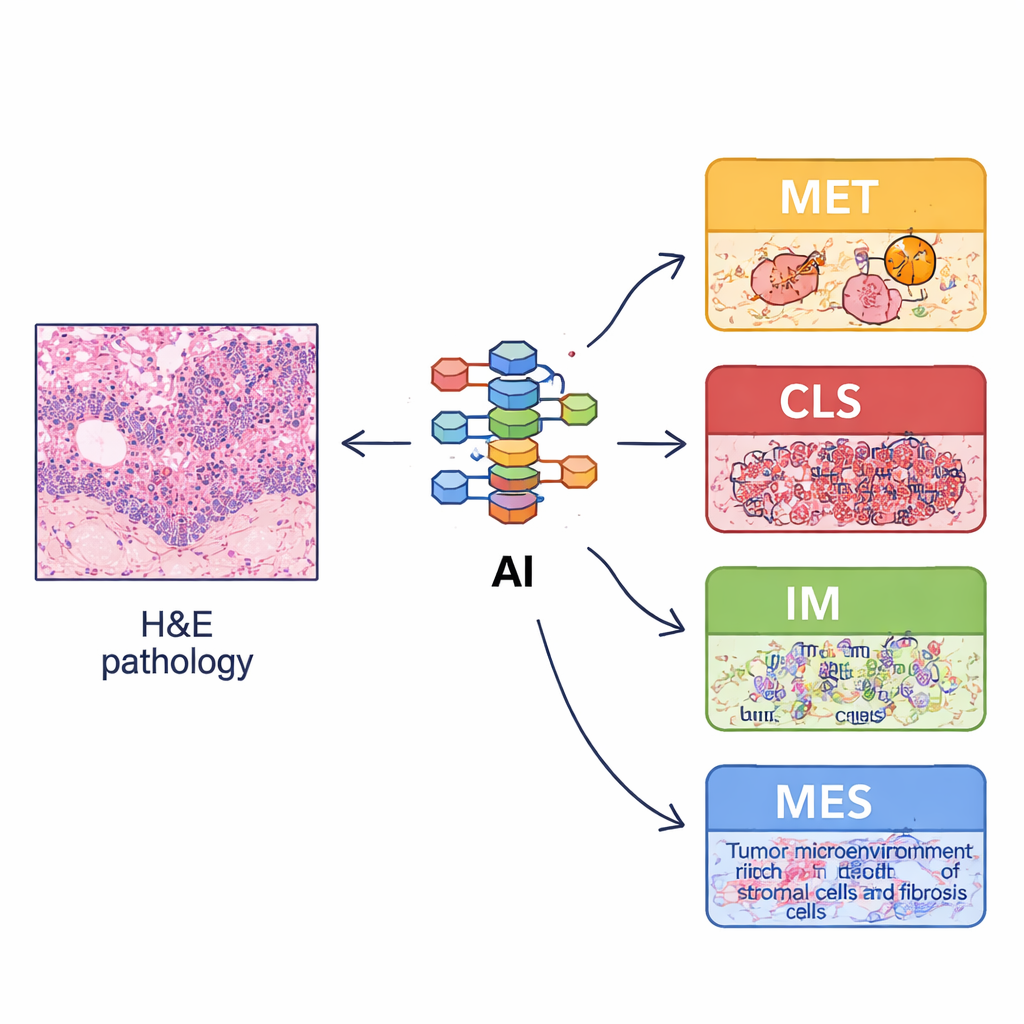
Nauka komputera rozpoznawania molekularnych wskazówek na rutynowych preparatach
Ponieważ pełne profilowanie molekularne jest kosztowne i niedostępne w wielu szpitalach, zespół sprawdził, czy zwykłe preparaty hematoksyliną i eozyną (H&E) mogą posłużyć jako substytut. Przeszkolili system uczenia głębokiego na dziesiątkach tysięcy oznaczonych fragmentów obrazów, aby rozpoznawać podstawowe elementy tkanki, takie jak komórki guza, zrąb, limfocyty, gruczoły i mięśnie. Z całościowych obrazów ze szkiełek obliczali następnie „cechy organizacji przestrzennej” – ile każdego typu tkanki występuje, jak są rozmieszczone i jak bardzo są wymieszane lub odseparowane. Wzorce wyprowadzane z obrazów odzwierciedlały biologię czterech podtypów: na przykład typ immunologiczny ECMS3 miał więcej limfocytów i zachowanych struktur, natomiast typ mezenchymalny ECMS4 wykazywał więcej wspierającego zrębu. Wykorzystując te cechy, zbudowali klasyfikator oparty na obrazach, nazwany imECMS, który potrafił przypisywać preparaty do MET, CLS, IM lub MES z dobrą dokładnością w kilku niezależnych kohortach pacjentów.
Co to oznacza dla przyszłej opieki
Dla osób niezwiązanych ze specjalistyczną medycyną wnioskiem jest to, że badanie to przekształca pozornie jednorodny nowotwór w cztery biologicznie odrębne choroby, z odmiennym przebiegiem i najlepszymi strategiami leczenia dla każdej z nich. Co istotniejsze, pokazuje, że dużą część tych informacji można wydobyć automatycznie z rutynowych obrazów mikroskopowych, które posiada każdy pacjent, bez potrzeby kosztownego sekwencjonowania. Po dalszej walidacji w większych i bardziej zróżnicowanych populacjach systemy ECMS i imECMS mogłyby pomóc lekarzom dopasować pacjentów z rakiem płaskonabłonkowym przełyku do terapii, z których najprawdopodobniej odniesie korzyść, jednocześnie oszczędzając im leczeń mało skutecznych.
Cytowanie: Cui, H., Zhu, Z., Xu, E. et al. The consensus molecular subtypes of esophageal squamous cell carcinoma. Sig Transduct Target Ther 11, 65 (2026). https://doi.org/10.1038/s41392-026-02577-9
Słowa kluczowe: rak przełyku, podtypy guza, precyzyjna onkologia, patologia z użyciem uczenia głębokiego, immunoterapia