Clear Sky Science · pl
Hiperglutaminoliza napędza starzenie i senescencję poprzez aktywację osi arginina–mTORC1
Dlaczego te badania mają znaczenie dla zdrowego starzenia się
Starzenie to nie tylko zmarszczki i siwe włosy — to proces, w którym komórki w całym ciele stopniowo tracą zdolność do naprawy i odnowy. To badanie zadaje przewrotnie proste pytanie o dalekosiężnych konsekwencjach: czy sposób, w jaki komórki spalają aminokwas glutaminę, rzeczywiście sprzyja przejściu w stan starości? Autorzy odkrywają dotąd ukryty łańcuch metaboliczny łączący przetwarzanie glutaminy z potężnym przełącznikiem wzrostu mTORC1 i pokazują, że nadmierne uruchomienie tej ścieżki może aktywnie przyspieszać starzenie komórek u muszek i myszy.
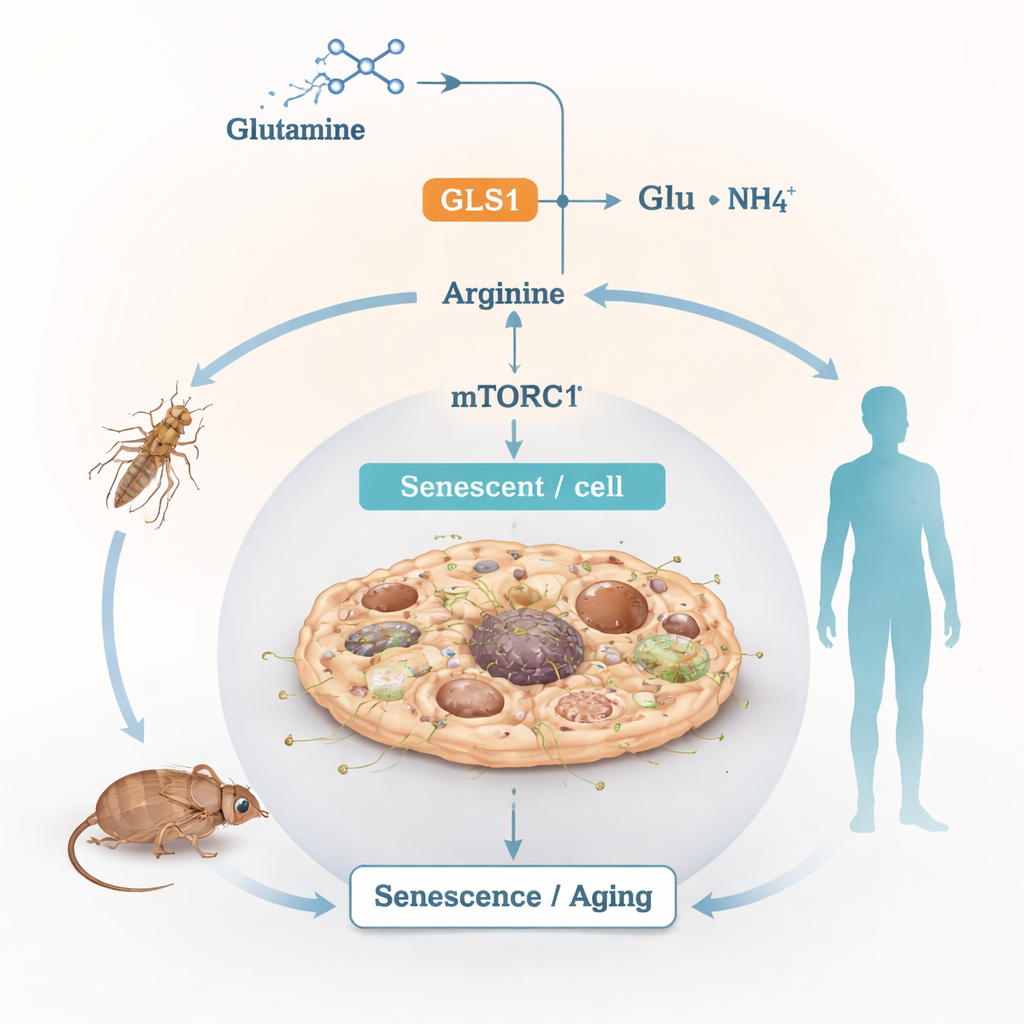
Linia paliwowa pracująca zbyt intensywnie
Glutamina jest najobficiej występującym wolnym aminokwasem we krwi i tkankach. Komórki wykorzystują ją jako wszechstronne paliwo i budulec, rozkładając ją przez proces zwany glutaminolizą. Pierwszy krok katalizuje enzym GLS1, który przekształca glutaminę w glutaminian i amoniak; produkty te następnie zasilają produkcję energii, mechanizmy antyoksydacyjne i syntezę innych aminokwasów. Choć rozkład ten jest kluczowy dla normalnego funkcjonowania, autorzy zastanawiali się, co się dzieje, gdy staje się przewlekle nadmierny w kontekście starzenia i stresu.
Odkrycie „hiperglutaminolizy” w starych komórkach i organizmach
Wykorzystując zaawansowane profilowanie metabolitów, zespół porównał młode, dzielące się komórki z komórkami senescentnymi — starszymi komórkami, które przestały się dzielić i wydzielają czynniki zapalne. Stwierdzili, że wiele aminokwasów jest podwyższonych, a glutamina znajduje się w centrum przestawionej sieci. Komórki senescentne wykazywały większe zużycie glutaminy, wyższe poziomy i aktywność GLS1 oraz akumulację glutaminianu i amoniaku. Podobne zmiany zaobserwowano w całych organizmach: postarzałe muszki owocowe i stare myszy miały zwiększoną aktywność GLS w wielu tkankach. Autorzy nazwali ten wspólny stan nasilonego rozkładu glutaminy „hiperglutaminolizą”, sugerując, że jest to zachowana cecha starzenia, a nie drobny efekt uboczny.
Ograniczenie rozkładu glutaminy spowalnia oznaki starzenia
Jeśli hiperglutaminoliza towarzyszy starzeniu, czy rzeczywiście je napędza? Aby to sprawdzić, badacze zablokowali glutaminolizę na kilka sposobów: obniżając glutaminę w pożywce, hamując GLS za pomocą leków lub genetycznie zmniejszając poziom GLS1. W komórkach poddanych stresowi lub replikacyjnie postarzałych te interwencje zmniejszały klasyczne markery senescencji, takie jak barwienie SA-β-gal, inhibitor cyklu komórkowego p16 oraz zapalne sygnały „SASP”. U muszek owocowych zarówno wyciszenie genetyczne GLS, jak i niskodawkowe leki blokujące GLS wydłużały życie, poprawiały zdolność wspinaczkową (test witalności) i zmniejszały wiekowe przeciekanie jelit. Co ważne, gdy ograniczenie glutaminolizy zastosowano od początku ekspozycji na stres, efekt nie wynikał głównie z eliminacji starych komórek, lecz z zapobiegania ich wejściu w stan senescencji.
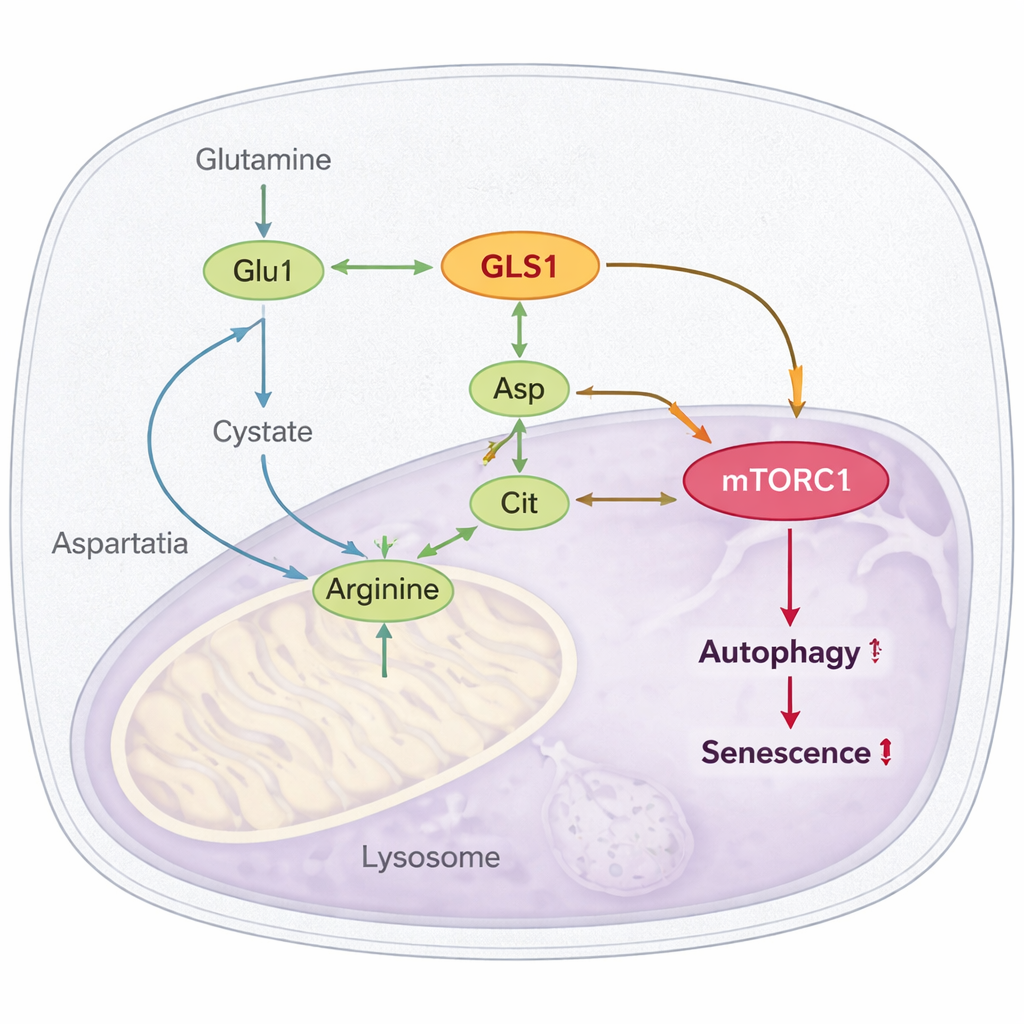
Ukryte połączenie: od glutaminy przez argininę do mTORC1
Najbardziej uderzające jest to, jak ta nadmierna ścieżka łączy się z mTORC1, głównym regulatorem, który przy przewlekłej aktywacji sprzyja starzeniu i blokuje komórkowe sprzątanie (autofagię). Autorzy pokazują, że hiperglutaminoliza zwiększa produkcję argininy, innego aminokwasu, który bezpośrednio aktywuje mTORC1. Glutaminian i amoniak powstające z glutaminy zasilają syntezę asparaginianu i cytruliny, które następnie łączą się w argininę. W starych komórkach i muszkach poziomy argininy i jej prekursorów rosną; blokowanie GLS lub wyciszenie kluczowego enzymu syntezy argininy (ASL) obniża argininę i tłumi aktywność mTORC1. Dodatkowo wykazano, że białko sensoryczne argininy CASTOR1 jest wymagane dla tego efektu: gdy CASTOR1 jest wyłączony, blokowanie glutaminolizy przestaje uspokajać mTORC1 i poprawiać autofagię, a ulga w senescencji zanika.
Kiedy zbyt wiele dobrego przyspiesza starzenie
Aby sprawdzić, czy samo zwiększenie aktywności tej ścieżki przyspiesza starzenie, zespół przez tygodnie zasilał zdrowe komórki dużymi ilościami glutaminy, argininy lub kombinacjami pośrednich metabolitów. Efektem był wyraźny wzrost markerów senescencji i genów zapalnych. U muszek długotrwałe suplementowanie dodatkową glutaminą lub argininą skróciło średnią i maksymalną długość życia. W sumie praca opisuje pełną kaskadę: nadmiar rozkładu glutaminy (hiperglutaminoliza) zwiększa produkcję argininy, która jest wykrywana przez CASTOR1, utrzymuje mTORC1 w stanie nadmiernej aktywności, hamuje komórkowe sprzątanie i sprzyja senescencji oraz starzeniu organizmu.
Co to oznacza dla przyszłych strategii przeciwstarzeniowych
Dla osób niebędących specjalistami badanie to przedefiniowuje metabolizm glutaminy jako broń obosieczną: niezbędny dla zdrowia, lecz potencjalnie szkodliwy, gdy jest przewlekle nadaktywny w średnim i późnym życiu. Mapując konkretną drogę od katabolizmu glutaminy do nadaktywacji mTORC1, autorzy wskazują nowe punkty interwencji — takie jak enzymy GLS1 i ASL czy etap wykrywania argininy — które mogłyby być modulowane, aby spowolnić wiekowy spadek funkcji bez całkowitego wyłączania kluczowego metabolizmu. Choć jest jeszcze zbyt wcześnie, by przekładać te wyniki na zalecenia dietetyczne czy terapie, praca dokłada istotny element do układanki, jak codzienne przetwarzanie składników odżywczych może przesuwać nasze komórki w stronę odporności albo przyspieszonego starzenia.
Cytowanie: Chen, H., Huang, N., Xu, W. et al. Hyperglutaminolysis drives senescence and aging through arginine-mTORC1 axis activation. Sig Transduct Target Ther 11, 64 (2026). https://doi.org/10.1038/s41392-026-02576-w
Słowa kluczowe: metabolizm glutaminy, senescencja komórkowa, sygnalizacja mTORC1, biosynteza argininy, interwencje przeciwstarzeniowe