Clear Sky Science · pl
Egzogenne białko jądrowe wirusa Epstein–Barra 1 wywołuje oporność nowotworu na immunoterapię napędzaną przez ADAR1
Dlaczego powszechny wirus ma znaczenie dla leczenia raka
Wiele nowotworów leczy się dziś lekami immunoterapeutycznymi, które uwalniają własny układ odpornościowy pacjenta. Mimo to większość chorych nadal nie odnosi korzyści, ponieważ ich guzy uczą się ukrywać przed atakiem immunologicznym. Badanie to ujawnia, jak bardzo powszechny wirus — Epstein–Barra (EBV) — pomaga guzom wyłączać mechanizmy odpornościowe i opierać się tym potężnym lekom — oraz jak nowy typ zaprojektowanej cząsteczki może ponownie uruchomić te mechanizmy.
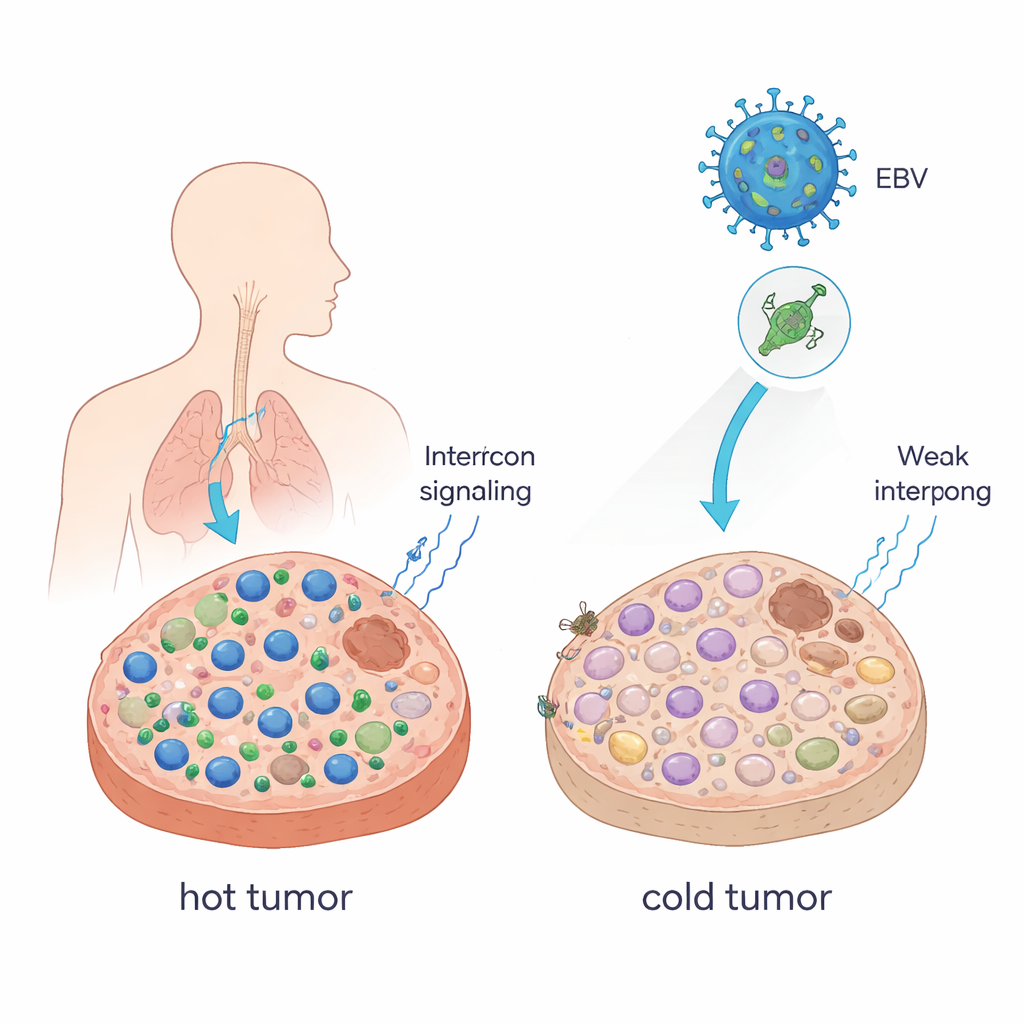
Zmiana gorących guzów w zimne
Lekarze często opisują guzy jako „gorące”, gdy są pełne komórek T zabijających komórki nowotworowe, oraz „zimne”, gdy tych komórek brakuje. Gorące guzy zwykle dobrze reagują na blokadę punktów kontrolnych immunologicznych (ICB), taką jak przeciwciała przeciw PD-1; guzy zimne często nie reagują. Autorzy wykazali, że pojedyncze białko EBV, nazywane EBNA1, może przesunąć guzy w kierunku stanu chłodniejszego i bardziej unikającego wykrycia. Gdy zmusili mysie komórki nowotworowe do produkcji EBNA1 i hodowali je w myszach z nienaruszonym układem odpornościowym, guzy stały się większe, zawierały mniej komórek CD8+ T oraz komórek NK, a więcej makrofagów o działaniu immunosupresyjnym. Sygnały zwane interferonami — kluczowymi przekaźnikami mobilizującymi komórki odpornościowe — były także silnie zredukowane. W próbkach od pacjentów z rakiem nosogardzieli, nowotworem ściśle związanym z EBV, guzy ekspresjonujące EBNA1 również wykazywały mniej komórek CD8+ T w porównaniu z tkanką zdrową.
Wirusowe skrócenie drogi do komórkowej machinerii kontroli RNA
Aby zrozumieć, jak EBNA1 przekształca środowisko guza, badacze poszukiwali ludzkich białek, które fizycznie z nim współdziałają. Skoncentrowali się na białku IGF2BP3, które rozpoznaje drobne chemiczne znaki (m6A) na mRNA i może zwiększać ich stabilność lub tłumaczenie na białko. EBNA1 ściśle wiązał się z IGF2BP3 w kilku typach komórek, w tym w komórkach nowotworowych pozytywnych na EBV. Dane z guzów pacjentów pokazały, że wysoki poziom IGF2BP3 szedł w parze ze słabą aktywnością genów związanych z interferonami i niższą infiltracją komórek CD8+ T, co sugeruje, że sojusz wirus–gospodarz może tłumić odporność przeciwnowotworową.
Wzmocnienie edytora RNA, który ucisza sygnały zagrożenia
Bardziej szczegółowa analiza wyróżniła jeden kluczowy cel tej interakcji: ADAR1, enzym edytujący dwuniciowe RNA przez zamianę niektórych liter „A” na „I”. Taka edycja może sprawić, że wirusopodobne RNA wewnątrz komórek będzie wyglądać na mniej niebezpieczne dla wewnętrznych czujników, zmniejszając odpowiedzi interferonowe. Autorzy odkryli, że EBNA1, IGF2BP3 i czynnik translacyjny EIF4G1 tworzą trójskładnikowy kompleks na mRNA ADAR1. Kompleks ten zwiększa znakowanie m6A, rekrutuje maszynerię translacyjną i selektywnie zwiększa produkcję białka ADAR1 bez podnoszenia poziomu jego mRNA. W rezultacie komórki nowotworowe wykonują więcej edycji RNA w powtarzalnych elementach genetycznych znajdujących się w pobliżu genów związanych z interferonami. Te edycje zmniejszają pulę nieedytowanego dwuniciowego RNA, który normalnie alarmowałby czujniki takie jak MDA5 i PKR, tłumiąc produkcję interferonu i pomagając guzom ukryć się przed atakiem immunologicznym.
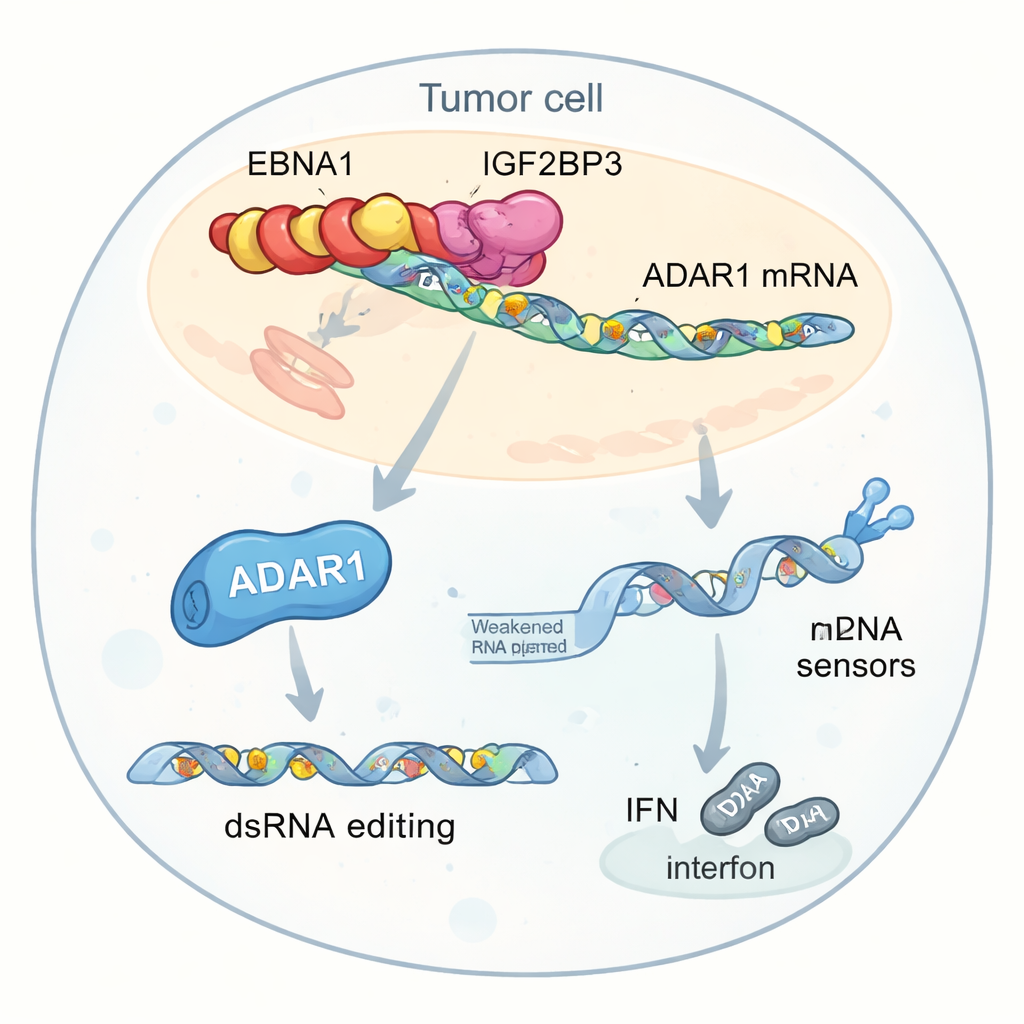
Mniej interferonu, słabsza immunoterapia
Gdy komórki nowotworowe ekspresjonujące EBNA1 były eksponowane na komórki T i przeciwciała przeciw PD-1 w warunkach laboratoryjnych, były trudniejsze do zabicia niż komórki kontrolne i wydzielały mniej interferonu. Nawet po bezpośrednim leczeniu interferonem, komórki posiadające EBNA1 były mniej wrażliwe, a ich wewnętrzne czujniki RNA były słabiej aktywowane. Obniżenie poziomów ADAR1 częściowo odwracało te efekty, przywracając aktywność czujników i sygnalizację interferonową. Eksperymenty genetyczne i sekwencjonowanie potwierdziły, że komórki ekspresjonujące EBNA1 wykazywały więcej zdarzeń A-do-I w określonych regionach RNA, szczególnie po stymulacji interferonem, co dodatkowo wspiera tezę, że wirusowe wzmocnienie ADAR1 pomaga neutralizować sygnały zagrożenia, które w przeciwnym razie wywołałyby silne odpowiedzi immunologiczne.
Projektowany degrader, który na nowo budzi atak odpornościowy
Zespół zapytał następnie, czy pozbawienie guzów EBNA1 może przywrócić ich podatność na immunoterapię. Zaprojektowali cząsteczkę typu PROTAC, EP-1215, która znakowała EBNA1 do zniszczenia przez system utylizacji komórkowej. Przy niskich dawkach EP-1215 skutecznie degradował EBNA1 i obniżał poziomy białka ADAR1. W doświadczeniach na myszach EP-1215 sam w sobie miał ograniczony wpływ na guzy pozytywne na EBNA1, podobnie jak pojedyncze podanie przeciwciała przeciw PD-1. Jednak w połączeniu oba leczenia gwałtownie zmniejszały guzy, zwiększały infiltrację komórek CD8+ T i podnosiły liczbę komórek T produkujących interferon. W modelach myszy humanizowanych, niosących ludzkie komórki odpornościowe i guzy związane z EBV, połączenie ponownie przewyższało terapie pojedyncze, bez oczywistej toksyczności wątroby czy nerek.
Co to oznacza dla przyszłej opieki onkologicznej
Dla odbiorców niebędących specjalistami przesłanie jest takie: powszechny wirus może po cichu przepiształcać komórki nowotworowe, aby stłumić wewnętrzne systemy alarmowe, wyłączając chemiczne sygnały, które w przeciwnym razie przyciągnęłyby i aktywowały komórki odpornościowe. EBNA1 robi to, przejmując czytnik RNA gospodarza (IGF2BP3) oraz czynnik translacyjny (EIF4G1), by nadprodukcją zwiększyć edytor RNA ADAR1, który usuwa struktury RNA, do których zbudowane są czujniki immunologiczne. Poprzez degradację EBNA1 za pomocą dostosowanego PROTAC-a takiego jak EP-1215, autorzy byli w stanie przywrócić te sygnały zagrożenia i ponownie uczynić oporne guzy podatnymi na istniejące leki blokujące punkty kontrolne. Jeśli podobne strategie okażą się bezpieczne i skuteczne u ludzi, celowanie w pomocników wirusowych, takich jak EBNA1, może zaoferować nowy sposób przekształcania zimnych, powiązanych z EBV guzów w gorące cele, na które nowoczesne immunoterapie będą mogły skutecznie oddziaływać.
Cytowanie: Liu, C., Sun, Z., Li, C. et al. Exogenous Epstein–Barr virus nuclear antigen 1 induces ADAR1-driven tumor resistance against immunotherapy. Sig Transduct Target Ther 11, 63 (2026). https://doi.org/10.1038/s41392-026-02574-y
Słowa kluczowe: wirus Epstein–Barra, oporność na immunoterapię, ADAR1, edycja RNA, rak nosogardzieli