Clear Sky Science · pl
Mechanizm molekularny zależnej od cholesterolu fuzji błon podczas wejścia SARS-CoV-2
Dlaczego cholesterol ma znaczenie dla wirusa oddechowego
Wirus wywołujący COVID-19, SARS-CoV-2, przedostaje się do naszych komórek poprzez zlanie swojej zewnętrznej otoczki z błonami komórkowymi. Artykuł stawia pozornie proste pytanie o daleko idących konsekwencjach: w jakim stopniu cholesterol — tłuszczowa substancja znana głównie z chorób serca — kształtuje etap fuzji? Autorzy pokazują, że cholesterol w błonie wirusa nie tylko subtelnie wpływa na wydajność zakażenia; faktycznie pomaga uporządkować białka kolca w potężne platformy dokujące, które ułatwiają i zwiększają niezawodność wejścia.
Budowa minimalnego modelu wejścia wirusa
Aby rozłożyć ten proces na czynniki, badacze odtworzyli spotkanie wirusa z komórką w probówce, używając małych pęcherzyków tłuszczowych zwanych liposomami. Jedna pula liposomów niosła białko kolca SARS-CoV-2 i zastępowała błonę wirusa; druga zawierała receptor ACE2, naśladując powierzchnię komórki gospodarza. Po zmieszaniu i aktywacji przez specyficzne enzymy, które „tną” kolca do formy gotowej do fuzji, te sztuczne błony zlewają się, pozwalając barwnikowi fluorescencyjnemu przejść z jednego pęcherzyka do drugiego. Ten uproszczony układ pozwolił zespołowi precyzyjnie regulować skład lipidowy — w tym poziomy cholesterolu — po każdej stronie i obserwować, jak fuzja przebiega krok po kroku. 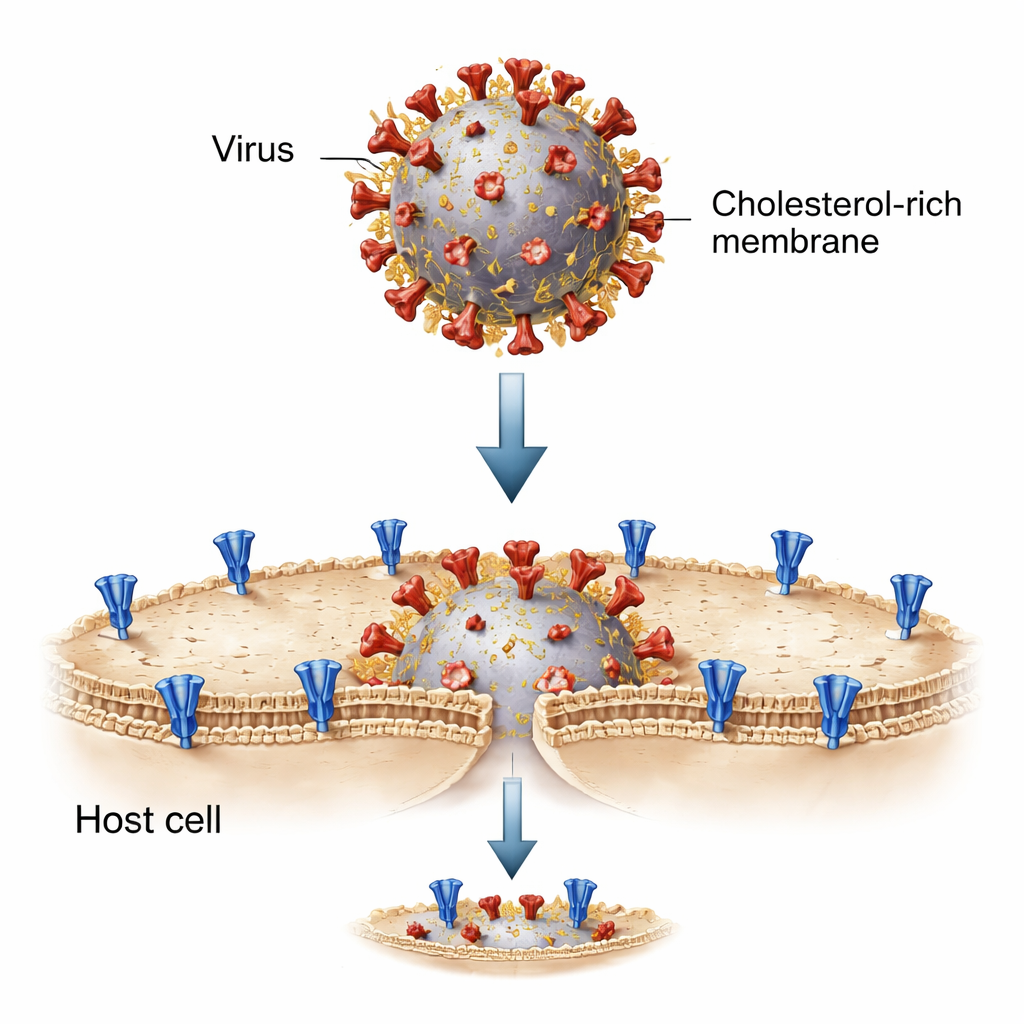
Cholesterol wzmacnia dokowanie bardziej niż samą fuzję
Regulując ilość cholesterolu, zespół odkrył, że dodanie cholesterolu do błony z kolcami zwiększa częstotliwość fuzji, ale nie w sposób, którego można by się spodziewać. Wysoki poziom cholesterolu nie zmieniał radykalnie prawdopodobieństwa, że dwie już przyległe błony faktycznie się zespają. Zamiast tego wyraźnie zwiększał częstotliwość, z jaką pęcherzyki niosące kolce najpierw dokowały do pęcherzyków z ACE2. Obrazowanie pojedynczych cząstek wykazało znacznie więcej udanych zdarzeń dokowania, gdy kolce znajdowały się w błonach bogatych w cholesterol, podczas gdy prawdopodobieństwo, że zadokowana para przejdzie do pełnej fuzji, pozostawało w przybliżeniu stałe. Co ciekawe, nasycenie cholesterolem strony z ACE2 przynosiło niewielkie korzyści, a przy bardzo wysokich poziomach wręcz utrudniało fuzję, co wskazuje na cholesterol po stronie wirusa — a nie gospodarza — jako główny czynnik napędowy.
Od błon modelowych do komórek żywych
Następnie badacze sprawdzili, czy ten sam wzorzec występuje w żywych komórkach. Zaprojektowali ludzkie komórki do ekspresji albo kolca, albo ACE2 i obserwowali, jak po zmieszaniu tworzą duże struktury zlane, zwane syncytiami. Usunięcie cholesterolu z komórek eksprymujących kolce niemal znosiło tworzenie syncytiów, podczas gdy przywrócenie cholesterolu ratowało fuzję. W równoległych eksperymentach z „pseudowirusami” SARS-CoV-2 (bezpiecznymi cząstkami wirusa używającymi kolca koronawirusa do wejścia do komórek) pozbawienie błony wirusowej cholesterolu wyraźnie zmniejszyło zakaźność, a jego ponowne dodanie zwiększało zakażenie w sposób zależny od dawki. W przeciwieństwie do tego, zmiany cholesterolu wyłącznie po stronie komórek ACE2 dały niewielkie efekty. We wszystkich testach przekaz był spójny: cholesterol w błonie zawierającej kolce jest niezbędny do efektywnego wejścia.
Klastry kolców: tajna broń cholesterolu
Dlaczego cholesterol po stronie wirusa ma tak duże znaczenie? Obrazowanie o wysokiej rozdzielczości błon komórkowych wykazało, że białka kolca mają tendencję do tworzenia gęstych klastrów, gdy cholesterol jest obfity, podczas gdy przy jego niedoborze pozostają bardziej rozproszone. Pomiary pojedynczych cząsteczek posunęły się dalej, pokazując, że te klastry zawierają więcej kopii kolca w warunkach bogatych w cholesterol. Autorzy przypisali ten efekt regionowi bogatemu w cysteiny (CRR) na końcu ogonka kolca, wewnątrz błony wirusowej. Ten fragment ulega modyfikacji przez palmitoylację — rodzaj tłuszczowego „kotwiczenia”, który sprzyja fragmentom bogatym w cholesterol. Gdy zespół skrócił ogon kolca lub zmienił wszystkie dziesięć cystein, blokując palmitoylację, kolce przestały grupować się z cholesterolem, a cholesterolowy wzrost dokowania i fuzji zniknął. 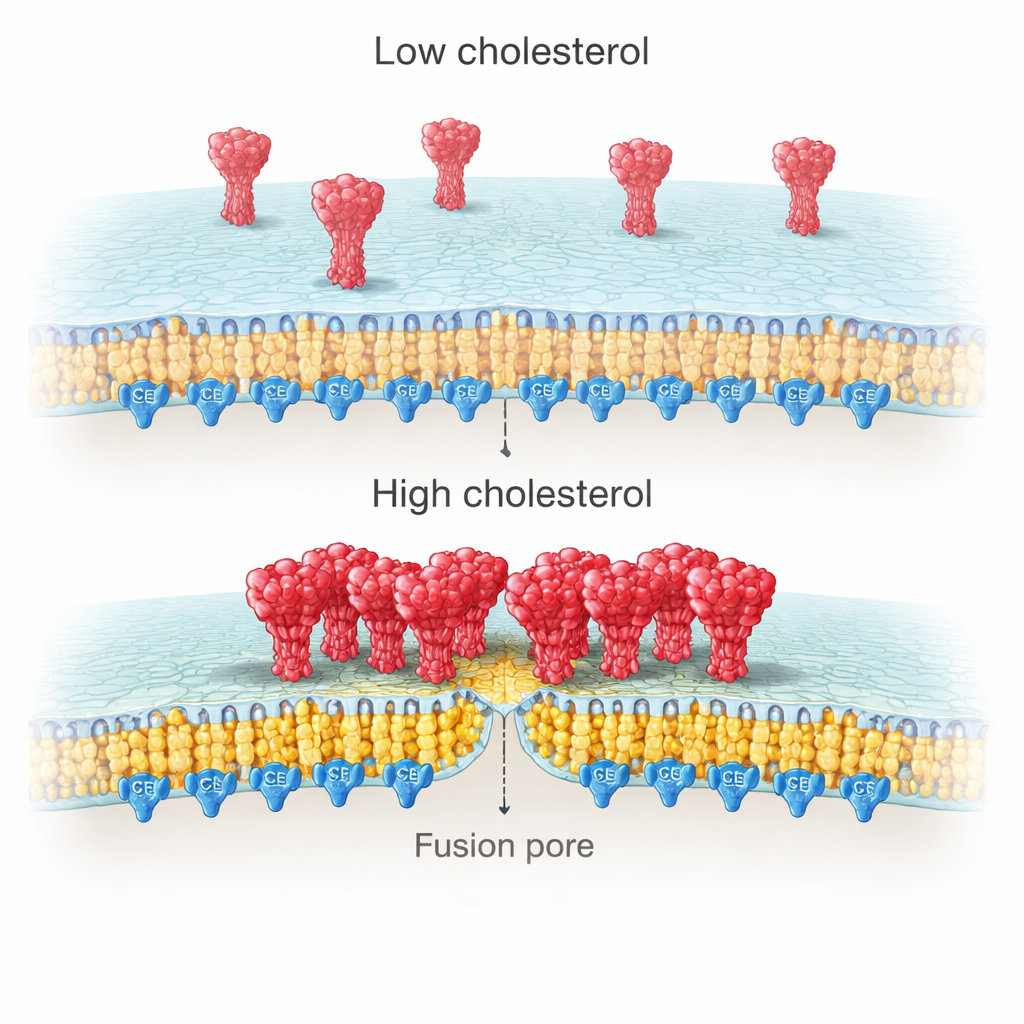
Jak to może pomóc w przyszłych terapiach
Mówiąc wprost, badanie konkluduje, że cholesterol przekształca błonę wirusa w platformę fuzji, gromadząc wiele białek kolca w ciasne klastry poprzez ich palmitoylowany region ogonkowy. Takie klastry efektywniej dokują do ACE2 na komórkach gospodarza, zwiększając szanse, że dane zetknięcie doprowadzi do udanej fuzji i zakażenia. Dla czytelników niebędących specjalistami kluczowy wniosek jest taki, że cholesterol nie jest tylko biernym składnikiem powłoki wirusa; jest aktywnym organizatorem aparatu kolca. To sprawia, że cysteinowy, wrażliwy na cholesterol ogonek kolca — oraz enzymy dokonujące jego palmitoylacji — są obiecującymi celami dla szeroko działających strategii przeciwwirusowych, które mogłyby działać w różnych wariantach koronawirusa.
Cytowanie: Li, W., Wu, M., Feng, S. et al. Molecular mechanism of cholesterol-dependent membrane fusion in SARS-CoV-2 entry. Sig Transduct Target Ther 11, 57 (2026). https://doi.org/10.1038/s41392-026-02573-z
Słowa kluczowe: cholesterol, kolce SARS-CoV-2, fuzja błon, wejście wirusa, palmitoylacja