Clear Sky Science · pl
PKC-eta promuje przerzuty raka piersi przez regulację szlaku sygnalizacyjnego Hippo–YAP
Dlaczego te badania mają znaczenie
Rak piersi potrójnie ujemny (TNBC) należy do najgroźniejszych postaci raka piersi, ponieważ wcześnie daje przerzuty i nie ma terapii celowanych. W tym badaniu odkryto, że specyficzny enzym wewnątrz komórek nowotworowych, nazywany PKC‑eta (PKCη), działa jak główny przełącznik, który pomaga guzom odrywać się, podróżować po organizmie i tworzyć nowe ogniska choroby. Zrozumienie tego przełącznika pozwoliło też zidentyfikować niewielki naturalny peptyd, który potrafi go wyłączyć, wskazując potencjalną nową drogę leczenia tej agresywnej choroby. 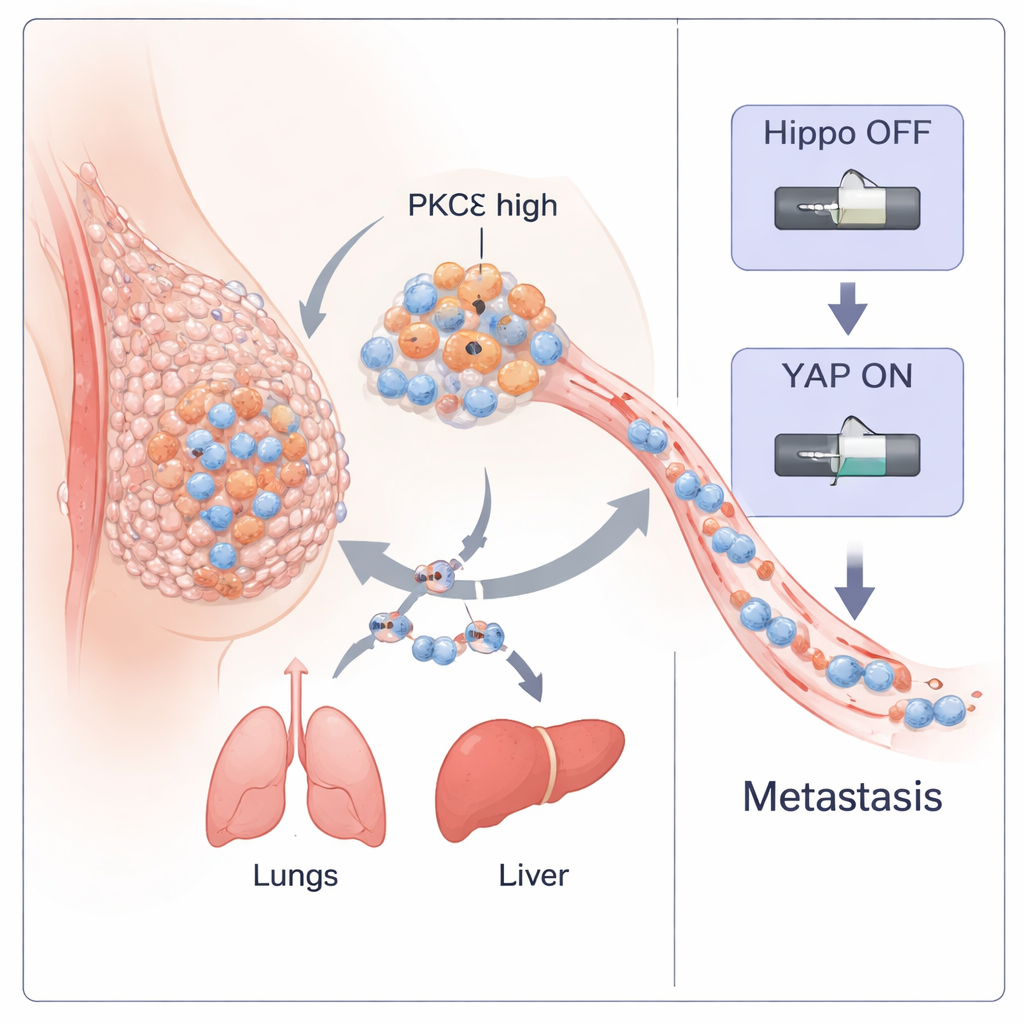
Ukryty czynnik napędzający agresywne guzy
Zespół rozpoczął od analizy dużych zbiorów danych pacjentów z rakiem piersi. Stwierdzili, że gen kodujący PKCη (PRKCH) jest szczególnie silnie wyrażany w podtypie guzów znanym jako „claudin‑low”, który w dużym stopniu pokrywa się z TNBC i zawiera dużo komórek o cechach komórek macierzystych oraz wysokiej zdolności do przemieszczania się. W wielu kohortach pacjentów guzy o wysokim poziomie PRKCH wykazywały silne sygnatury przejścia nabłonkowo‑mezenchymalnego (EMT) — procesu, w którym uporządkowane komórki tracą połączenia, zmieniają kształt i stają się bardziej inwazyjne. Poziomy PRKCH były też wyższe w próbkach przerzutowych niż w pierwotnych guzach, a barwienie białkowe tkanek ludzkiego TNBC wykazało więcej aktywnego, okołojądrowego PKCη w wyższych stopniach zaawansowania choroby. Razem te obserwacje sugerowały bliski związek PKCη z agresywnością guza i jego zdolnością do szerzenia się.
Od hodowli do myszy: dowód, że PKCη napędza rozprzestrzenianie
Aby sprawdzić związek przyczynowo‑skutkowy, badacze zastosowali edycję genów CRISPR, by usunąć PKCη z dwóch wysoce przerzutowych linii komórkowych TNBC, jednej mysiej (4T1) i jednej ludzkiej (MDA‑MB‑231). Bez PKCη komórki przesunęły się w kierunku stanu bardziej „nabłonkowego”: zwiększyła się ekspresja białek adhezyjnych takich jak E‑kadheryna i EpCAM, a zmniejszyły się klasyczne markery mezenchymalne, w tym wimentyna i N‑kadheryna. Komórki pozbawione PKCη tworzyły mniej i mniejsze kolonie, mniej efektywnie migrowały i inwadowały, były bardziej wrażliwe na śmierć po oderwaniu i wykazywały wyraźny spadek cech komórek nowotworowych typu macierzystego, w tym mniej komórek CD44high/CD24low i ALDH‑pozytywnych oraz obniżoną zdolność do tworzenia sfer. Po wstrzyknięciu do myszy komórki bez PKCη dawały mniejsze guzy pierwotne i znacznie mniej przerzutów do płuc, wątroby, mózgu i innych narządów; myszy również żyły dłużej. Przywrócenie PKCη odwróciło te zmiany, potwierdzając, że enzym aktywnie promuje progresję i rozprzestrzenianie TNBC.
Jak PKCη przejmuje kontrolę nad szlakiem regulującym wzrost
Następnie badanie skupiło się na mechanizmie, dzięki któremu PKCη wywiera ten prometastatyczny efekt. Dane pacjentów wykazały, że poziomy PKCη zmieniają się równolegle z YAP — potężnym białkiem regulatorowym kontrolowanym przez szlak Hippo, będący komórkowym „hamulcem bezpieczeństwa” normalnie ograniczającym wzrost. Wysokie poziomy PRKCH lub YAP1 prognozowały gorsze wyniki u pacjentów, a jednoczesnie wysoki poziom obu był związany ze szczególnie złym odsetkiem przeżycia wolnego od odległych przerzutów. W komórkach TNBC usunięcie PKCη obniżało całkowite poziomy YAP i przesuwało je z jądra do cytoplazmy, gdzie jest nieaktywne. Eksperymenty biochemiczne wykazały, że PKCη fizycznie wiąże się z YAP i specyficznie dodaje grupę fosforanową w miejscu Ser128. Ta modyfikacja stabilizuje YAP i ułatwia jego wejście do jądra, gdzie włącza geny napędzające EMT, cechy komórek macierzystych i przerzutowanie. Gdy PKCη jest nieobecne, YAP jest fosforylowane w innych miejscach (Ser127 i Ser397), co powoduje wiązanie z białkami 14‑3‑3, zatrzymanie w cytoplazmie i w końcu degradację. PKCη dodatkowo zwiększa poziom PTEN — naturalnego hamulca kinazy AKT — utrzymując aktywność AKT na niskim poziomie i tłumiąc górne kinazy Hippo, które w przeciwnym razie inaktywowałyby YAP. W ten sposób PKCη zarówno bezpośrednio aktywuje YAP, jak i pośrednio wyłącza „hamulec” Hippo. 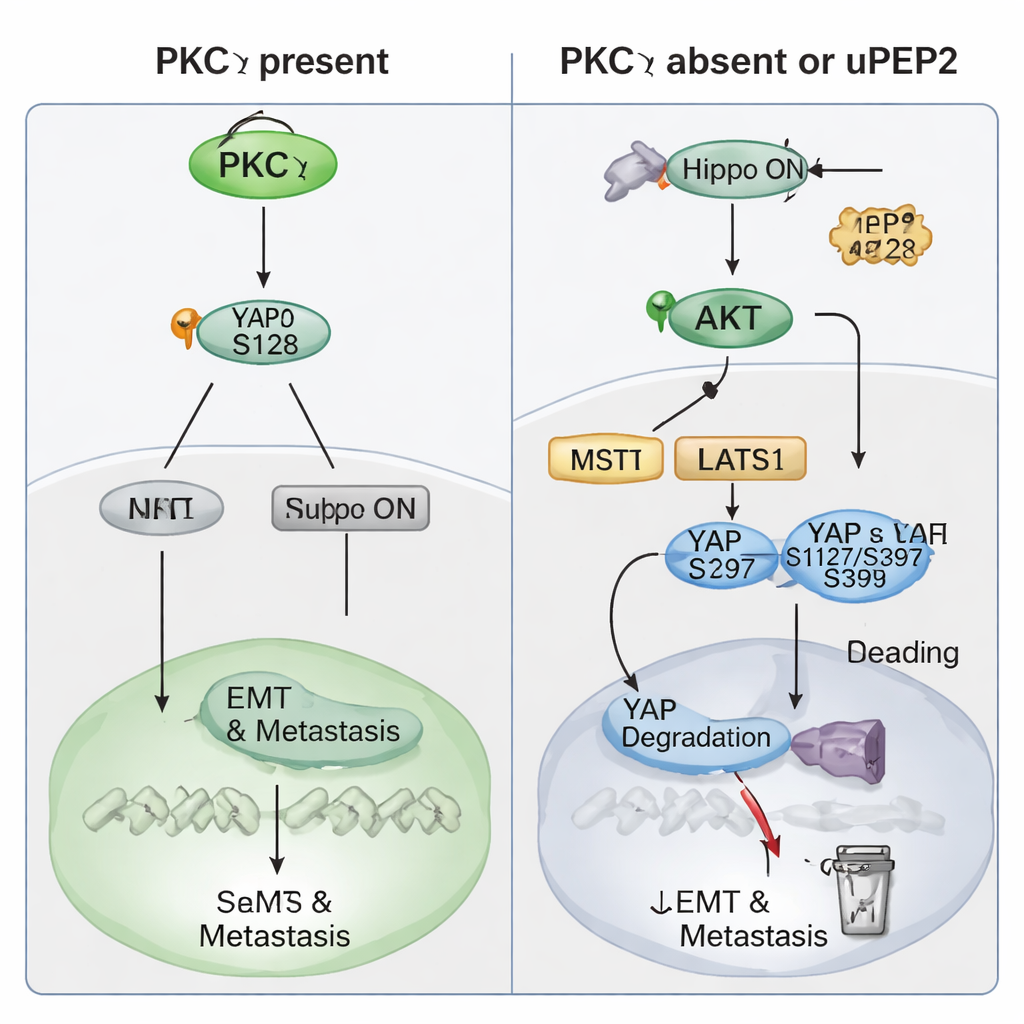
Mały peptyd, który unieszkodliwia nowotworowy przełącznik
Ciekawie, gen PKCη zawiera krótki, uprzedni otwarty odczyt (uORF), który koduje mikropeptyd zwany uPEP2. Wcześniejsze badania wykazały, że uPEP2 może wiązać się z PKCη i hamować pokrewne enzymy. Tutaj leczenie komórek TNBC syntetycznym uPEP2 naśladowało efekty braku PKCη: spadły migracja, inwazja i zachowania typu komórek macierzystych, markery EMT przesunęły się w kierunku mniej agresywnego profilu, a poziomy YAP zmalały przy jednoczesnym wzroście fosforylacji „wyłączającej”. W guzach mysich uPEP2 zmniejszał PKCη i YAP w guzach pierwotnych, zwiększał inaktywację YAP i wiązał się z mniejszą liczbą mikrprzerzutów w wątrobie i płucach. Mechanistycznie uPEP2 promuje degradację PKCη, przywracając aktywność szlaku Hippo i kierując YAP ku zatrzymaniu w cytoplazmie i rozkładowi.
Co to oznacza dla przyszłych terapii
Dla czytelnika niebędącego specjalistą kluczowy wniosek jest taki, że badacze zidentyfikowali PKCη jako centralny element pozwalający najbardziej agresywnym rakom piersi poluzować połączenia, poruszać się i kolonizować odległe narządy, poprzez wyłączenie naturalnego systemu kontroli wzrostu i aktywację „pedału gazu” YAP. Poprzez usunięcie PKCη lub zastosowanie małego naturalnego peptydu uPEP2 prowadzącego do jego degradacji, udało się przywrócić hamulec Hippo, uciszyć YAP i znacznie zmniejszyć przerzuty w modelach przedklinicznych. Choć prace te są nadal na etapie eksperymentalnym i przeprowadzone zostały na liniach komórkowych oraz w myszach immunodeficjentnych, podkreślają PKCη i jego interakcję z YAP jako obiecujące cele dla nowych terapii TNBC i sugerują, że leki na bazie uPEP2 mogłyby kiedyś pomóc zapobiegać lub ograniczać rozprzestrzenianie się tego trudnego do leczenia nowotworu.
Cytowanie: Liju, V.B., Waidha, K., Muraleedharan, A. et al. PKC-eta promotes breast cancer metastasis by regulating the Hippo–YAP signaling pathway. Sig Transduct Target Ther 11, 58 (2026). https://doi.org/10.1038/s41392-026-02572-0
Słowa kluczowe: rak piersi potrójnie ujemny, PKC-eta, szlak Hippo-YAP, przejście nabłonkowo-mezenchymalne, przerzutowanie nowotworu