Clear Sky Science · pl
Odkrywanie i rozwój leków przeciwwirusowych: wyzwania i kierunki na przyszłość
Dlaczego wciąż potrzebujemy lepszych leków przeciw wirusom
Pandemia COVID-19 pokazała, jak szybko nowy wirus może zaburzyć codzienne życie — oraz jak bardzo nadal polegamy na dobrych lekach, gdy szczepionki nie wystarczają. Niniejszy artykuł przeglądowy cofa się o 60 lat rozwoju leków przeciwwirusowych i stawia pytanie: jak zbudować szybsze, mądrzejsze i szersze systemy obronne wobec przyszłych zagrożeń wirusowych? Wyjaśnia przystępnym językiem, jak naukowcy odkrywają, projektują i dostarczają leki przeciwwirusowe, czego nauczyli się na przykładzie COVID-19 i jak narzędzia takie jak sztuczna inteligencja i nanotechnologia mogą zmienić zasady gry.
Od pierwszych leków przeciwwirusowych do współczesnego arsenału
Medycyna przeciwwirusowa to stosunkowo młoda dziedzina. Pierwszy zatwierdzony lek, idoksurydyna w latach 60., pokazał, że modyfikowanie cegiełek DNA może spowolnić replikację wirusa, ale jednocześnie uszkadzało zdrowe komórki i można było go stosować wyłącznie miejscowo na oko. Później pojawił się acyklowir — przełomowy lek na opryszczkę, aktywowany głównie wewnątrz zainfekowanych komórek, co uczyniło go zarówno skutecznym, jak i bezpiecznym. W latach 80. zidowudyna została pierwszym lekiem na HIV, otwierając drogę do współczesnych terapii skojarzonych, które zamieniły HIV w chorobę przewlekłą możliwą do kontrolowania. Na przestrzeni dekad lepsza chemia i projektowanie wspomagane komputerowo doprowadziły do powstania bardziej precyzyjnych leków przeciw grypie, wirusom zapalenia wątroby typu B i C, HIV i, najnowsze, SARS‑CoV‑2. Artykuł śledzi tę oś czasu i pokazuje, jak każde przełomowe odkrycie wnosiło nowy sposób przechytrzenia wirusów.
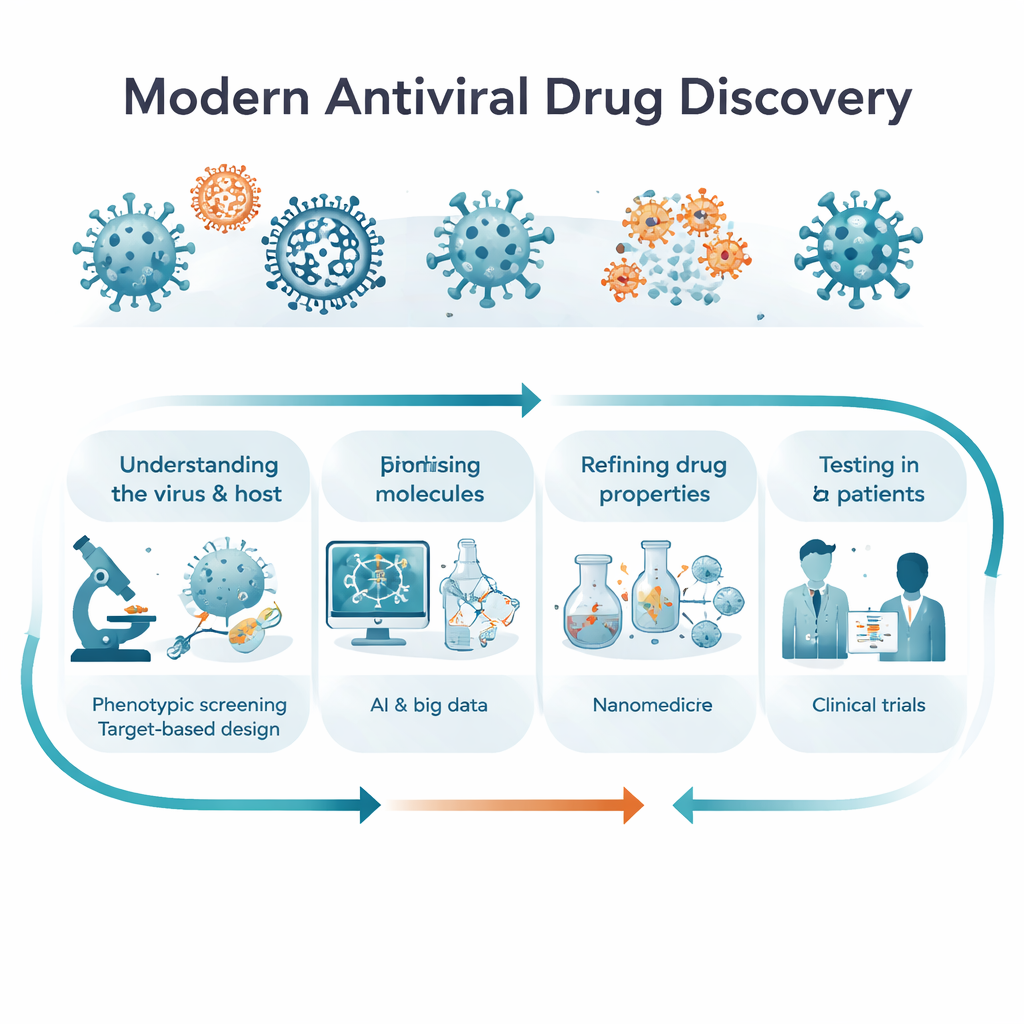
Dwie drogi do dobrego leku: obserwacja komórek kontra celowanie w białka
Naukowcy zazwyczaj podążają dwiema uzupełniającymi się ścieżkami do nowych leków przeciwwirusowych. W odkrywaniu „fenotypowym” nie zaczynają od konkretnego białka; zamiast tego wystawiają zainfekowane komórki lub modele organizmów na działanie tysięcy cząsteczek i po prostu pytają: które z nich powstrzymują wirusa i utrzymują komórki przy życiu? Ta metoda może ujawnić zaskakujące, pierwszej klasy leki, w tym takie, które działają na więcej niż jedną ścieżkę. W odkrywaniu „ukierunkowanym” naukowcy najpierw identyfikują białko wirusowe lub gospodarza kluczowe dla infekcji — takie jak polimeraza, proteaza czy sygnał immunologiczny — i następnie projektują molekuły blokujące lub modulujące ten cel. Artykuł wyjaśnia, czym te strategie się różnią, dlaczego każda z nich jest ważna na różnych etapach badań i jak przyszłe projekty prawdopodobnie będą je łączyć, przechodząc płynnie od szerokiej obserwacji do precyzyjnego zrozumienia molekularnego.
Atakując wirusa — i jego system wsparcia — tam, gdzie boli
Współczesne leki przeciwwirusowe robią znacznie więcej niż blokowanie pojedynczej wirusowej enzymu. Przegląd prowadzi przez cykl życiowy wirusa, od wejścia do komórki, przez kopiowanie genomu, aż po uwalnianie, i wyróżnia typy leków interferujące na każdym z tych etapów. Niektóre związki wiążą się bezpośrednio z enzymami wirusa lub białkami strukturalnymi. Inne działają przez celowanie w czynniki gospodarza, od których wirusy zależą — takie jak receptory na powierzchni komórek, kluczowe enzymy metaboliczne czy wrodzone drogi odpornościowe, np. interferony i receptory typu toll. Działając na „pomocnicze” białka gospodarza, te leki mogą zmniejszyć prawdopodobieństwo, że szybko mutujący wirus je przechytrzy. Autorzy opisują też nowe pomysły, na przykład małe molekuły zakłócające bezbłonowe „kropelki” wewnątrz komórek, gdzie wirusy się montują, albo związki selektywnie degradowujące białka i RNA wirusa zamiast jedynie je blokować.
Projektowanie lepszych cząsteczek: kształt, właściwości i dostarczanie
Przemiana początkowego „hitu” w użyteczny lek to coś więcej niż maksymalizacja mocy działania. Chemicy dostosowują kształt i ładunek cząsteczek tak, by pasowały do celów jak klucz do zamka, często kierując się strukturami białek o wysokiej rozdzielczości i symulacjami. Modyfikują też rozpuszczalność w wodzie, stabilność i metabolizm, aby zapewnić, że lek dotrze do właściwej tkanki, pozostanie aktywny wystarczająco długo i nie będzie nadmiernie toksyczny. Artykuł podaje przykłady, jak małe zmiany — np. dodanie łańcucha bocznego lub utworzenie soli — mogą zwiększyć aktywność przeciw opornym szczepom HIV czy koronawirusów przy równoczesnym poprawieniu bezpieczeństwa. Wyjaśnia też proleki — nieaktywne lub słabiej aktywne formy zaprojektowane do konwersji w organizmie — oraz ukierunkowane systemy dostarczania, takie jak znaczniki cukrowe celujące w wątrobę i nanocząstki lipidowe, które bezpiecznie przenoszą kruche mRNA lub leki nukleinowe do komórek.
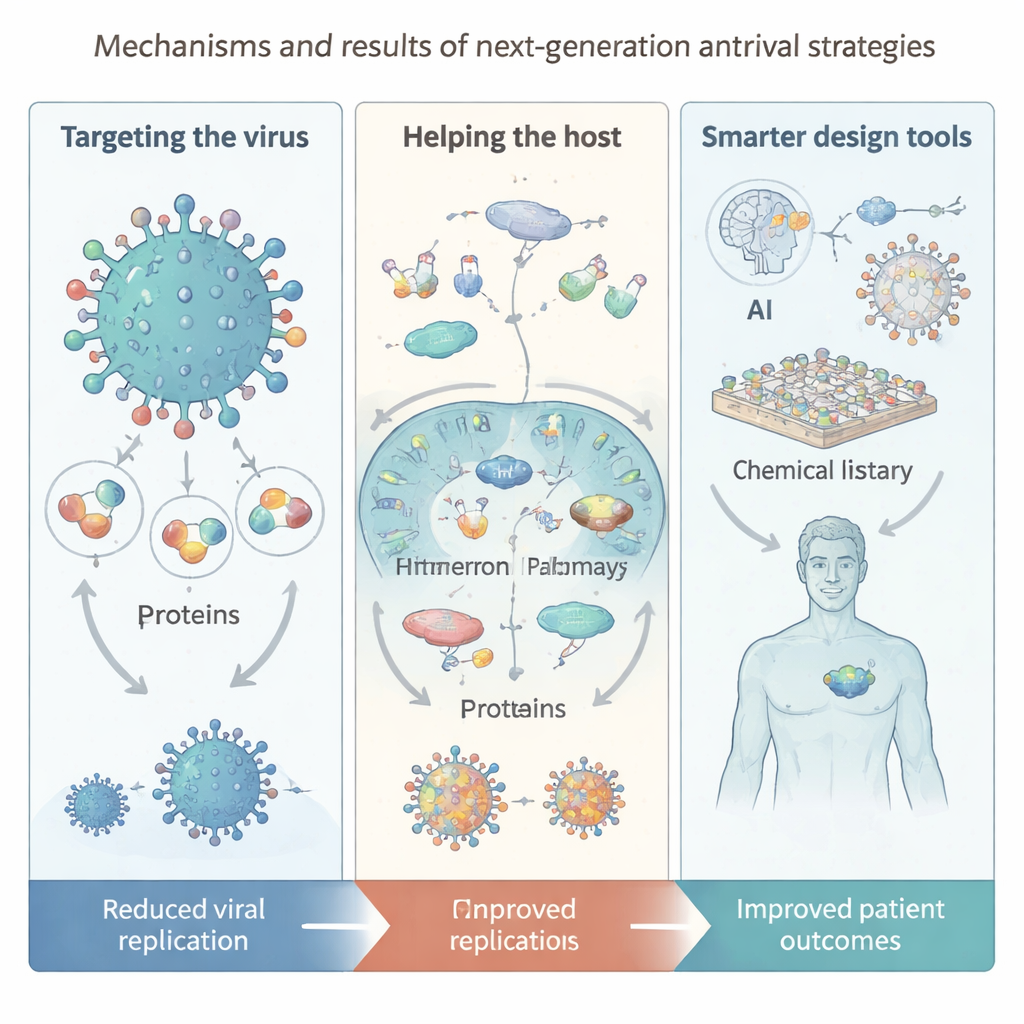
Nowe narzędzia: sztuczna inteligencja, olbrzymie biblioteki i nanotechnologia
Główny motyw przeglądu to to, jak technologia przeobraża odkrywanie leków przeciwwirusowych. Sztuczna inteligencja pomaga obecnie przewidywać struktury białek, przeszukiwać ogromne „wirtualne” biblioteki zawierające miliardy możliwych cząsteczek oraz proponować nowe związki czy kombinacje terapeutyczne. Biblioteki kodowane DNA i platformy peptydów makrocyklicznych pozwalają na ultraw szybkie przesiewanie olbrzymich przestrzeni chemicznych, podczas gdy zautomatyzowane systemy syntezy i oczyszczania przyspieszają cykl buduj-i-testuj. Po stronie dostarczania nanotechnologia oferuje cząstki przypominające wirusy, inteligentne polimery i „nanozymy”, które mogą bezpośrednio uszkadzać osłonki wirusowe lub wzmacniać reakcje odpornościowe. Jednak autorzy ostrzegają, że modele AI wciąż zależą od danych wysokiej jakości, że wiele wygenerowanych molekuł jest trudnych do wytworzenia lub przetestowania, oraz że należy poruszyć kwestie bezpieczeństwa, równości i prywatności w miarę jak te narzędzia stają się bardziej centralne.
Dokąd zmierza odkrywanie leków przeciwwirusowych
Dla czytelnika niebędącego specjalistą kluczowe przesłanie artykułu jest zarówno trzeźwiące, jak i budujące nadzieję. Wirusy mutują szybko i żadna pojedyncza pigułka nie zadziała na zawsze ani wobec wszystkich zagrożeń. Jednak ucząc się na doświadczeniach z COVID‑19, pogłębiając wiedzę o interakcjach wirus–gospodarz oraz łącząc inteligentną chemię, zaawansowaną biologię, AI i nanotechnologię, naukowcy budują bardziej zwinne narzędzia przeciwwirusowe. Przyszłe terapie prawdopodobnie będą miały szerszy zakres działania, lepszą tolerancję i będą ukierunkowane tak, by trafiać nie tylko w wirusa, lecz także w wrażliwe „słabe ogniwa” procesu infekcyjnego. Kontynuacja współpracy między dyscyplinami, przemysłem i krajami będzie niezbędna, aby przekształcić te postępy naukowe w przystępne i praktyczne leki zanim nadejdzie następna pandemia.
Cytowanie: Du, S., Hu, X., Li, P. et al. Antiviral drug discovery and development: challenges and future directions. Sig Transduct Target Ther 11, 69 (2026). https://doi.org/10.1038/s41392-025-02539-7
Słowa kluczowe: odkrywanie leków przeciwwirusowych, terapie COVID-19, leki przeciwwirusowe celowane w gospodarza, sztuczna inteligencja w projektowaniu leków</keyword;s> <keyword>nanotechnologia w medycynie