Clear Sky Science · pl
Limfocyty CD4+ z właściwościami cytotoksycznymi: pochodzenie, funkcje biologiczne, choroby i cele terapeutyczne
Kiedy komórki pomocnicze stają się zabójcami
Układ odpornościowy zwykle opisuje się w prostych rolach: jedne komórki dostrzegają zagrożenie, inne prowadzą bezpośrednią walkę. Artykuł koncentruje się na zaskakującej grupie rozmywającej tę granicę — cytotoksycznych limfocytach CD4. Długo postrzegane głównie jako komórki „pomocnicze” koordynujące odpowiedź immunologiczną, niektóre limfocyty CD4 same mogą stać się uzbrojonymi zabójcami. Zrozumienie, jak powstają te zmieniające się komórki, co robią i jak przyczyniają się do chorób takich jak nowotwory, infekcje wirusowe, schorzenia autoimmunologiczne i choroby serca, może otworzyć nowe sposoby zarówno na wzmocnienie odporności, jak i łagodzenie szkodliwego zapalenia. 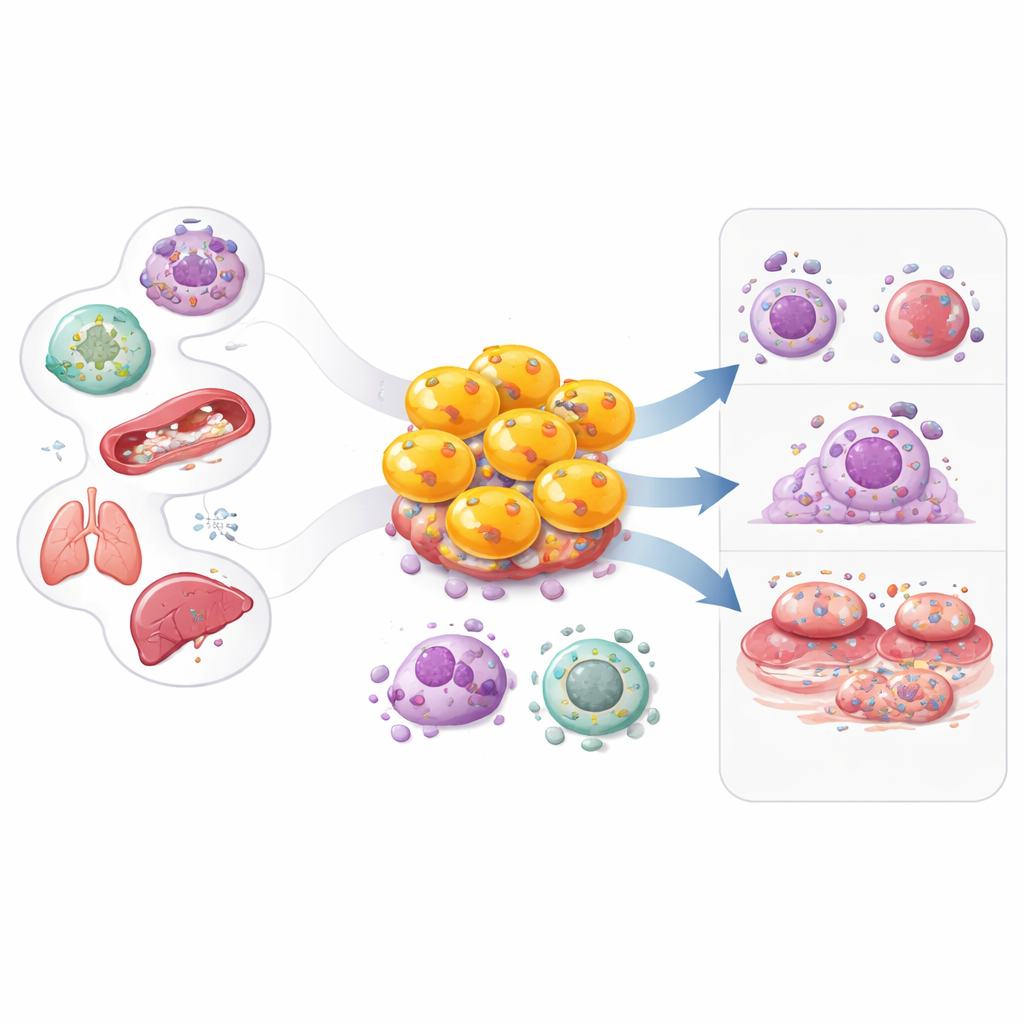
Jak wykształcił się ten elastyczny obrońca
Pierwsze prace z końca lat 70. i z lat 80. pokazały, że część limfocytów CD4 może bezpośrednio zabijać inne komórki prezentujące odpowiednie sygnały immunologiczne, podobnie jak klasyczne limfocyty CD8 „zabójcy”. Początkowo wielu naukowców odrzucało te obserwacje jako artefakty hodowli in vitro. W kolejnych dekadach modele zwierzęce grypy oraz badania u osób z reumatoidalnym zapaleniem stawów, chorobami serca, przewlekłymi infekcjami wirusowymi i rakiem potwierdziły, że cytotoksyczne limfocyty CD4 są rzeczywiste i klinicznie istotne. Nowoczesne narzędzia, takie jak cytometria przepływowa i sekwencjonowanie RNA pojedynczych komórek, zmapowały ich różnorodność, ukazując, że te komórki rozszerzają się w przewlekłych zakażeniach, nowotworach, w starzeniu oraz w kilku chorobach zapalnych, gdzie mogą utrzymywać się przez długi czas.
Skąd pochodzą ci zabójczy pomocnicy
Przegląd wyjaśnia, że cytotoksyczne limfocyty CD4 prawdopodobnie powstają na dwa zasadnicze sposoby. Jedna hipoteza zakłada, że częściowo przypominają komórki NK, ponieważ dzielą wiele tych samych receptorów powierzchniowych i cząsteczek cytotoksycznych, co sugeruje pokrewną ścieżkę rozwojową. Jednak rosnące dowody skłaniają ku innej interpretacji: większość tych komórek zaczyna jako zwykłe pomocnicze limfocyty CD4 — szczególnie komórki o fenotypie Th1 — które pod wpływem przewlekłej ekspozycji na antygen i silnych sygnałów zapalnych „przeprogramowują się” w końcowo zróżnicowany, cytotoksyczny stan. Ten przełom kontrolowany jest przez sieć zewnętrznych wskazówek (takich jak interleukiny 2, 7 i 15) oraz wewnętrznych przełączników (w tym Runx3, T‑bet, Eomes, Blimp‑1 i Hobit), które łącznie włączają geny kodujące perforynę, granzymy i ligandy indukujące śmierć.
Jak zabijają i jak kształtują zapalenie
Funkcjonalnie cytotoksyczne limfocyty CD4 działają dwiema głównymi drogami ataku. W drodze ziarnistej tworzą ciasny kontakt z komórką docelową i uwalniają pakiety zawierające perforynę i granzymy, które tworzą otwory i uruchamiają programowaną śmierć komórki od wewnątrz. W drodze ligandów śmierci eksponują na powierzchni cząsteczki takie jak ligand Fas i TRAIL, wiążące dopasowane receptory na komórkach docelowych i uruchamiające wewnętrzny program samobójczy. Poza bezpośrednim zabijaniem, komórki te wydzielają silne mediatory zapalne, jak interferon‑gamma, czynnik martwicy nowotworów i czynniki wzrostu, które rekrutują i aktywują inne komórki odpornościowe, przebudowują naczynia krwionośne i zmieniają lokalne zachowanie tkanek. W przeciwieństwie do klasycznych komórek pomocniczych, często są odporne na normalne „hamulce” takie jak komórki regulatorowe (Treg) i mniej podatne na apoptozę, co umożliwia ich kumulację w chorobach przewlekłych. 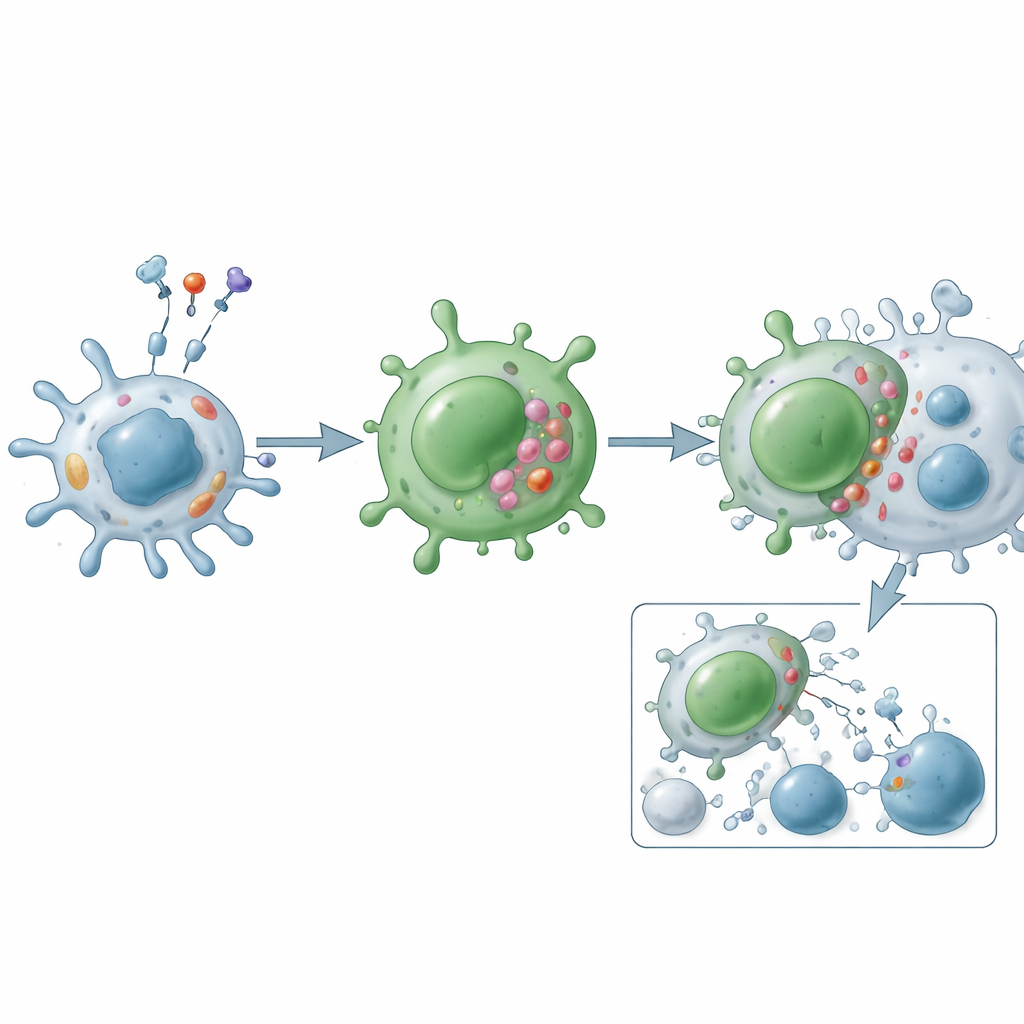
Sprzymierzeńcy w infekcji i nowotworze, wrogowie w autoimmunizacji i chorobach serca
To obosieczne zachowanie ujawnia się w wielu stanach. W przewlekłym zapaleniu wątroby typu B, HIV i COVID‑19 cytotoksyczne limfocyty CD4 pomagają kontrolować wirusy, gdy limfocyty CD8 są wyczerpane, a ich obecność może korelować z lepszą kontrolą infekcji lub powrotem do zdrowia. W nowotworach litych i nowotworach krwi mogą bezpośrednio rozpoznawać komórki nowotworowe prezentujące odpowiednie markery immunologiczne lub sygnały stresu i mogą poprawiać odpowiedzi na immunoterapie, takie jak inhibitory punktów kontrolnych czy terapie CAR‑T. Jednocześnie te same mechanizmy mogą powodować szkody: w toczniu, reumatoidalnym zapaleniu stawów, chorobach zapalnych jelit, chorobie wieńcowej, migotaniu przedsionków, olbrzymiokomórkowym zapaleniu tętnic i odrzuceniu przeszczepu poszerzone cytotoksyczne limfocyty CD4 naciekają tkanki, uszkadzają naczynia lub narządy i wzmacniają długotrwałe zapalenie, często korelując z gorszym rokowaniem.
Przekształcanie ryzykownego narzędzia w terapię
Ponieważ cytotoksyczne limfocyty CD4 mogą być zarówno ochronne, jak i destrukcyjne, artykuł podkreśla pojawiające się strategie terapeutyczne, które mają na celu raczej precyzyjne dostrojenie tej populacji niż jej całkowite wymazanie. Jedne podejścia dążą do stłumienia ich szkodliwej aktywności za pomocą selektywnych inhibitorów celujących w receptory kostymulujące (takie jak OX40 lub 4‑1BB), cytokiny prozapalne, kanały jonowe lub szlaki przetrwania. Inne polegają na wykorzystaniu ich mocy zabijania w adoptatywnych terapiach komórkowych, w tym komórkach T z edycją genową i produktach CAR‑T, gdzie cytotoksyczne komórki CD4 często wykazują lepszą trwałość niż produkty zawierające wyłącznie CD8. Trzecia strategia proponuje przekierowanie długo żyjących, swoistych dla wirusa limfocytów CD4 przeciwko nowotworom za pomocą szczepionek lub peptydów pochodzących od patogenów prezentowanych przez komórki nowotworowe. Razem te linie badań stawiają cytotoksyczne limfocyty CD4 nie tylko jako biologiczną ciekawostkę, lecz jako centralną dźwignię przyszłych terapii, które mogłyby precyzyjniej wzmocnić obronę przed infekcjami i nowotworami przy jednoczesnym ograniczeniu uszkadzającego tkanki zapalenia.
Nowa dźwignia dla przyszłych terapii immunologicznych
Dla czytelników niebędących specjalistami kluczowy przekaz jest taki, że „pomocnicze” limfocyty CD4 są znacznie bardziej wszechstronne, niż sądzono: niektóre mogą przestawić się w w pełni uzbrojone zabójcze komórki, które chronią nas przed przewlekłymi zakażeniami i rakiem, ale także przyczyniają się do autoimmunizacji, uszkodzeń naczyń i odrzucenia przeszczepu. Przegląd argumentuje, że nauczenie się śledzenia tych komórek, przewidywania, kiedy będą pomagać, a kiedy szkodzić, oraz modulowania ich zachowania za pomocą leków lub terapii inżynieryjnych może przekształcić sposób leczenia szerokiego spektrum chorób przewlekłych — od zapalenia wątroby i HIV po zapalenia stawów, zapalenia jelit, choroby serca i białaczki. Zamiast po prostu zwiększać lub tłumić aktywność układu odpornościowego, przyszłe terapie mogą coraz częściej działać poprzez ukierunkowywanie potężnych typów komórek, takich jak cytotoksyczne limfocyty CD4, na korzystne cele i z dala od własnych tkanek.
Cytowanie: Lai, L., Ran, S., Li, Y. et al. Cytotoxic CD4+ T cells: origin, biological functions, diseases and therapeutic targets. Sig Transduct Target Ther 11, 85 (2026). https://doi.org/10.1038/s41392-025-02533-z
Słowa kluczowe: cytotoksyczne limfocyty CD4, plastyczność komórek układu odpornościowego, przewlekłe zapalenie, immunoterapia nowotworów, choroba autoimmunologiczna