Clear Sky Science · pl
IFFO1 hamuje raka piersi, koordynując mitochondrialny rozszczep i syntezę kwasów tłuszczowych przez oś LaminA/C-PGC1α
Dlaczego to badanie ma znaczenie
Rak piersi pozostaje jedną z głównych przyczyn zgonów z powodu nowotworów u kobiet, w dużej mierze dlatego, że niektóre guzy nadal rosną, dają przerzuty i uodparniają się na dostępne terapie. To badanie ujawnia wcześniej niedoceniany komórkowy „hamulec” nazwany IFFO1, który spowalnia raka piersi przez ujarzmienie dwóch kluczowych mechanizmów napędzających wzrost guza: mitochondriów, czyli „elektrowni” komórkowych, oraz zdolności komórki do produkcji i magazynowania tłuszczów. Poznanie tego hamulca otwiera nowe perspektywy terapeutyczne, które mogłyby działać w różnych podtypach raka piersi.
Ukryty strażnik wewnątrz komórek piersi
Naukowcy zaczęli od analizy próbek od 30 kobiet z rakiem piersi oraz dużych publicznych baz danych o nowotworach. Stwierdzili, że poziomy białka IFFO1 były konsekwentnie niższe w tkance nowotworowej niż w pobliskiej tkance piersi prawidłowej. Im bardziej zaawansowany był nowotwór, tym mniejsze było stężenie IFFO1, a pacjentki, których guzy miały wyższe poziomy IFFO1, miały tendencję do dłuższego przeżycia. W hodowlach komórek raka piersi wymuszenie nadprodukcji IFFO1 wyraźnie zmniejszało ich zdolność do wzrostu, podziałów i migracji — zachowań niezbędnych do rozrostu i rozprzestrzeniania się nowotworu. IFFO1 tłumił także program komórkowy znany jako przejście nabłonkowo-mezenchymalne (EMT), które pomaga komórkom nowotworowym odrywać się i naciekać inne tkanki.
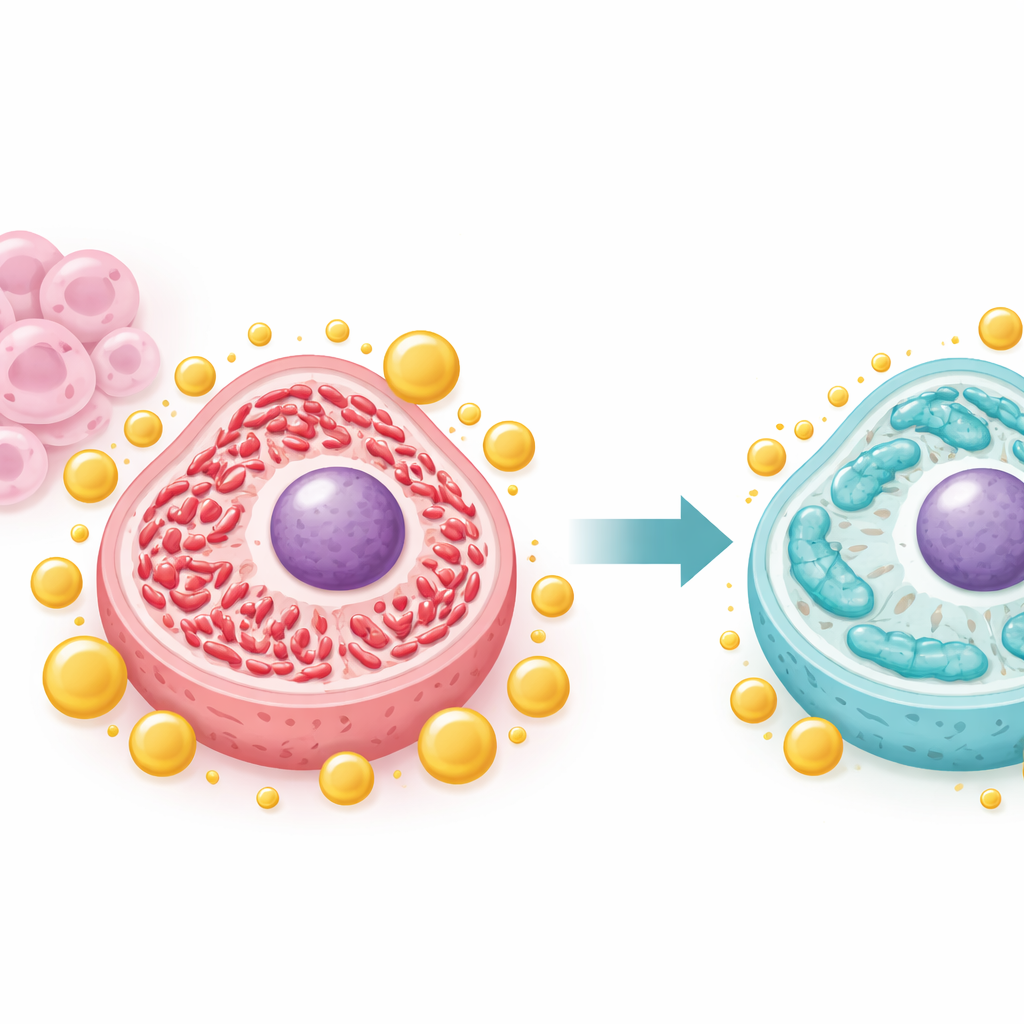
Uspokajanie nadaktywnych „elektrowni”
Komórki nowotworowe często przekształcają mitochondria, by napędzać szybki wzrost. Zespół wykazał, że IFFO1 przesuwa równowagę z silnie pociętego stanu „fuzji” w kierunku bardziej wydłużonego stanu „fuzji” — związanej z bardziej stabilnymi i zdrowszymi mitochondriami. Przy obfitym IFFO1 poziomy kluczowych białek odpowiedzialnych za rozszczepianie, takich jak Drp1 i Fis1, spadały, podczas gdy białka promujące łączenie mitochondriów rosły. Mikroskopia pokazała, że mitochondria stały się dłuższe i mniej pofragmentowane, a miary DNA mitochondrialnego i produkcji energii zmniejszyły się z patologicznie wysokich poziomów obserwowanych w agresywnych komórkach. Zmiany te sugerują, że IFFO1 zapobiega wejściu mitochondriów w hiperaktywne ustawienie sprzyjające niekontrolowanemu wzrostowi guza.
Odcięcie linii zaopatrzenia w tłuszcze
Szybko rosnące guzy potrzebują nie tylko energii; potrzebują także stałego dostępu do tłuszczów potrzebnych do budowy błon i cząsteczek sygnałowych. Badanie wykazało, że IFFO1 hamuje także ten metaboliczny akcelerator. W komórkach z nadmiarem IFFO1 podstawowe białka syntetyzujące lipidy — w tym FASN, SREBP‑1, SCD1 i inne — były zmniejszone. Testy enzymatyczne potwierdziły niższą aktywność syntezy tłuszczów, a oznaczenia chemiczne wykazały spadek wolnych kwasów tłuszczowych, triglicerydów i cholesterolu. Barwniki obrazujące zapasy tłuszczu ujawniły mniej kropli lipidowych i mniejsze ogólne nagromadzenie tłuszczów obojętnych w komórkach nowotworowych. Z kolei nadekspresja białka rozszczepiającego Drp1 wywołała efekt przeciwny, zwiększając produkcję tłuszczów, podczas gdy wyciszenie Drp1 ją ograniczało — co wspiera bezpośredni związek między kształtem mitochondriów a zaopatrzeniem w tłuszcze w raku.
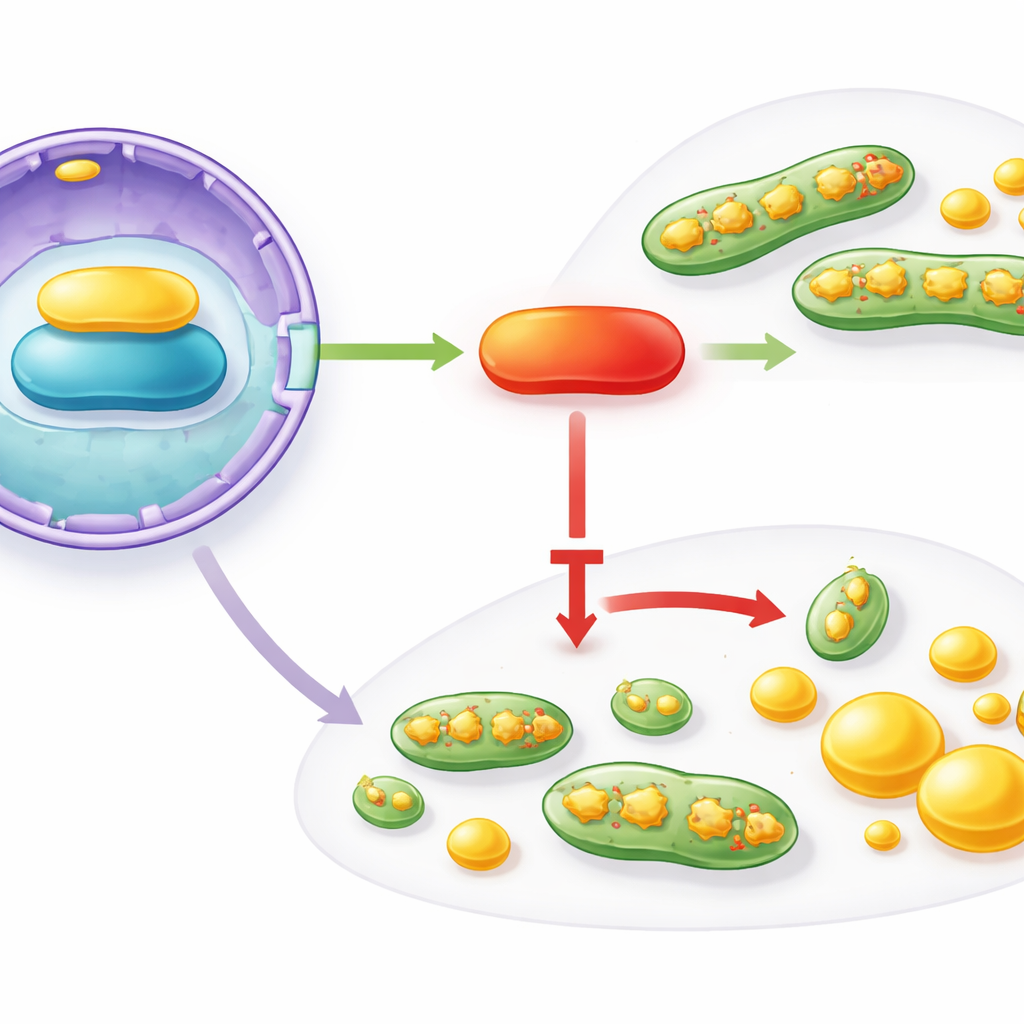
Szlak sygnałowy z jądra do mitochondriów
Jak IFFO1 orkiestruje te szerokie zmiany? Autorzy odtworzyli łańcuch interakcji, który zaczyna się w jądrze komórkowym i kończy na mitochondriach oraz aparacie do syntezy tłuszczów. IFFO1 fizycznie wiąże się ze strukturalnym białkiem otoczki jądrowej zwanym Lamin A/C i zwiększa jego poziomy. Lamin A/C z kolei wspiera aktywność PGC1α, głównego regulatora nadzorującego zdrowie mitochondriów i metabolizm. W tkankach i komórkach raka piersi zarówno Lamin A/C, jak i PGC1α były obniżone, odzwierciedlając utratę IFFO1. Gdy naukowcy sztucznie podnieśli poziom IFFO1, Lamin A/C i PGC1α rosły, rozszczepienie mitochondriów malało, a synteza tłuszczów osłabła. Wyciszenie Lamin A/C niwelowało te korzyści, ale przywrócenie PGC1α przywracało je — wskazując na funkcjonalną oś IFFO1 → Lamin A/C → PGC1α, która powstrzymuje sprzyjające nowotworowi zmiany mitochondrialne i lipidowe.
Testowanie hamulca in vivo
Aby sprawdzić, czy te efekty komórkowe przekładają się na rzeczywiste guzy, zespół wszczepił do myszy ludzkie komórki raka piersi z dodatkowym IFFO1 lub bez niego. Guzy z podwyższonym IFFO1 rosły wolniej, ważyły mniej na końcu eksperymentu i wykazywały mniej oznak nagromadzenia tłuszczu. W odrębnym modelu, w którym komórki nowotworowe wstrzyknięto do krwiobiegu, by zaszczepić przerzuty w płucach, komórki nadprodukujące IFFO1 tworzyły wyraźnie mniej guzków płucnych. Analizy tkanek z tych myszy potwierdziły obserwacje z hodowli komórek: wyższe Lamin A/C i PGC1α, mniejsze rozszczepienie mitochondriów i niższa synteza tłuszczów.
Co to oznacza dla przyszłych terapii
W sumie praca przedstawia IFFO1 jako wielopoziomowy supresor guza, który łączy szkielet strukturalny komórki, jej „elektrownie” i aparat do produkcji tłuszczów. Stabilizując Lamin A/C i zwiększając PGC1α, IFFO1 zapobiega nadmiernemu rozpadowi mitochondriów i odcina nadprodukcję tłuszczów, od których komórki nowotworowe są uzależnione. Dla osób niebędących specjalistami kluczowy komunikat jest taki, że to białko działa jak wewnętrzny hamulec zarówno dla mocy, jak i materiałów budulcowych napędzających wzrost i rozprzestrzenianie się raka piersi. Leki podnoszące poziom IFFO1 lub naśladujące jego wpływ na oś Lamin A/C–PGC1α mogą w przyszłości dać nowe możliwości, szczególnie w agresywnych lub opornych na leczenie postaciach raka piersi.
Cytowanie: Cai, H., He, J. IFFO1 inhibits breast cancer by coordinating mitochondrial fission and fatty acid synthesis via the LaminA/C-PGC1α axis. Oncogenesis 15, 16 (2026). https://doi.org/10.1038/s41389-026-00609-1
Słowa kluczowe: rak piersi, dynamika mitochondriów, synteza kwasów tłuszczowych, metabolizm nowotworu, szlak PGC1α