Clear Sky Science · pl
Onkogeniczna kontrola syntezy nukleotydów
Dlaczego komórki nowotworowe dbają o składniki budulcowe
Nowotwór często opisuje się jako komórki, które nie przestają się dzielić. Aby się jednak kopiować, komórki te potrzebują stałej dostawy drobnych składników budulcowych zwanych nukleotydami, które tworzą DNA i RNA oraz zasilają wiele procesów komórkowych. Ten przegląd wyjaśnia, w jaki sposób geny powodujące nowotwory przestawiają chemię komórkową, by utrzymać wysoką produkcję nukleotydów, jak guzy przełączają się między różnymi sposobami pozyskiwania tych cząsteczek oraz jak lekarze mogą wykorzystywać te sztuczki przy pomocy starych i nowych leków.
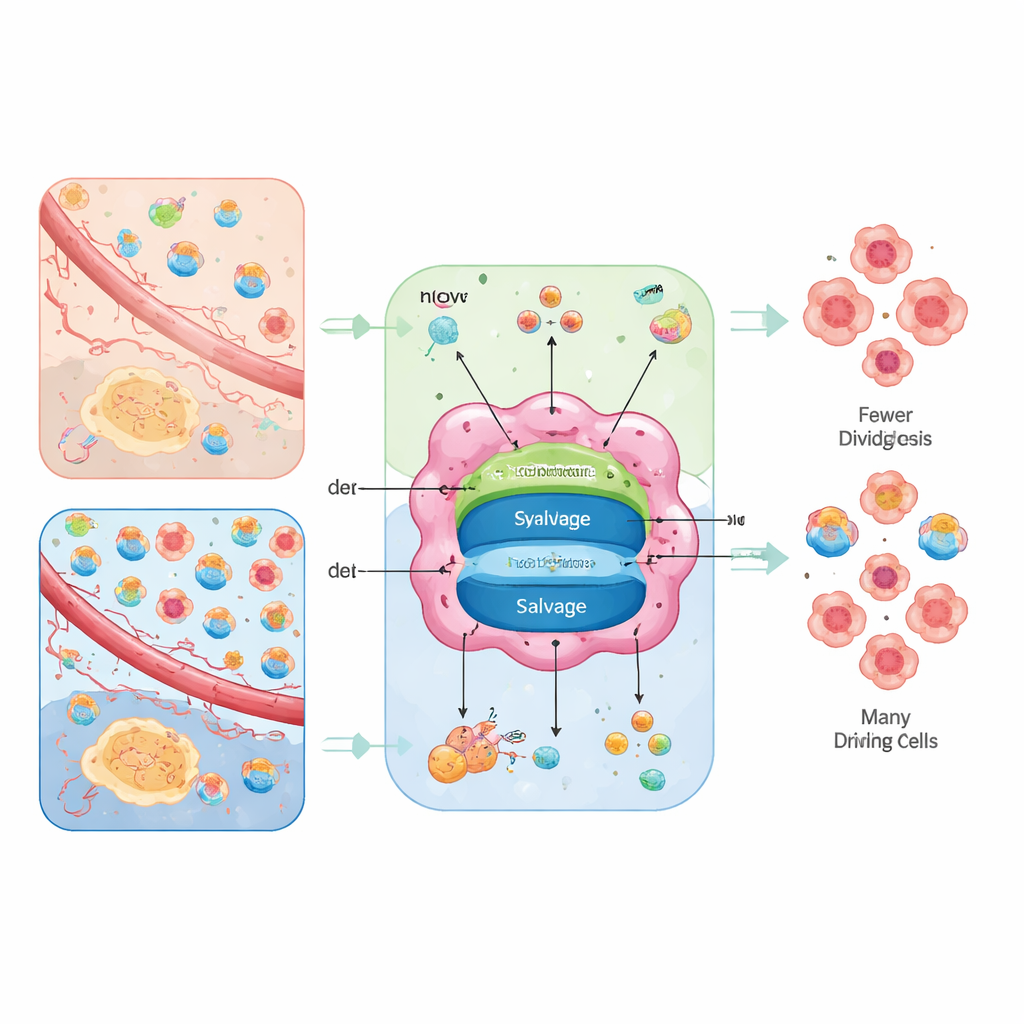
Dwie drogi do tych samych składników
Komórki mogą wytwarzać nukleotydy od podstaw lub je odzyskiwać. Trasa „od podstaw”, nazywana syntezą de novo, składa pierścienie z podstawowych składników odżywczych, takich jak glukoza, aminokwasy, dwutlenek węgla i wodorowęglan, wykorzystując wieloetapowe reakcje pochłaniające dużo energii. Droga odzysku (salvage) bierze rozłożone zasady i nukleozydy z zewnątrz lub z odpadów komórkowych i przekształca je z powrotem w użyteczne nukleotydy przy znacznie mniejszym koszcie energetycznym. Guzy korzystają z obu opcji, ale równowaga między nimi zależy od wewnętrznego zapasu energii i od tego, co dostarcza otaczająca tkanka.
Jak mikrośrodowisko guza kieruje wyborem
Autorzy przedstawiają zaopatrzenie w nukleotydy jako problem „trasowania kształtowanego przez środowisko”. W słabiej odżywionych obszarach, gdzie są dostępne aminokwasy, ale brakuje wolnych nukleozydów, komórki nowotworowe silnie polegają na szlakach de novo i stają się wrażliwe na leki blokujące te etapy. W lepiej perfundowanych rejonach, gdzie krew dostarcza wiele nukleozydów lub gdy mitochondria są osłabione, guzy mogą bardziej polegać na ścieżce salvage, stając się wtedy wrażliwe na blokery transporterów zapobiegające pobieraniu nukleozydów. Gdy obie opcje są dostępne, guzy wykazują elastyczność metaboliczną i mogą unikać działania pojedynczych leków; gdy obie są zablokowane, komórki zatrzymują replikację DNA, kumulują uszkodzenia i mogą obumrzeć lub przejść w bardziej dojrzałe, mniej agresywne stany.
Ukryte linie wsparcia zaopatrujące produkcję nukleotydów
Utrzymanie „fabryk nukleotydów” wymaga kilku obwodów wspierających. Szlak pentozofosforanowy dostarcza szkieletu cukrowego i mocy redukcyjnej; glutamina i cykl energetyczny w mitochondriach dostarczają azotu i asparaginianu; chemia seryny, glicyny i folianów oddaje jednostki jednowęglowe kończące pierścienie; wodorowęglan wnosi niezbędne atomy węgla. Onkogeny takie jak PI3K–AKT–mTORC1, RAS–MAPK i MYC zwiększają aktywność tych szlaków razem, podkręcają kluczowe enzymy, a nawet organizują kompleksy wieloenzymatyczne, które efektywnie kierują nietrwałymi pośrednikami. W przeciwieństwie do tego sensory stresu, takie jak LKB1–AMPK i p53, zwykle działają jak hamulce, ograniczając produkcję nukleotydów, gdy energia lub integralność DNA są zagrożone — hamulce, które wiele guzów wyłącza.
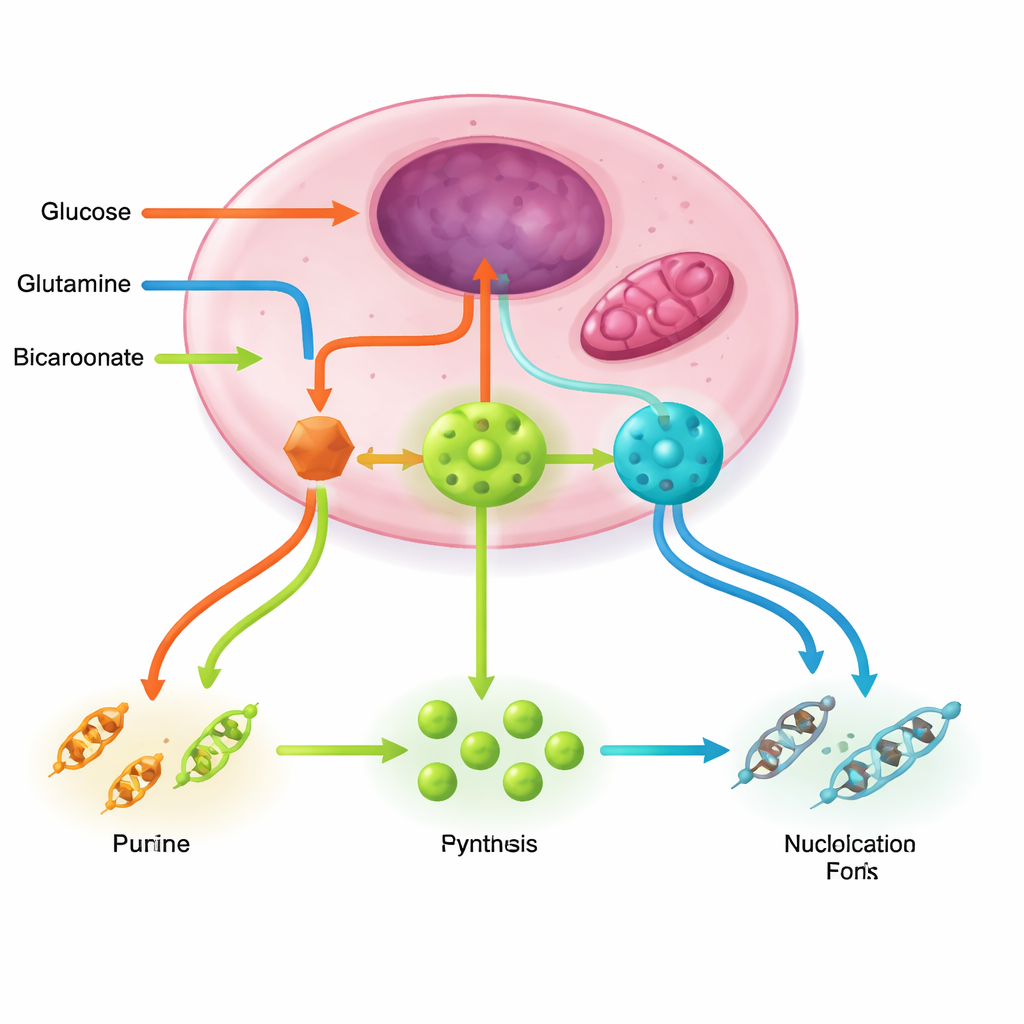
Stara chemioterapia, nowa logika metaboliczna
Ponieważ szybko rosnące komórki tak bardzo zależą od nukleotydów, niektóre z najwcześniejszych chemioterapii celowały w tę słabość. Klasyczne leki, takie jak metotreksat, 5‑fluorouracyl, cytarabina, gemcytabina i różne analogi purynowe, albo blokują wykorzystanie folianów, albo hamują specyficzne enzymy, albo podszywają się pod wadliwe składniki budulcowe, które zatruwają DNA i RNA. Przegląd ujmuje te leki przez pryzmat modelu trasowania, wyjaśniając, dlaczego skutki uboczne i oporność są powszechne: tkanki niezłośliwe też potrzebują nukleotydów, a guzy często potrafią przekierować przepływ przez salvage lub równoległe ścieżki, gdy jedno ogniwo zostanie zablokowane.
Strategie nowej generacji i otwarte pytania
Nowsze podejścia mają być bardziej selektywne, uderzając w elementy sieci silniej faworyzowane przez nowotwory. Opracowywane są eksperymentalne leki przeciw mitochondrialnym enzymom jednowęglowym, takim jak MTHFD2, enzymowi syntezy pirymidyn DHODH oraz enzymom purynowym, takim jak IMPDH i PAICS, często w kombinacjach, które także blokują transportery salvage. Autorzy proponują praktyczne markery — takie jak poziomy transporterów, gęstość naczyń krwionośnych, sprawność mitochondriów i ekspresja konkretnych enzymów metabolicznych — aby ustalić, które guzy bardziej polegają na de novo lub salvage i dopasować pacjentów do terapii ukierunkowanych na odpowiednie ścieżki. Patrząc w przyszłość, zwracają uwagę na kluczowe pytania, w tym jak te trasy zmieniają się w przestrzeni i czasie w realnych guzach, jak otaczające komórki odpornościowe i zrębu kształtują dostępność nukleotydów oraz jak zaprojektować tolerowane schematy dawkowania, które wykorzystają stres replikacyjny bez nadmiernego obciążenia tkanek normalnych. Razem praca ta argumentuje, że zrozumienie i ukierunkowanie metabolizmu nukleotydów może przekształcić podstawową konieczność podziału komórki w potężne, spersonalizowane narzędzie przeciw nowotworom.
Cytowanie: Vidal-Cruchez, O., Ben-Sahra, I. The oncogenic control of nucleotide synthesis. Oncogenesis 15, 17 (2026). https://doi.org/10.1038/s41389-026-00608-2
Słowa kluczowe: metabolizm nukleotydów, metabolizm nowotworów, synteza de novo, ścieżki odzysku, terapie metaboliczne