Clear Sky Science · pl
Teriflunomid modyfikuje oś PD-1/PD-L1 i wzmacnia odporność przeciwnowotworową w raku jelita grubego
Wykorzystanie leku na stwardnienie rozsiane przeciwko rakowi jelita
Wiele nowoczesnych terapii przeciwnowotworowych dąży do pobudzenia układu odpornościowego, by lepiej rozpoznawał i atakował guzy. Jednak u większości chorych na raka jelita grubego obecne terapie immunologiczne dają ograniczone korzyści. W badaniu tym przeanalizowano niespodziewanego sojusznika: teriflunomid, od dawna stosowaną pigułkę na stwardnienie rozsiane, i pokazano, jak może on przestawić kluczowy „hamulec” immunologiczny, aby pomóc własnym limfocytom T zabójcom zmniejszać nowotwory okrężnicy w modelach eksperymentalnych. 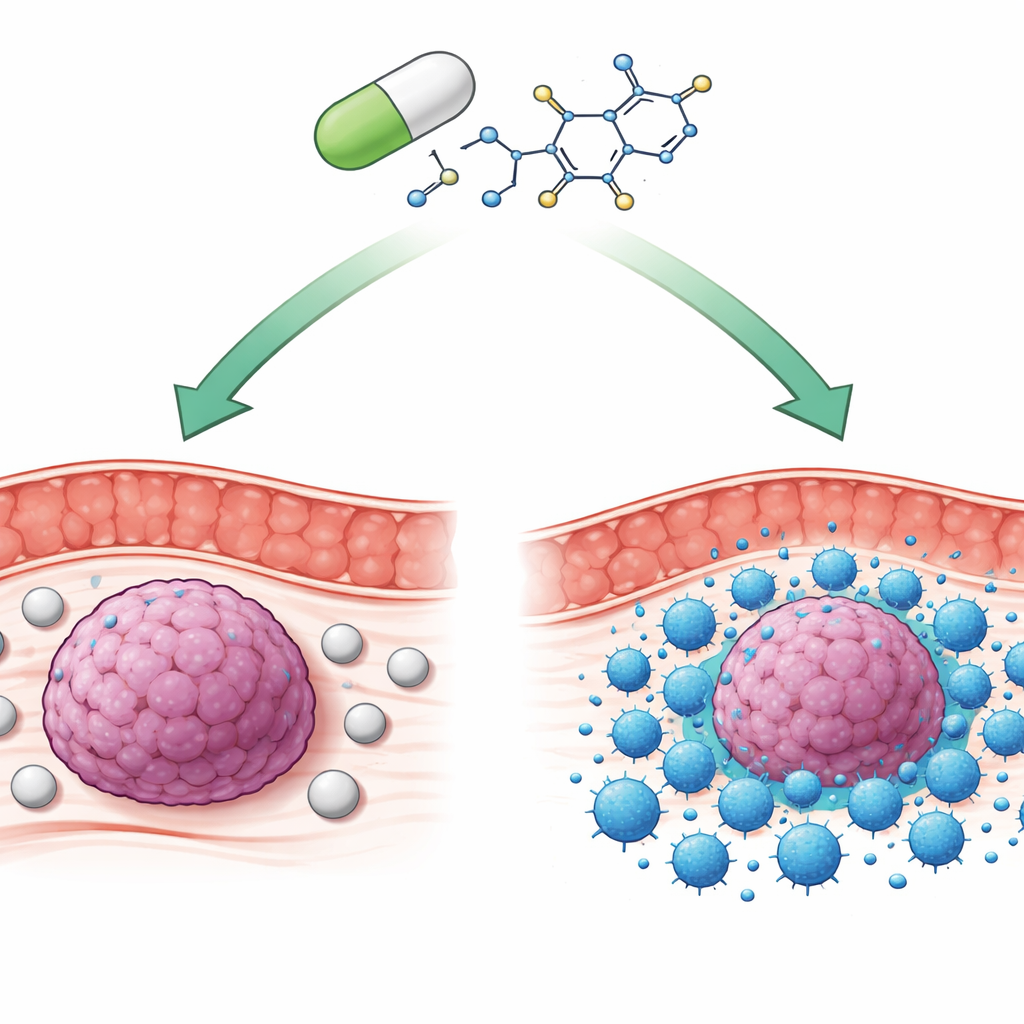
Hamulec organizmu przeciw atakowi immunologicznemu
Nasz układ odpornościowy działa dzięki równowadze między gazem a hamulcem. Jednym z głównych hamulców jest molekularne przywitanie między dwoma białkami zwanymi PD-1, obecnym na limfocytach T, oraz PD-L1, często eksponowanym na komórkach nowotworowych. Gdy się łączą, limfocyty T ulegają wyczerpaniu i przestają atakować, co pozwala nowotworom rosnąć niezauważenie. Obecne leki blokujące to „uściski dłoni” — głównie przeciwciała podawane w lecznictwie — zrewolucjonizowały terapię niektórych nowotworów. Jednak w większości raków jelita grubego, zwłaszcza w powszechnym typie o stabilnych mikrosatelitach, leki te działają słabo, a wielu pacjentów albo w ogóle nie reaguje, albo z czasem nabywa oporność.
Stary lek z nową misją
Teriflunomid to lek doustny stosowany od lat w leczeniu stwardnienia rozsianego poprzez uspokajanie nadaktywności komórek odpornościowych. Ze względu na udokumentowane bezpieczeństwo u ludzi jest atrakcyjnym kandydatem do ponownego wykorzystania, jeśli wykaże się, że może wspierać układ odpornościowy w kontekście nowotworów, a nie tylko go tłumić. Badacze sprawdzili, czy teriflunomid może działać bezpośrednio na układ PD-1/PD-L1 w komórkach raka jelita grubego i w limfocytach T. Na kilku liniach ludzkich komórek raka okrężnicy hodowanych w laboratorium stwierdzono, że teriflunomid zmniejsza ilość białka PD-L1 na komórkach nowotworowych bez bezpośredniego ich zabijania w stosowanych dawkach. Co ciekawe, efekt ten nie wynikał z wyłączenia genu PD-L1; zamiast tego lek przyspieszał rozkład białka PD-L1 w komórkowych „centrach recyklingu” zwanych lizosomami.
Blokowanie „uścisku dłoni” i wzmacnianie limfocytów T
Aby zbadać, jak teriflunomid wpływa bezpośrednio na hamulec immunologiczny, zespół przeanalizował jego wpływ na wiązanie PD-1 z PD-L1. Testy biochemiczne i modelowanie komputerowe wskazały, że teriflunomid może przyłączać się do samego PD-1, wnikając w obszar, do którego zwykle przyczepia się PD-L1. Ten bezpośredni kontakt blokował interakcję PD-1/PD-L1 przy bardzo niskich stężeniach leku. W zmodyfikowanych układach komórkowych imitujących punkt kontrolny immunologiczny dodanie teriflunomidu przywracało sygnalizację wewnątrz limfocytów T, co świadczyło o zwolnieniu hamulca. Gdy komórki nowotworowe i limfocyty T hodowano razem, teriflunomid zarówno obniżał poziomy PD-L1 na komórkach nowotworowych, jak i zwiększał markery aktywacji i zdolności zabijania przez limfocyty T.
Z płytki Petriego do myszy z guzami
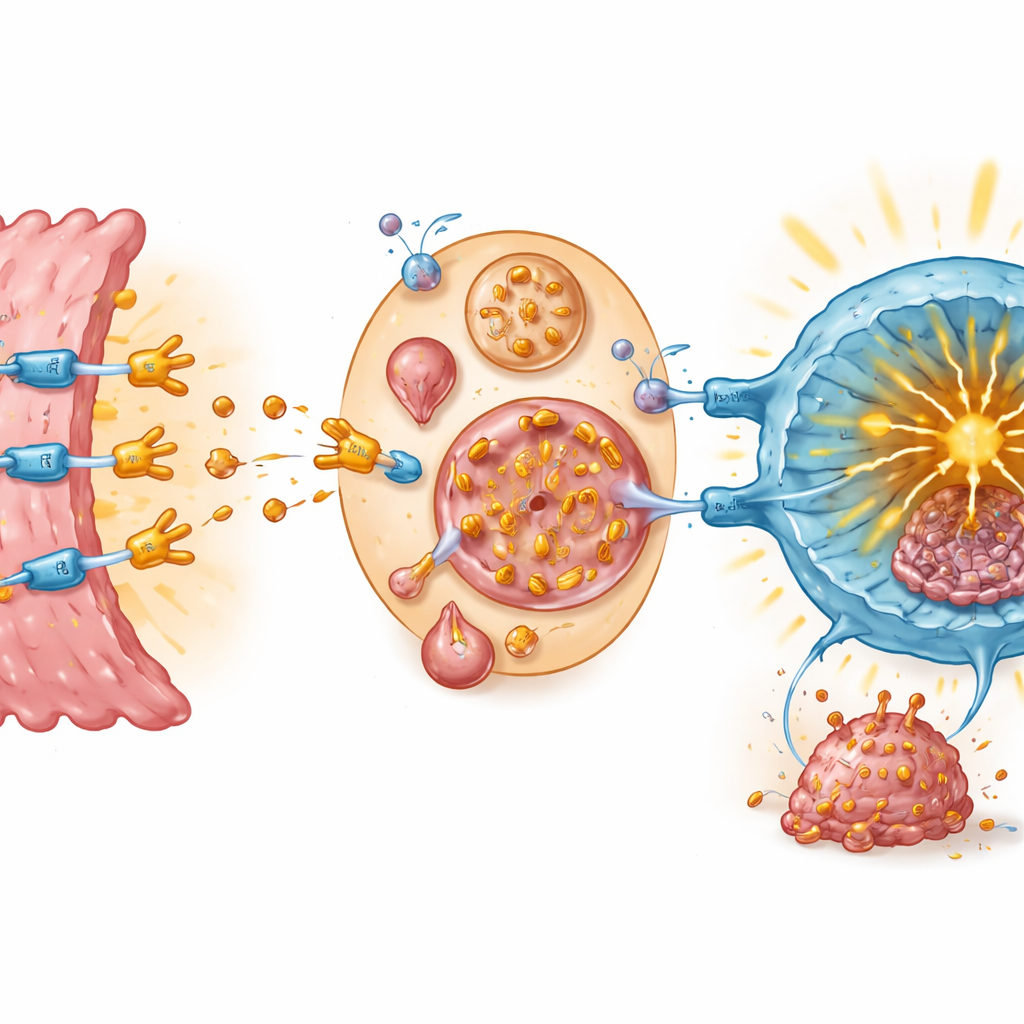
Co to może oznaczać dla przyszłej opieki onkologicznej
Dla osoby niezaznajomionej z tematem kluczowy przekaz jest taki, że teriflunomid wydaje się działać jako podwójnie działający bloker punktu kontrolnego: przyłącza się do PD-1 na limfocytach T, by zapobiec paraliżującemu „uściskowi dłoni”, a jednocześnie skłania komórki nowotworowe do pozbycia się osłony PD-L1. Te działania razem pozwalają limfocytom zabójcom napływać do guzów i skuteczniej je atakować w modelach raka jelita grubego. Ponieważ teriflunomid jest już zatwierdzony, a jego profil bezpieczeństwa dobrze opisany, może trafić do badań onkologicznych szybciej niż całkowicie nowy lek. Choć potrzebne są jeszcze badania u ludzi, praca ta sugeruje, że znana pigułka na stwardnienie rozsiane mogłaby kiedyś stać się częścią strategii łączonych pomagających pacjentom z rakiem okrężnicy, którzy nie odnoszą korzyści z obecnych immunoterapii.
Cytowanie: Han, J.H., Lee, EJ., Park, YH. et al. Teriflunomide modulates the PD-1/PD-L1 axis and enhances antitumor immunity in colorectal cancer. Oncogenesis 15, 15 (2026). https://doi.org/10.1038/s41389-026-00607-3
Słowa kluczowe: immunoterapia raka jelita grubego, hamulec PD-1 PD-L1, teriflunomid, limfocyty CD8, ponowne zastosowanie leku