Clear Sky Science · pl
Inhibicja transkrypcji ADPGK zależnej od ZBTB7B przez NEDD4 hamuje glikolizę i rozwój gruczolakoraka płuca
Dlaczego te badania mają znaczenie
Gruczolakorak płuca to najczęstsza postać raka płuca i często bywa wykrywany dopiero po cichym postępie choroby, kiedy terapie działają gorzej. Jednym z powodów, dla których te guzy są trudne do opanowania, jest to, że komórki nowotworowe przeprogramowują sposób, w jaki spalają cukier, co zapewnia im dodatkowe paliwo do wzrostu, przerzutów i oporności na leki. W tym badaniu odkryto wcześniej nieznany molekularny „termoregulator”, który może podkręcać lub przygasać ten system spalania cukru w komórkach gruczolakoraka płuca, wskazując na nowe sposoby głodzenia guza bez szkody dla reszty organizmu.
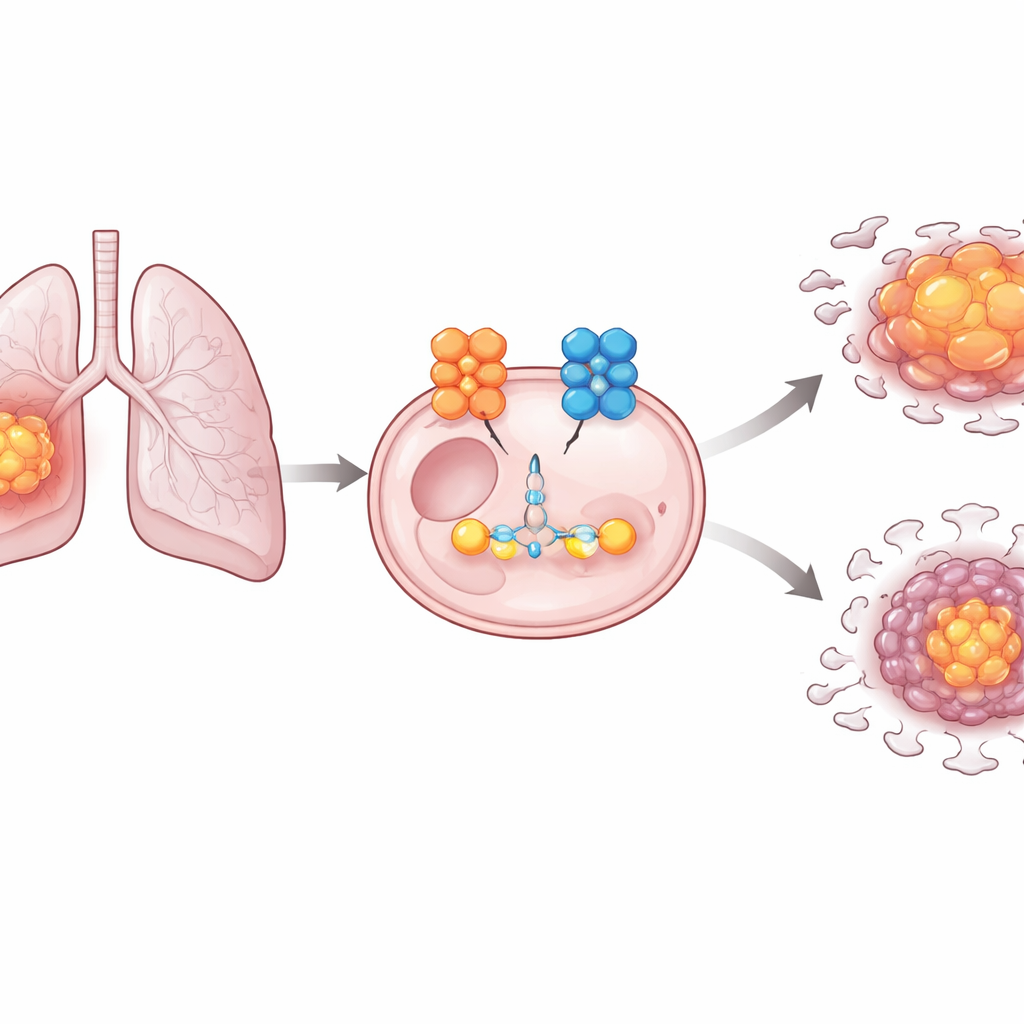
Nowotwór żyjący na cukrze
Komórki nowotworowe często silnie polegają na glikolizie — szybkiej, lecz mało wydajnej drodze przetwarzania glukozy na energię i elementy budulcowe — nawet gdy tlenu jest pod dostatkiem. Ta zmiana metaboliczna pomaga guzom szybko rosnąć i przetrwać w trudnych warunkach, takich jak ubogi dopływ krwi czy stres związany z leczeniem. W gruczolakoraku płuca znamy wiele pojedynczych enzymów biorących udział w glikolizie, ale mniej jasne były przełączniki kontrolujące, kiedy są wytwarzane i jak intensywnie działają. Autorzy postanowili zidentyfikować kluczowe regulatorowe ogniwa łączące kontrolę genową, stabilność białek i zmienione wykorzystanie cukru w tej chorobie.
Niespodziewany promotor wzrostu guza
Badacze skupili się na białku zwanym ZBTB7B, wcześniej znanym z ról w komórkach odpornościowych i metabolizmie tłuszczów. Analiza dużych zbiorów danych pacjentów i próbek nowotworowych wykazała, że poziomy białka ZBTB7B są konsekwentnie wyższe w tkance gruczolakoraka płuca i liniach komórkowych niż w normie, a pacjenci, których guzy zawierają więcej tego białka, mają gorsze rokowanie. Gdy ZBTB7B został zmniejszony w hodowanych komórkach raka płuca, komórki dzieliły się wolniej, tworzyły mniej kolonii i mniej migrowały — wszystkie te cechy wskazują na osłabienie zachowań sprzyjających nowotworowi. Te same komórki zużywały też mniej glukozy, wydzielały mniej mleczanu i produkowały mniej ATP, co ujawniło, że ZBTB7B wspiera „cukrożerną” aktywność nowotworu.
W centrum uwagi nietypowy enzym cukrowy
Aby zrozumieć, jak ZBTB7B zwiększa glikolizę, zespół połączył dane o wiązaniu w całym genomie z mapami aktywności genów i skupił się na stosunkowo nietypowym enzymie o nazwie ADPGK. W przeciwieństwie do typowych heksokinaz, które używają ATP do zainicjowania glikolizy, ADPGK może wykorzystywać ADP, co pozwala komórkom przetwarzać glukozę nawet przy niskim stanie energetycznym. Autorzy wykazali, że ZBTB7B wiąże się bezpośrednio z krótkim regionem sekwencji kontrolnej genu ADPGK i włącza jego ekspresję, zwiększając zarówno poziom RNA, jak i białka. Gdy ADPGK został wyciszony, wzrost, ruchliwość i nasilona glikoliza wywołane przez nadmiar ZBTB7B w dużej mierze znikały, a przywrócenie ADPGK odtwarzało te sprzyjające nowotworowi cechy. To sugeruje, że ZBTB7B przesuwa komórki raka płuca w kierunku stanu o wysokiej glikolizie i intensywnym wzroście głównie poprzez ADPGK.
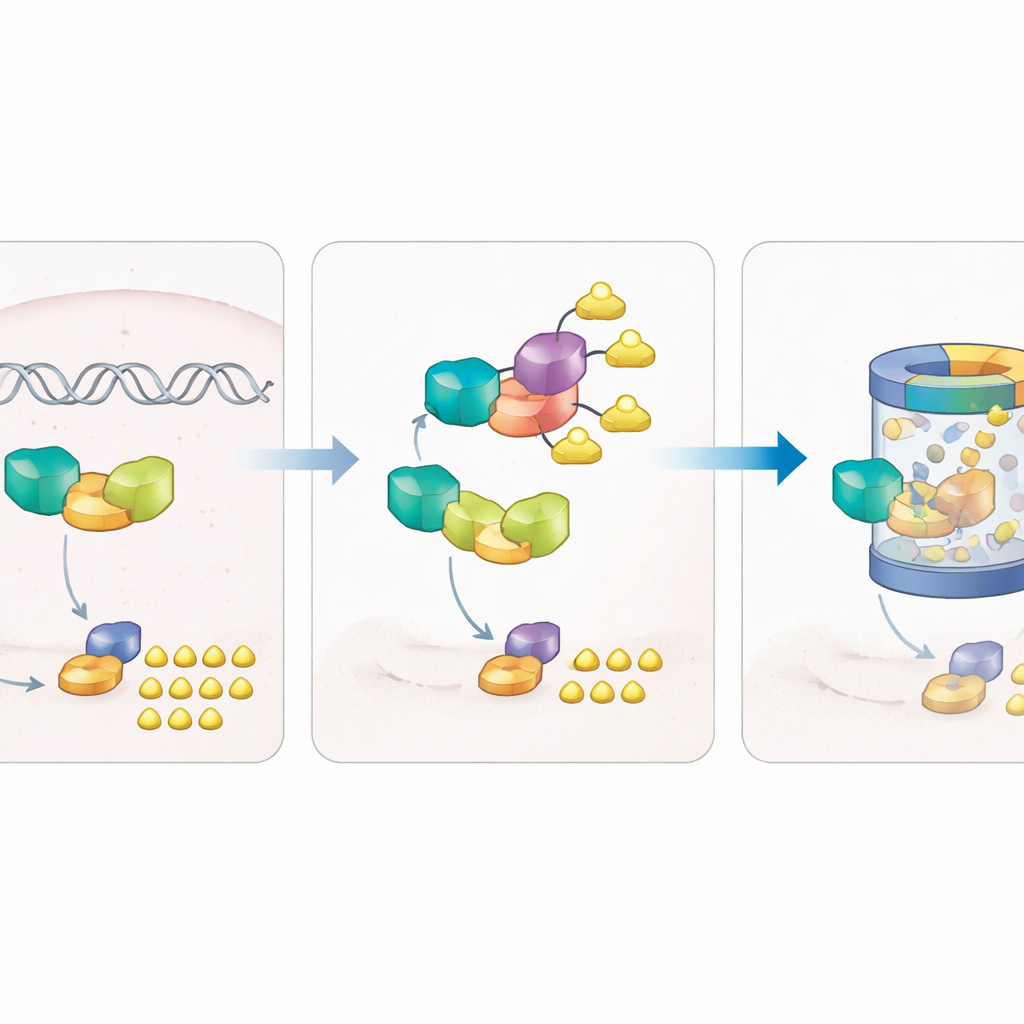
Wbudowany hamulec celujący w przełącznik cukrowy
Zagadkę pogłębiło odkrycie, że RNA ZBTB7B nie było podwyższone w guzach, mimo iż jego białko było. Wskazywało to na kontrolę po translacyjnej. Badacze odkryli, że inne białko, ligaza E3 NEDD4, fizycznie wiąże się z ZBTB7B i ozdabia je tagami ubikwityny w specyficznym miejscu, oznaczając je do zniszczenia przez komórkowy system recyklingu białek. Gdy NEDD4 był zwiększony, ZBTB7B stawał się mniej stabilny, poziomy ADPGK spadały, a glikoliza zwalniała; zmniejszenie NEDD4 wywoływało odwrotny efekt. Pojedyncza zmiana w opisanym miejscu na ZBTB7B chroniła je przed NEDD4 i zapobiegała jego rozkładowi. W modelach mysimy komórki raka płuca zaprojektowane tak, by produkować więcej NEDD4, tworzyły mniejsze, mniej glikolityczne guzy i mniej przerzutów do płuc, ale ponowne wprowadzenie ZBTB7B odwracało tę korzyść.
Co to oznacza dla przyszłych terapii
Wspólnie te ustalenia ujawniają nowy obwód kontrolny w gruczolakoraku płuca: ZBTB7B włącza ADPGK, zasilając glikolizę i progresję guza, podczas gdy NEDD4 działa jako naturalny hamulec, znakując ZBTB7B do usunięcia. Dla osób nietechnicznych można to porównać do pedału gazu (ZBTB7B–ADPGK) i stopy na hamulcu (NEDD4), które razem decydują, jak mocno „silnik” guza pracuje na cukrze. Projektując leki, które osłabią pedał gazu — blokując ZBTB7B lub ADPGK — lub wzmocnią hamulec przez zwiększenie działania NEDD4 na ZBTB7B, może stać się możliwe odcięcie ważnego źródła energii komórek gruczolakoraka płuca. Choć takie terapie pozostają na etapie koncepcyjnym, ta praca wskazuje konkretne cele molekularne dla przyszłych terapii przeciwnowotworowych ukierunkowanych na metabolizm.
Cytowanie: Liu, FP., Huang, T., Yang, HY. et al. Inhibition of ZBTB7B-mediated ADPGK transcription by NEDD4 impedes glycolysis and progression of lung adenocarcinoma. Oncogenesis 15, 14 (2026). https://doi.org/10.1038/s41389-026-00605-5
Słowa kluczowe: gruczolakorak płuca, metabolizm nowotworu, glikoliza, ligaza ubikwitynowa NEDD4, czynnik transkrypcyjny ZBTB7B