Clear Sky Science · pl
Profilowanie transkryptomiczne współhodowanych komórek nowotworowych i gospodarza wskazuje niedotlenienie jako czynnik napędzający antyproliferacyjny efekt komórek mięśni szkieletowych na komórki nowotworowe
Dlaczego niektóre tkanki opierają się rozprzestrzenianiu się raka
Nowotwór zazwyczaj staje się śmiertelny, gdy komórki guza opuszczają pierwotne miejsce i osiedlają się w odległych narządach. Dziwnie, niektóre tkanki, jak płuca, są częstym miejscem osadzania się, podczas gdy inne, takie jak mięsień szkieletowy, niemal nigdy nie zostają skolonizowane, mimo że stanowią dużą część masy ciała. To badanie stawia proste, lecz istotne pytanie dla pacjentów i lekarzy: co w mięśniu sprawia, że jest on tak złym podłożem do wzrostu komórek nowotworowych i czy zrozumienie tej naturalnej obrony może zmienić nasze podejście do leczenia przerzutów?
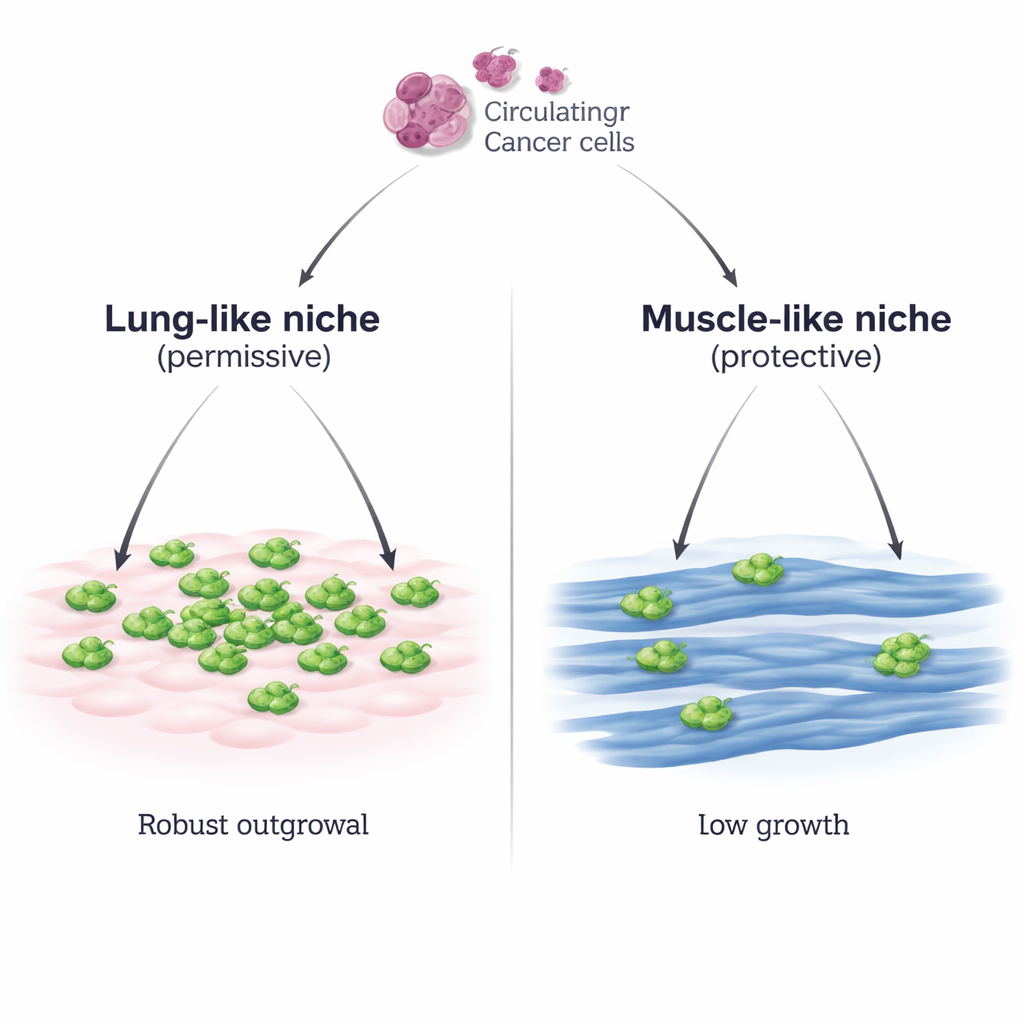
Dwie okolice dla podróżujących komórek guza
Naukowcy zbudowali kontrolowany system laboratoryjny, który naśladuje dwa różne środowiska, jakie mogą napotkać komórki raka piersi: środowisko przypominające płuco z komórek tkanki łącznej płuc (MLg) oraz środowisko przypominające mięsień z dojrzałych włókien mięśni szkieletowych (miotuby C2C12). Umieścili mysie komórki raka piersi na każdej z warstw i obserwowali, co się dzieje. Na komórkach płucnych komórki nowotworowe dobrze przylegały, a następnie szybko się mnożyły, tworząc gęste skupiska. Na komórkach mięśniowych przyczepiały się równie dobrze, ale ich wzrost pozostawał rozproszony i powolny, nawet gdy zwiększono liczbę początkowych komórek nowotworowych lub użyto innej linii raka piersi. Osobna linia mięśniowa (Sol8) wykazała tę samą zdolność do hamowania wzrostu nowotworu, co podkreśla, że jest to ogólna właściwość komórek mięśniowych, a nie specyfika jednej linii komórek.
Jak komórki nowotworowe i gospodarza przeprogramowują swoją aktywność
Aby zrozumieć, co działo się wewnątrz komórek, zespół wyizolował komórki nowotworowe i komórki gospodarza z tych mieszanin hodowlanych i zsekwencjonował ich RNA, co odzwierciedla, które geny są włączone lub wyłączone. Komórki nowotworowe siedzące na włóknach mięśniowych wykazywały znacznie bardziej rozległe zmiany aktywności genów niż te rosnące na komórkach płucnych, co sugeruje, że środowisko mięśniowe zmusza je do silnej adaptacji. W otoczeniu mięśniowym komórki nowotworowe uruchomiły programy związane z cechami przypominającymi mięsień, przetwarzaniem energii oraz, co zaskakujące, odpowiedziami na niskie stężenie tlenu (niedotlenienie). Jednocześnie zwykłe programy genowe napędzające szybkie podziały komórek zostały przyciszone. Dla porównania, komórki nowotworowe na komórkach płuc utrzymywały wyraźnie skupiony na wzroście profil i potrzebowały znacznie mniejszego przeprogramowania, co jest zgodne z ideą, że nisza przypominająca płuco jest przyjazna i łatwa do wykorzystania przez komórki nowotworowe.
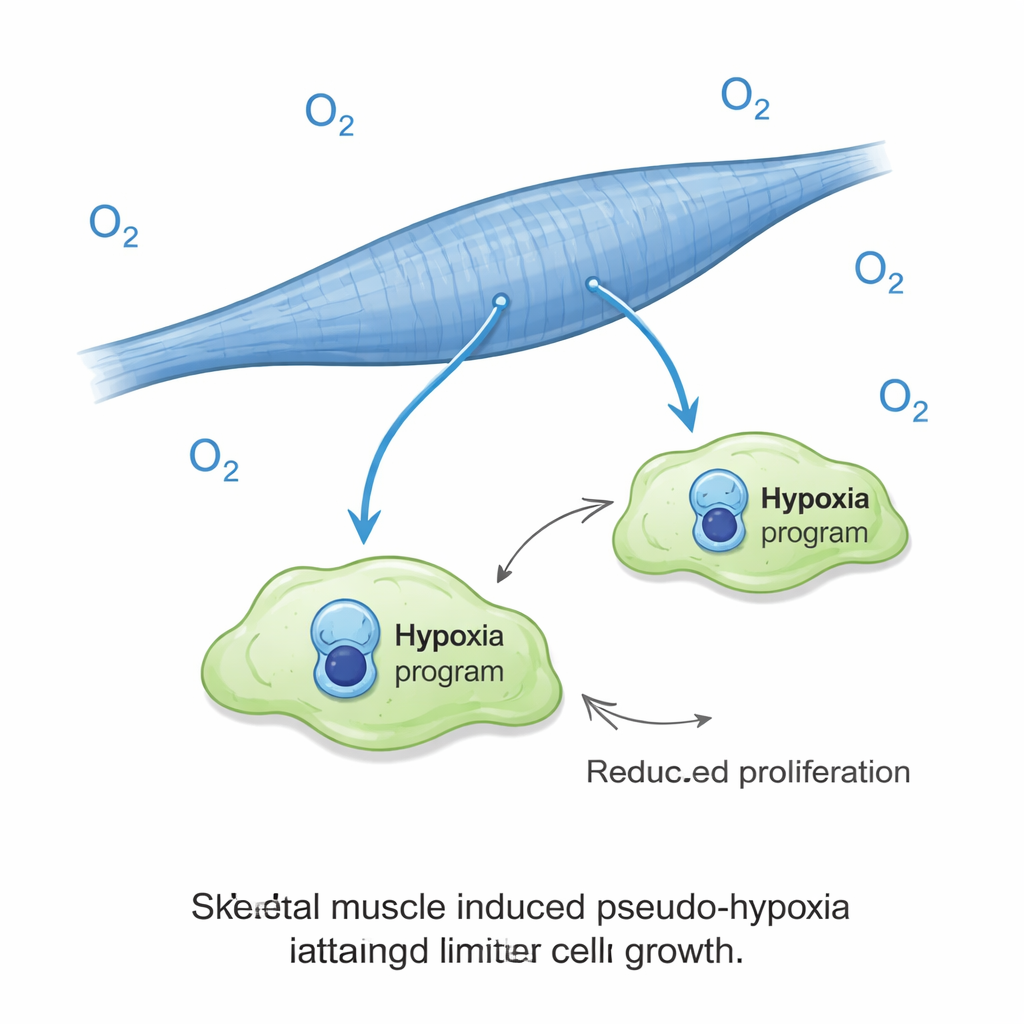
Zaskakująca rola sygnałów niedotlenienia
Jednym z najbardziej uderzających wyników było to, że komórki nowotworowe na włóknach mięśniowych włączały sygnaturę genową przypominającą niedotlenienie, mimo że były hodowane przy normalnym stężeniu tlenu. W większości guzów niedotlenienie jest złym prognostykiem, zwykle związanym z agresywnym zachowaniem i gorszymi wynikami. Tutaj wiązało się ono z odwrotnym efektem: słabym wzrostem. Naukowcy następnie wystawili hodowle na rzeczywiście niskie stężenie tlenu i stwierdzili, że prawie całkowicie zahamowało to ekspansję komórek nowotworowych na mięśniach, podczas gdy w środowisku przypominającym płuco wręcz pobudzało wzrost nowotworu. Innymi słowy, ten sam sygnał, który zwykle pomaga guzom przetrwać, stał się hamulcem, gdy komórki nowotworowe znalazły się w środowisku mięśniowym. Efekt tlenu nie wydawał się wynikać z prostych zmian stężenia mleczanu, kwasowości czy dostępności cukru w pożywce hodowlanej.
Więcej niż tylko czynniki wydzielane
Zespół sprawdził również, czy prostsze rozpuszczalne substancje uwalniane przez komórki mięśniowe mogą tłumaczyć ich ochronny efekt. Dodanie dodatkowego mleczanu, zmiana pH, modyfikacja poziomów glukozy czy hodowla komórek nowotworowych w pożywce, która wcześniej kontaktowała się z komórkami mięśniowymi, nie odtworzyły silnej supresji obserwowanej w bezpośrednich współhodowlach. To sugeruje, że kluczowe są bliski kontakt fizyczny lub bardzo krótkodystansowe sygnały na powierzchni komórek, które popychają komórki mięśniowe do wprowadzenia komórek nowotworowych w stan niskiego wzrostu, możliwej dormancji. Co ciekawe, same komórki mięśniowe pozostawały stosunkowo stabilne w swojej aktywności genowej w obliczu obecności raka, podczas gdy komórki płucne były łatwiej przeprogramowywane, co podkreśla mięsień jako odporną na przerzuty tkankę.
Co to oznacza dla pacjentów i terapii
Podsumowując, badanie pokazuje, że mięsień szkieletowy działa jako wrogie siedlisko, które zmusza komórki nowotworowe do stanu przypominającego niedotlenienie o niskiej proliferacji, nawet gdy tlenu jest pod dostatkiem. To pomaga wyjaśnić, dlaczego mięsień jest tak rzadkim miejscem przerzutów. Wynika z tego także ostrzeżenie dla rozwoju leków: terapie mające na celu blokowanie sygnalizacji niedotlenienia w całym organizmie mogą niezamierzenie osłabić tę naturalną mięśniową obronę, ułatwiając komórkom nowotworowym wzrost tam, gdzie normalnie by tego nie zrobiły. Zrozumienie i zachowanie, a nawet naśladowanie ochronnych cech tkanki mięśniowej, może otworzyć nowe drogi zapobiegania i kontroli choroby przerzutowej.
Cytowanie: Aunan, A., Claeyssen, C., Abdelhalim, M. et al. Transcriptomic profiling of co-cultured cancer-host cells identifies hypoxia as a driver of the skeletal muscle cell’s anti-proliferative effect on cancer cells. Oncogenesis 15, 7 (2026). https://doi.org/10.1038/s41389-026-00601-9
Słowa kluczowe: przerzuty nowotworowe, mięsień szkieletowy, niedotlenienie, mikrosrodowisko guza, uśpienie nowotworu