Clear Sky Science · pl
Wchłanianie kwasów tłuszczowych pośredniczone przez FABP4 sprzyja tworzeniu się starzenia komórek CD8+ przez peroksydację lipidów w mikrośrodowisku bogatym w adipocyty w raku jajnika
Dlaczego tłuszcz i komórki odpornościowe mają znaczenie w raku jajnika
Rak jajnika często rozprzestrzenia się do jamy brzusznej, gdzie napotyka duże złogi tkanki tłuszczowej. To tłuste otoczenie nie jest jedynie biernym tłem — aktywnie kształtuje zachowanie komórek odpornościowych. W szczególności może osłabiać komórki CD8, czyli tzw. „zabójcze” limfocyty T, które powinny atakować guzy. W badaniu przeanalizowano, w jaki sposób substancje pochodzące z tłuszczu wpędzają te komórki w stan starzenia się (senescencji) oraz czy zablokowanie kluczowego białka transportującego tłuszcze może przywrócić ich zdolność do zwalczania nowotworu.
Tłuszczowe otoczenie, które postarza obrońców immunologicznych
Lekarze od dawna obserwują, że wiele pacjentek z zaawansowanym rakiem jajnika gromadzi płyn w jamie brzusznej i ma guzy osadzone w tkankach bogatych w tłuszcz, zwanych siecią większą. Analiza danych z pojedynczych komórek (single-cell RNA) od pacjentek oraz badanie próbek guza pod mikroskopem wykazały, że komórki CD8 znajdujące się w pobliżu tych złogów tłuszczu częściej wykazują cechy starzenia komórkowego, czyli senescencji. Te „zestarzałe” limfocyty gromadzą pigmenty odpadowe, zaprzestają się dzielić i wydzielają sygnały zapalne zamiast zabijać komórki nowotworowe. Zarówno w próbkach ludzkich, jak i w modelach mysich, komórki CD8 pobrane z obszarów guza bogatych w tłuszcz i płyn były wyraźnie bardziej senescentne niż te z węzłów chłonnych czy śledziony, co łączy bogate w adipocyty mikrośrodowisko guza bezpośrednio ze starzeniem się limfocytów T.
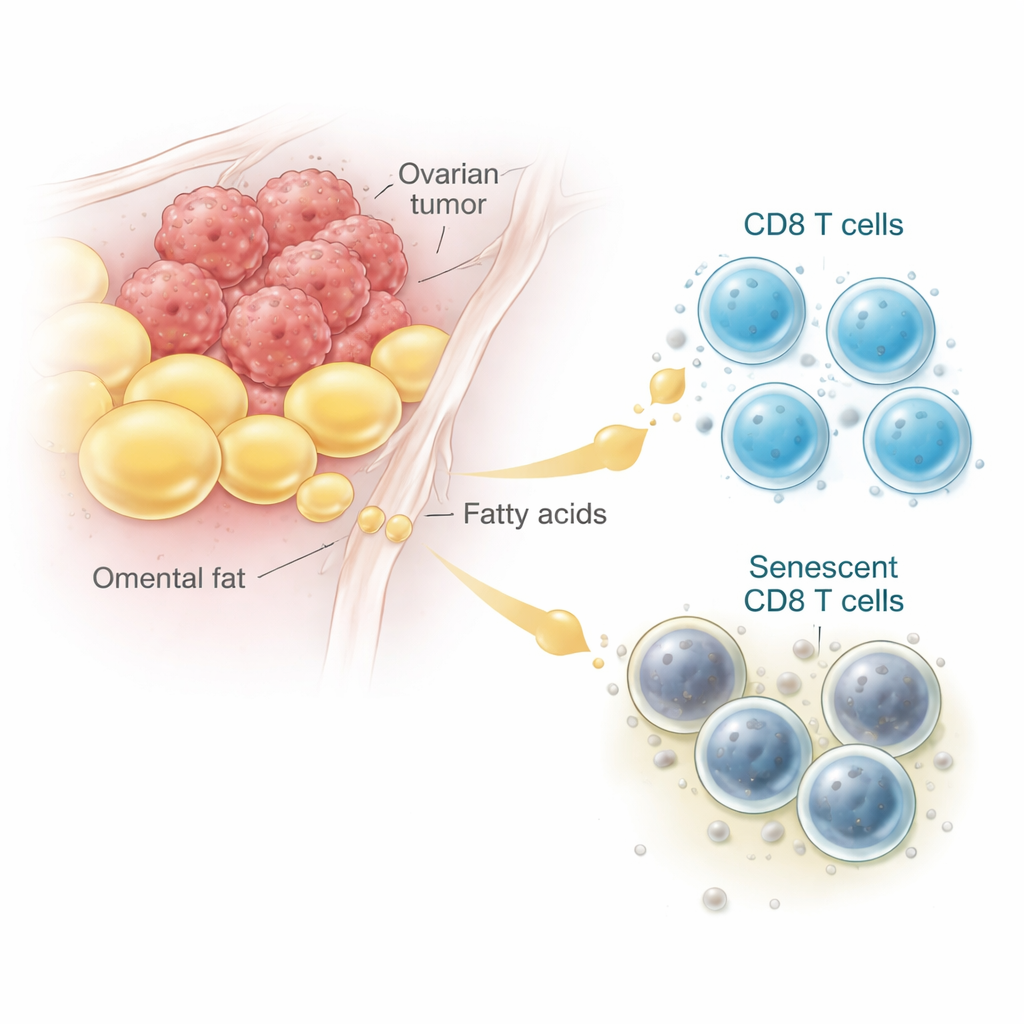
Jak powszechny kwas tłuszczowy zmienia pożyteczne paliwo w szkodę
Aby zrozumieć, co tłuszcz robi komórkom T, zespół odtworzył środowisko guza w laboratorium. Hodowali komórki raka jajnika razem z mysimi komórkami CD8, a następnie dodawali ekstrakty z tkanki tłuszczowej lub specyficzny kwas tłuszczowy — kwas oleinowy — który jest obfity w płynie związanym z rakiem jajnika. Przy umiarkowanych i wysokich dawkach kwas oleinowy powodował, że większy odsetek komórek CD8 przechodził w stan senescencji — ale tylko w obecności komórek nowotworowych. Zamiast zużywać napływający tłuszcz jako źródło energii, limfocyty gromadziły lipidy, które ulegały uszkodzeniom chemicznym w procesie zwanym peroksydacją lipidów. Analizy genetyczne i lipidowe wykazały wzrost markerów utlenionych tłuszczów i stresu, podczas gdy produkcja energii z tłuszczów nie wzrastała. Krótko mówiąc, w obecności guza tłuszcz, który powinien służyć jako paliwo, był kierowany w reakcje powodujące uszkodzenie i postarzenie komórek T.
Transporter tłuszczu FABP4 jako kluczowy strażnik bramowy
Wnikliwsze badania wykazały, które cząsteczki kontrolują ten szkodliwy napływ tłuszczu. Stwierdzono, że białko transportujące zwane FABP4 jest silnie aktywowane w komórkach CD8 wystawionych na ekstrakty tłuszczowe lub kwas oleinowy. FABP4 działa jak promień, przenosząc długołańcuchowe kwasy tłuszczowe do wnętrza komórek. Gdy zablokowano FABP4 za pomocą małocząsteczkowego inhibitora (BMS309403) lub poprzez wyciszenie genetyczne, komórki T pobierały mniej tłuszczu, wykazywały mniejszą peroksydację lipidów i rzadziej przechodziły w stan senescencji. Te chronione limfocyty lepiej się dzieliły, produkowały więcej cząsteczek o działaniu przeciwnowotworowym, takich jak interferon-gamma i granzyme B, oraz wydzielały mniej sygnałów supresyjnych i zapalnych. Przywrócenie poziomów FABP4 odwracało te korzyści, potwierdzając, że transporter ten jest centralnym przełącznikiem łączącym pobieranie tłuszczu ze starzeniem się komórek T.
Od eksperymentów na myszach do potencjalnej strategii leczenia
Następnie zespół przetestował blokadę FABP4 u żywych myszy z rakiem jajnika, który rozprzestrzenił się w jamie brzusznej. Leczenie mysz inhibitorem FABP4 zmniejszyło pobieranie tłuszczu i uszkodzenia lipidowe w komórkach CD8 pobranych z płynu w jamie brzusznej, obniżyło odsetek senescentnych limfocytów i zwiększyło poziomy kluczowych molekuł efektorowych. Gdy inhibitor FABP4 połączono ze standardową chemioterapią, myszy miały mniej widocznych guzków nowotworowych, silniejsze odpowiedzi limfocytów T w śledzionie, węzłach chłonnych i w płynach ustrojowych oraz przeżywały dłużej niż zwierzęta otrzymujące wyłącznie chemioterapię. Wyniki te sugerują, że celowanie w metabolizm tłuszczów może zwiększyć skuteczność istniejących terapii przez ożywienie pierwszej linii obrony układu odpornościowego.
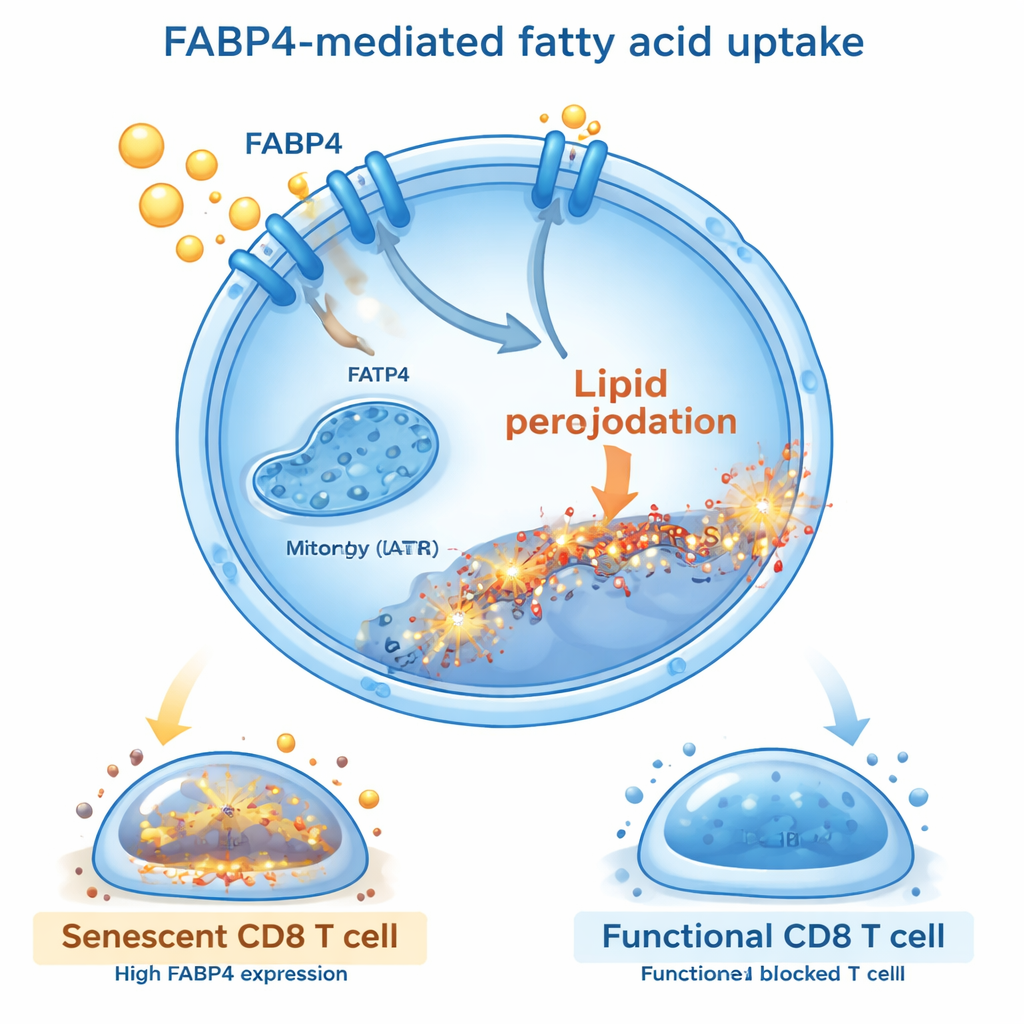
Co to oznacza dla pacjentek
Dla czytelników niebędących specjalistami kluczowa myśl jest taka: w raku jajnika ważny jest nie tylko sam nowotwór, lecz także tłuste sąsiedztwo, w którym on żyje. Molekuły pochodzące z tłuszczu, zwłaszcza niektóre kwasy tłuszczowe, mogą przedwcześnie postarzać „zabójcze” komórki T, odbierając im zdolność do ataku na nowotwór. Badanie identyfikuje transporter tłuszczu FABP4 jako głównego winowajcę tego procesu. Zablokowanie FABP4, przynajmniej u myszy, redukuje starzenie się komórek T, przywraca ich funkcję zabijania i poprawia efektywność chemioterapii. Choć potrzeba więcej badań, zanim stanie się to terapią dla pacjentek, praca otwiera nową ścieżkę: leczenie nie tylko samego nowotworu, lecz także metabolicznych pułapek w jego otoczeniu, które osłabiają układ odpornościowy.
Cytowanie: Yu, C., Li, X., Qian, X. et al. Fatty acid uptake mediated by FABP4 promotes the formation of CD8+T cell senescence through lipid peroxidation in the adipocyte-rich microenvironment of Ovarian Cancer. Oncogenesis 15, 9 (2026). https://doi.org/10.1038/s41389-026-00600-w
Słowa kluczowe: rak jajnika, senescencja komórek T, metabolizm kwasów tłuszczowych, mikrośrodowisko guza, FABP4