Clear Sky Science · pl
Reorganizację cytoszkieletu wywołaną przez nowy fusion keratyn K6-K14 promującą nowotworową pędowość i plastyczność komórkową poprzez selekcję cGAS-STING
Jak zmieniające kształt komórki nowotworowe przechytrzają swoje otoczenie
Komórki nowotworowe nie tylko rozmnażają się bez kontroli; uczą się też przeorganizowywać własny „szkielet” wewnętrzny, by przetrwać, ukryć się i rozprzestrzeniać. W badaniu pokazano, jak specyficzna strukturalna usterka w komórkach raka głowy i szyi może uszkadzać jądra komórkowe, uruchamiać wewnętrzny alarm niebezpieczeństwa, popychać komórki w stan uśpienia, a ostatecznie pozwalać im powrócić jako bardziej agresywne, inwazyjne komórki przypominające komórki macierzyste. Zrozumienie tej mechanicznej ścieżki ewolucji nowotworu może otworzyć nowe możliwości blokowania nawrotów i przerzutów.
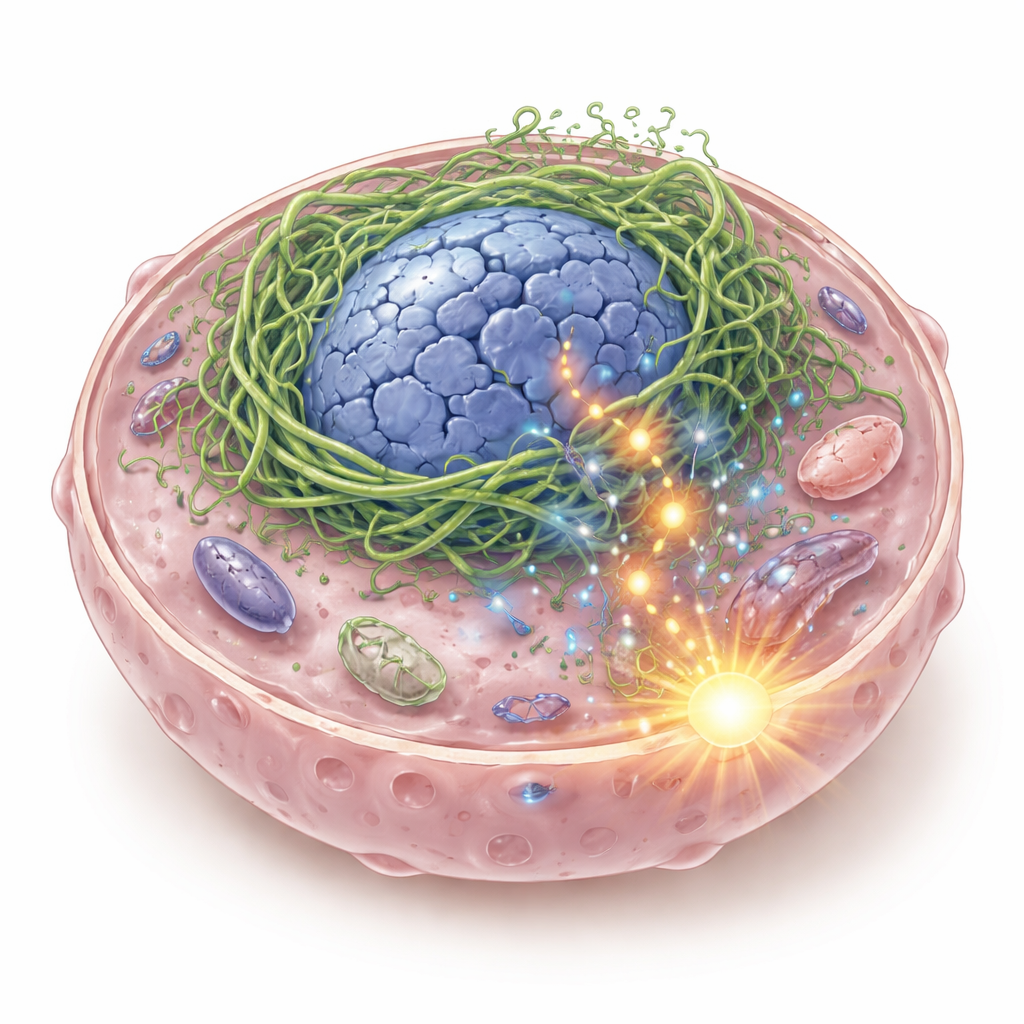
Pęknięty wewnętrzny szkielet z niebezpiecznymi konsekwencjami
W każdej komórce znajduje się elastyczny ruszt białkowych filamentów, który utrzymuje kształt komórki i jądra oraz pomaga w odczuwaniu sił fizycznych. Autorzy skupili się na keratynach, rodzinie białek rusztowania typowych dla tkanek nabłonkowych, w tym wyściełających jamę ustną i gardło. W niektórych rakach płaskonabłonkowych głowy i szyi odkryli hybrydową keratynę nazwaną K6-K14/V5, powstającą w wyniku połączenia dwóch genów keratynowych. Gdy to białko fuzyjne jest aktywowane w komórkach nowotworowych, nie tworzy gładkiej sieci podtrzymującej. Zamiast tego silnie zlepia się wokół jądra, deformując je w puste, zniekształcone struktury i powodując pęknięcia DNA. Fragmenty DNA wyciekają do cytoplazmy, gdzie wykrywa je układ rozpoznający zagrożenia zwany cGAS–STING, który zwykle uruchamia alarm przy obecności wirusowego DNA.
Od presji na śmierć komórki do ukrytego przetrwania
Bezpośredni skutek uszkodzeń jądra jest szkodliwy dla komórek nowotworowych: ich wzrost zwalnia i wiele z nich umiera. Jednak część potrafi przetrwać. Przeżywające komórki są silnie zależne od fizycznego otoczenia. Na standardowych płaskich plastikowych pojemnikach stopniowo zanikają, ale gdy hodowane są w miękkim żelu kolagenowym — bliższym strukturze prawdziwej tkanki — utrzymują się i pojawiają się ponownie jako populacja nazwana 3D-V5. Analizy aktywności genów pokazują, że te komórki reagują na trwający alarm z powodu uszkodzeń DNA przez uruchomienie autofagii, programu samoczyszczenia, który odzyskuje uszkodzone elementy, szczególnie wadliwe mitochondria. Ta reakcja pomaga im wejść w stan uśpienia o niskiej aktywności, co pozwala przetrwać stres zamiast zostać wyeliminowanym.
Uśpione komórki przepisują program i przygotowują się do migracji
Będąc uśpionymi, te przeżywające komórki cicho zmieniają swoje wewnętrzne programy. Zmieniają skład keratyn i przyjmują „częściową” przejściową tożsamość epitelialno-mezenchymalną (pEMT) — stan pośredni, który zachowuje niektóre cechy nabłonkowe, ale zyskuje elastyczność i ruchliwość. Zyskują znacznie większą zdolność do tworzenia sfer i zalążkowania nowych skupisk komórkowych, co jest cechą nowotworowej pędowości. Z czasem ich właściwości mechaniczne się odbudowują: jądra ponownie usztywniają się, odbudowują silne włókna aktynowe i rozwijają długie wypustki, które sondają i chwytają otaczającą macierz. Zwiększają też produkcję enzymów z rodziny metaloproteinaz macierzy (MMP), które rozkładają zewnątrzkomórkową sieć i torują drogę dla inwazji.
Rozmowa z sąsiednimi komórkami w celu zbudowania wspierającej niszy
Te przeprogramowane komórki nowotworowe nie działają w pojedynkę. Zespół zaobserwował, że komórki 3D-V5 wydzielają duże ilości drobnych pęcherzyków zwanych pozakomórkowymi pęcherzykami. Gdy te pęcherzyki oddziałują na pobliskie fibroblasty jamy ustnej — komórki tkanki łącznej — fibroblasty zmieniają swoją aktywność genową, stając się bardziej podobne do fibroblastów związanych z guzem, które wspierają wzrost nowotworu. Wiele wymienianych sygnałów kręci się wokół osi FGF–FGFR, rodziny czynników wzrostu i ich receptorów znanych z pobudzania proliferacji, plastyczności i oporności. Zarówno w hodowlach komórkowych, jak i w guzach w myszach, blokada aktywności FGFR zmniejszała tę przewagę wzrostu. U zwierząt guzy pochodzące z komórek 3D-V5 były słabo zróżnicowane, bardziej inwazyjne, bogate w markery komórek macierzystych i częściej rozprzestrzeniały się poza miejsce wstrzyknięcia.
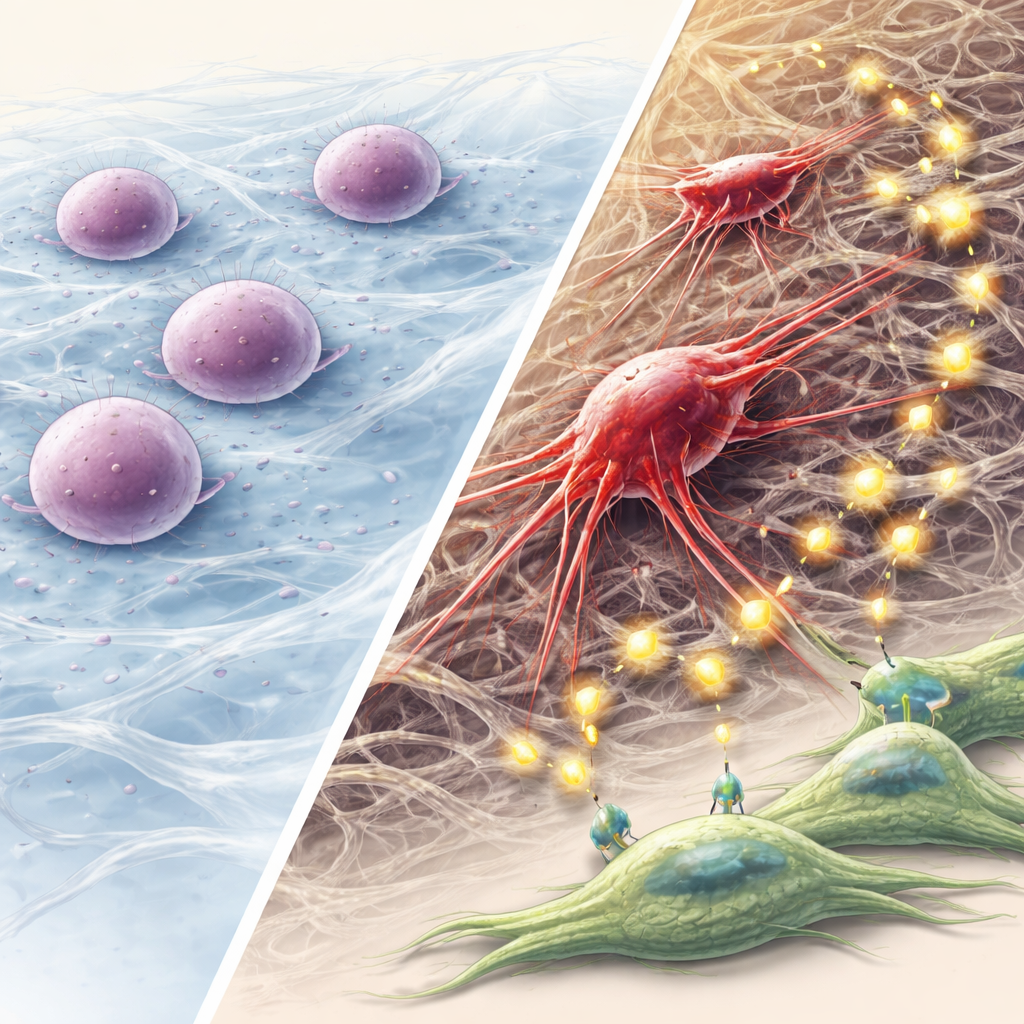
Dlaczego ta mechaniczna ścieżka do agresywnego nowotworu ma znaczenie
Praca proponuje model krok po kroku: fuzja keratyn zakłóca wewnętrzny ruszt komórki, miażdży jądro i wyzwala alarm uszkodzeń DNA; autofagia pozwala kilku komórkom wejść w uśpienie zamiast umrzeć; z czasem ci przeżywający reorganizują swój szkielet, zyskują cechy podobne do komórek macierzystych i inwazyjne oraz przekształcają otoczenie przez pęcherzyki i sygnalizację FGF. Dla odbiorcy niebędącego specjalistą kluczowe przesłanie jest takie, że siły fizyczne i białka strukturalne wewnątrz komórek mogą być równie ważne jak geny i związki chemiczne w napędzaniu ewolucji nowotworu. Celowanie w tę ścieżkę stresu mechanicznego–autofagii–FGF, szczególnie w rakach głowy i szyi z fuzjami keratyn, może dać nowe strategie zapobiegania ponownemu wybudzeniu uśpionych komórek nowotworowych i ich rozsiewowi.
Cytowanie: Chen, IH., Ravichandran, S., Lai, MT. et al. Cytoskeleton reorganization induced by a novel K6-K14 keratin fusion promotes cancer stemness and cellular plasticity via cGAS-STING selection. Oncogenesis 15, 5 (2026). https://doi.org/10.1038/s41389-026-00598-1
Słowa kluczowe: nowotworowa pędowość, cytoszkielet komórkowy, uśpienie guza, rak głowy i szyi, mechanotransdukcja