Clear Sky Science · pl
Rola demetylazy histonowej PHF2 jako supresora nowotworowego w raku wątrobowokomórkowym przez regulację SRXN1
Dlaczego to badanie nad rakiem wątroby ma znaczenie
Rak wątroby należy do najgroźniejszych nowotworów na świecie, a obecne leki wydłużają życie tylko w ograniczonym stopniu u wielu pacjentów. To badanie stawia pytanie inaczej: zamiast celować w powszechnie znane geny napędzające nowotwór, czy można wykorzystać sposób, w jaki DNA jest pakowane i chemicznie oznaczane w komórkach wątroby, by znaleźć nowe, precyzyjniejsze opcje leczenia? Badacze skupili się na mało znanym białku PHF2 i odkryli, w jaki sposób może ono pomagać zapobiegać przekształceniu komórek wątrobowych w nowotworowe.
Poszukiwanie słabości w systemie kontroli raka
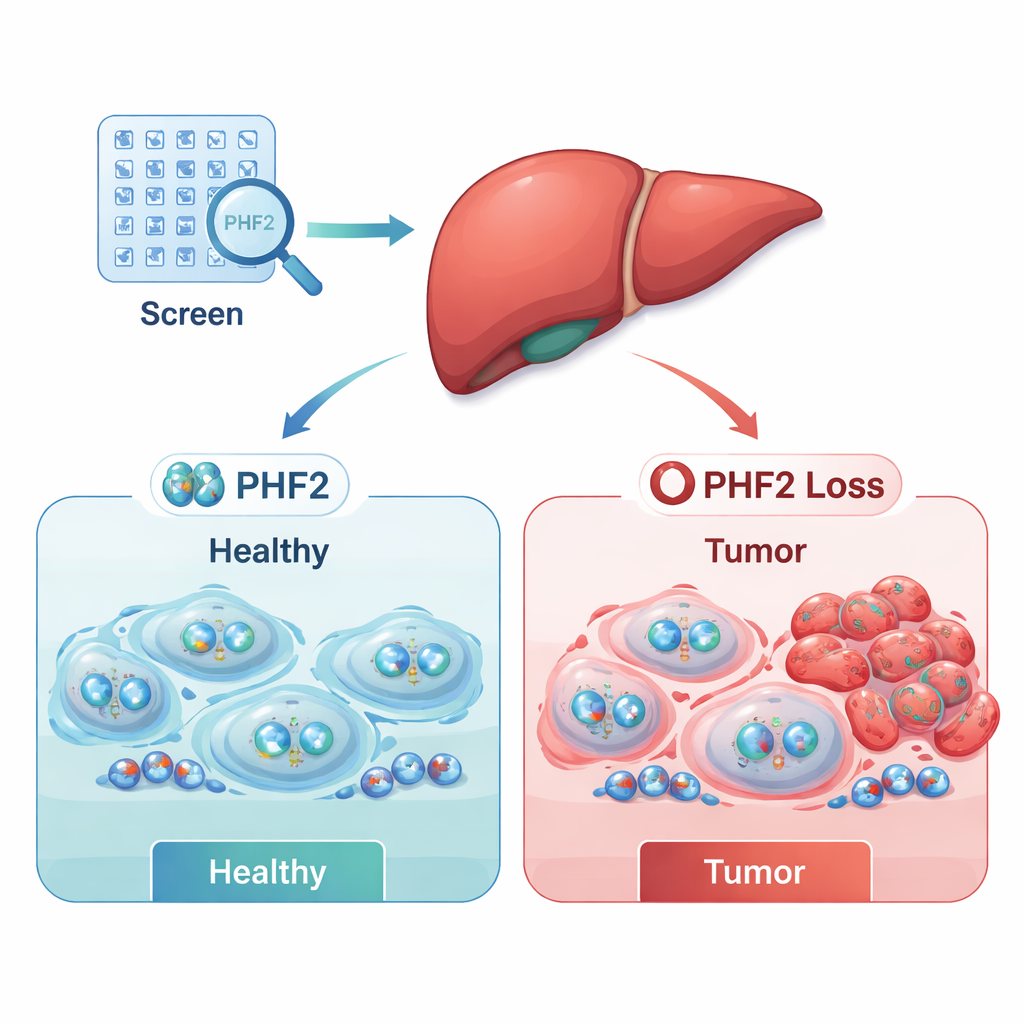
Nowotwór nie jest napędzany wyłącznie przez uszkodzone geny; rozwój choroby wspierają też zaburzenia „epigenetycznej” kontroli — chemiczne znaczniki i kompleksy białkowe, które decydują, które geny są włączone lub wyłączone. W raku wątrobowokomórkowym, najczęstszej postaci raka wątroby, wiele takich regulatorów jest zaburzonych. Zespół systematycznie przetestował 497 regulatorów epigenetycznych w sześciu liniach komórek raka wątroby, używając narzędzi RNA do tymczasowego obniżania aktywności każdego regulatora po kolei i mierząc, jak dobrze przeżywają komórki nowotworowe. Duże przesiewowe badanie miało ujawnić, na których regulatorach nowotwory polegają, by rosnąć, a które normalnie działają jak hamulec powstawania guza.
Odnalezienie nowych pomocników i obrońców raka
Przesiew ujawnił dwie szerokie grupy: potencjalne „przyspieszacze” raka (onkogeny), których utrata szkodziła przetrwaniu komórek nowotworowych, oraz potencjalne „hamulce” (supresory nowotworowe), których utrata sprzyjała wzrostowi komórek. Łącząc dane laboratoryjne z dużymi publicznymi zestawami danych pacjentów, badacze zawęzili listę do kilku klinicznie istotnych kandydatów. Dwaj regulatorzy, SUPT7L i SMARCC1, częściej były aktywne w guzach i wiązały się z gorszym przeżyciem. Natomiast regulator PHF2 był często mniej aktywny w nowotworach wątroby, a pacjenci, których guzy zachowywały wyższe poziomy PHF2, ogólnie żyli dłużej. Wzorce te sugerowały, że PHF2 może pełnić rolę supresora nowotworowego w raku wątroby u ludzi.
Jak utrata PHF2 zmienia komórki raka wątroby
Aby dokładniej przetestować PHF2, zespół zaprojektował komórki raka wątroby, które trwale wytwarzają mniej tego białka, i obserwował ich zachowanie w czasie. Komórki z obniżonym poziomem PHF2 rosły szybciej i wykazywały wyższe poziomy Ki-67, markera aktywnego podziału komórkowego, co wskazuje, że PHF2 normalnie pomaga hamować proliferację. Efekty te były najsilniejsze w już agresywnych liniach komórek raka wątroby, co sugeruje, że sama utrata PHF2 może nie zapoczątkować raka, ale może przyspieszyć wzrost komórek złośliwych, gdy guzy już się rozwiną.
Zaskakujące powiązanie z mechanizmami obrony przed stresem komórkowym
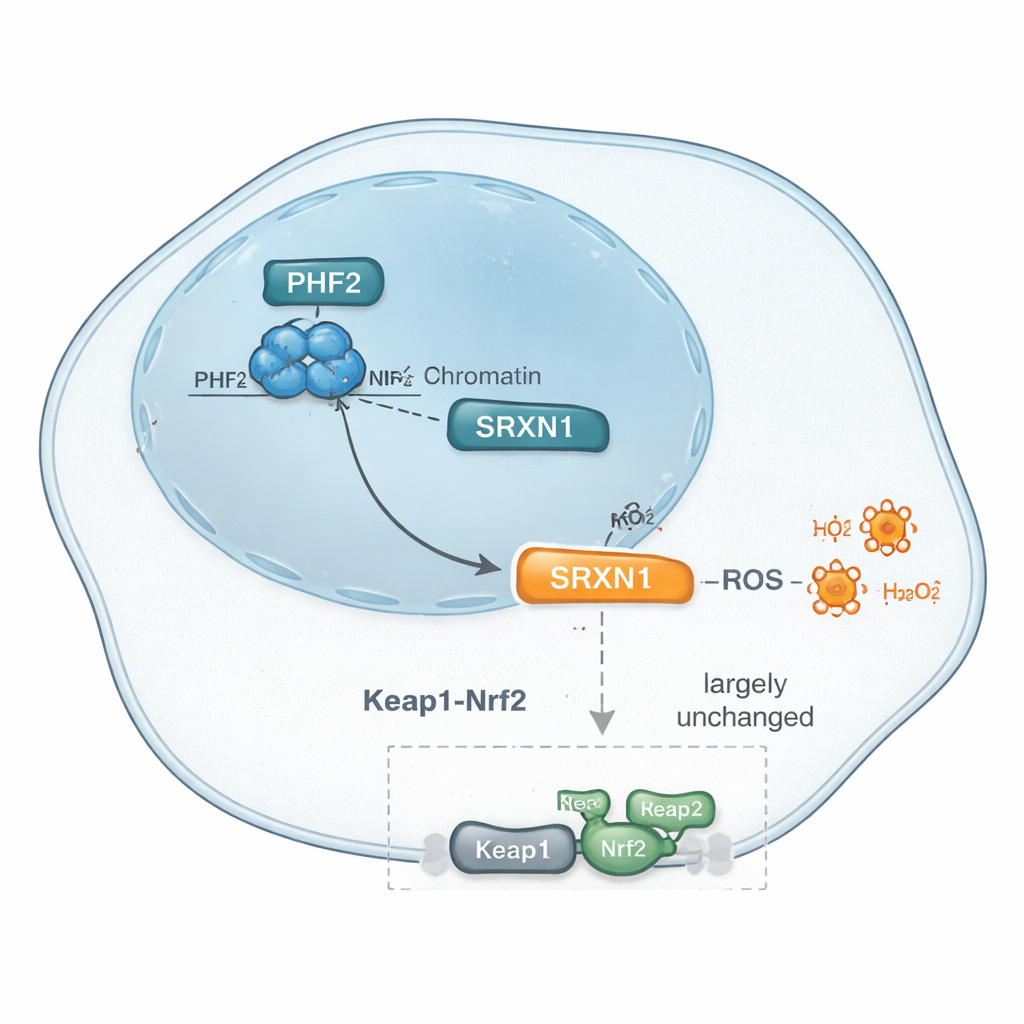
Następnie badacze użyli nowoczesnych metod profilowania białek, aby skatalogować tysiące białek, których poziomy zmieniały się po obniżeniu PHF2. Wśród wielu subtelnych zmian wyróżnił się jeden wzorzec: poziomy białka chroniącego przed stresem, SRXN1, konsekwentnie spadały przy utracie PHF2. SRXN1 pomaga komórkom radzić sobie z reaktywnymi formami tlenu — chemicznymi produktami ubocznymi, które mogą uszkadzać DNA i białka, ale też zmuszać komórki nowotworowe do adaptacji. Dane sugerowały, że PHF2 pomaga utrzymać poziomy SRXN1, a zmiana tej równowagi może wpływać na to, jak komórki raka wątroby reagują na wewnętrzny stres i w konsekwencji, jak szybko się dzielą.
Działanie poza znaną ścieżką stresową
SRXN1 zwykle kontrolowany jest przez główny przełącznik odpowiedzi na stres, Nrf2, który włącza wiele genów antyoksydacyjnych w obliczu stresu oksydacyjnego. Ponieważ SRXN1 spadał przy supresji PHF2, zespół zapytał, czy PHF2 nie działa po prostu przez tę znaną ścieżkę Nrf2. Przeanalizowali kluczowe geny i białka związane z Nrf2, potraktowali komórki lekami aktywującymi Nrf2 przez blokowanie jego inhibitora Keap1 i użyli narzędzi genetycznych do bezpośredniego obniżenia Keap1. W tych testach odpowiedź komórek pozbawionych PHF2 przypominała odpowiedź komórek normalnych, a szersze analizy ścieżek i czynników transkrypcyjnych nie wskazały Nrf2 jako głównego gracza. Zamiast tego pojawiły się inne czynniki, w tym ZNF384 i Nrf1 — oba wcześniej powiązane z rakiem wątroby. Razem dowody sugerują, że kontrola SRXN1 i odpowiedzi antyoksydacyjnej przez PHF2 może omijać klasyczne sygnalizowanie Nrf2, wskazując na odrębną drogę regulacji stresu w tych guzach.
Co to może oznaczać dla przyszłych terapii
Dla osoby nienależącej do specjalistów kluczowy wniosek jest taki, że to badanie identyfikuje PHF2 jako obiecujący czynnik ochronny w raku wątroby: gdy PHF2 jest obecny i aktywny, komórki nowotworowe rosną wolniej; gdy jest osłabiony, zyskują przewagę wzrostu i zmienia się ich sposób radzenia sobie ze stresem komórkowym. Ponieważ sam PHF2 może być trudny do bezpośredniego zahamowania lub pobudzenia konwencjonalnymi małocząsteczkowymi lekami, autorzy wskazują na rozwijające się strategie, takie jak terapie oparte na RNA lub leki zwiększające aktywność PHF2 poprzez partnerów sygnalizacyjnych działających powyżej niego. Podkreślają też, że efekty PHF2 zależą od kontekstu — jego wpływ może się różnić w zależności od innych mutacji, jak status p53 — więc ewentualne przyszłe terapie prawdopodobnie wymagałyby starannej selekcji pacjentów. Ogólnie praca doprecyzowuje naszą wiedzę o tym, jak regulatory epigenetyczne kształtują zachowanie raka wątroby i otwiera nowe drogi do projektowania terapii, które przywracają lub naśladują supresyjne działanie PHF2.
Cytowanie: Thng, D.K.H., Hooi, L., Yong, W.K. et al. The role of histone demethylase PHF2 as a tumour suppressor in hepatocellular carcinoma by regulating SRXN1. Oncogenesis 15, 6 (2026). https://doi.org/10.1038/s41389-026-00597-2
Słowa kluczowe: rak wątrobowokomórkowy, regulacja epigenetyczna, PHF2, SRXN1, terapia raka wątroby