Clear Sky Science · pl
Wydzielanie OPN zależne od Rab37 wzbogaca makrofagi SPP1+ poprzez sygnalizację autokrynowo–parakrynową, napędzając progresję nowotworu płuca
Jak komórki układu odpornościowego mogą potajemnie pomagać wzrostowi nowotworów płuca
Rak płuca nie rozwija się w izolacji. Rośnie w tętniącym życiem sąsiedztwie komórek odpornościowych i tkanki łącznej, które niekiedy zamieniają się z obrońców w sojuszników. To badanie pokazuje, jak niewielkie białko transportowe wewnątrz komórek odpornościowych, zwane Rab37, pomaga pewnym makrofagom wydzielać cząsteczkę zwaną osteopontyną (OPN), tworząc sprzyjające rakowi środowisko, które sprawia, że rak płuca staje się bardziej agresywny i trudniejszy do leczenia.
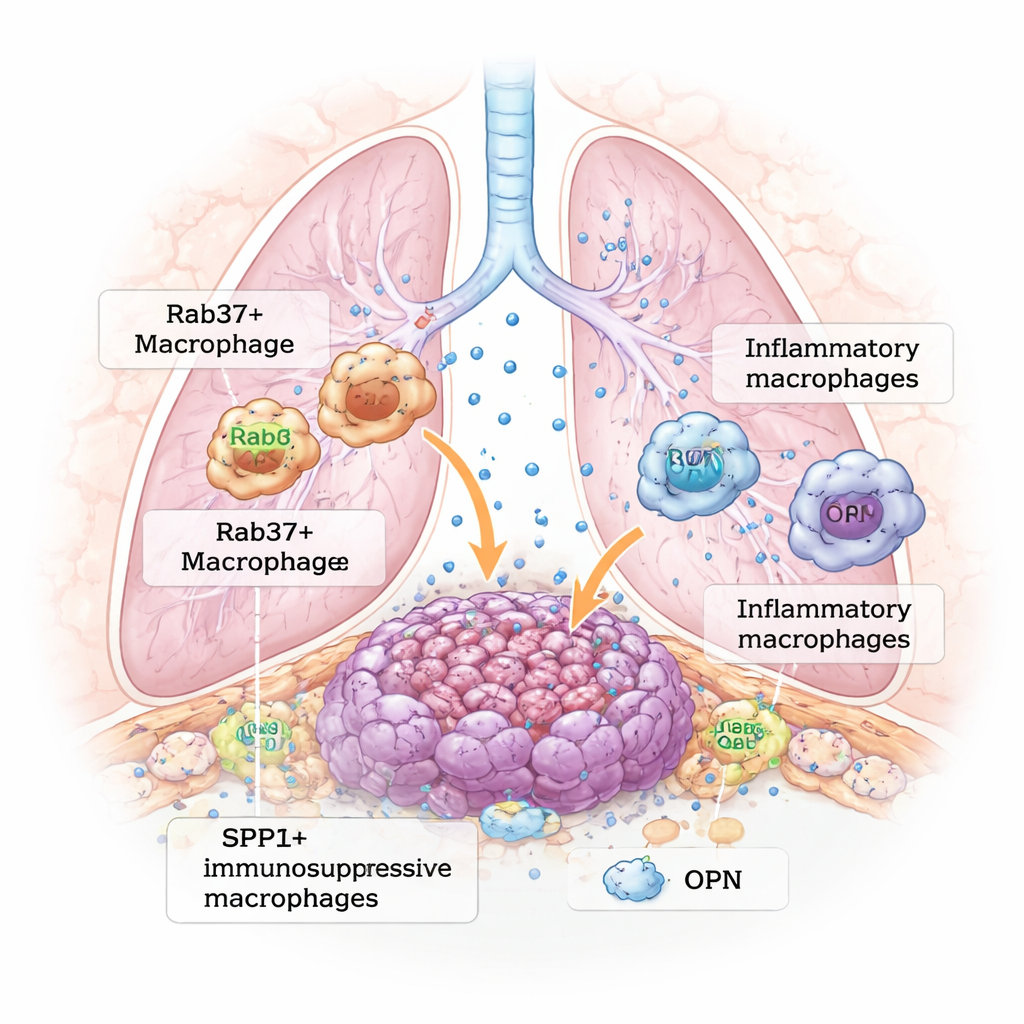
Gwarne sąsiedztwo wewnątrz guza płuca
Współczesne badania nad rakiem pokazują, że guzy przypominają bardziej złożone ekosystemy niż proste zbitki zbuntowanych komórek. Wokół guzów płuca komórki odpornościowe, naczynia krwionośne i komórki podporowe nieustannie wymieniają się sygnałami chemicznymi. Wśród nich makrofagi — komórki odpornościowe, które normalnie usuwają infekcje i szczątki — często osiedlają się w guzach jako „makrofagi związane z guzem”. Zamiast atakować nowotwór, wiele z tych komórek przechodzi w rolę opiekuńczą, łagodząc ataki układu odpornościowego i wspierając wzrost oraz rozsiew nowotworu. Główne pytanie, które porusza artykuł, brzmi: co popycha makrofagi do tego szkodliwego, sprzyjającego guzowi stanu?
Dwa typy makrofagów: pomagający i hamujący
Naukowcy zastosowali pojedynczokomórkowe sekwencjonowanie RNA, technologię odczytującą aktywność tysięcy genów w poszczególnych komórkach, aby zmapować komórki odpornościowe wewnątrz mysich guzów płuca. Porównali myszy normalne z myszami pozbawionymi Rab37. W guzach myszy kontrolnych znaleziono wiele makrofagów bogatych w gen SPP1, który koduje białko osteopontynę (OPN). Te makrofagi SPP1+ tworzyły immunosupresyjny, wspierający guz populację. Natomiast guzy u myszy z wyciszonym Rab37 miały mniej makrofagów SPP1+ i więcej makrofagów exprimujących inny gen, THBS1, powiązany z bardziej zapalną, potencjalnie hamującą guz odpowiedzią. W próbkach ludzkiego raka płuca pacjenci, których guzy zawierały dużo makrofagów pozytywnych dla CD163, Rab37 i OPN, częściej doświadczali nawrotów i mieli gorsze przeżycie, co sugeruje, że ten konkretny typ makrofagów ma znaczenie kliniczne.
Białko przewożące sekrety, które wzmacnia OPN
Rab37 należy do rodziny białek kontrolujących pakowanie i uwalnianie cząsteczek przez komórki. Zespół wykazał, że Rab37 ładuje OPN do małych pęcherzyków wewnątrz makrofagów i napędza jej uwalnianie na zewnątrz. Gdy makrofagi miały czynny Rab37, wydzielały dużo więcej OPN, szczególnie po wystawieniu na sygnały z komórek raka płuca. Po usunięciu Rab37 lub zablokowaniu jego aktywności, uwalnianie OPN gwałtownie malało. Badanie ujawniło też pętlę sprzężenia zwrotnego: uwolniona OPN aktywuje białko sygnałowe STAT3 w makrofagach, co z kolei zwiększa aktywność genu SPP1 i przesuwa makrofagi w stronę fenotypu podobnego do M2, sprzyjającego guzowi. Ta pętla utrzymuje komórki w prozapalnej, proguzinnej tożsamości, nieustannie wytwarzając więcej OPN.
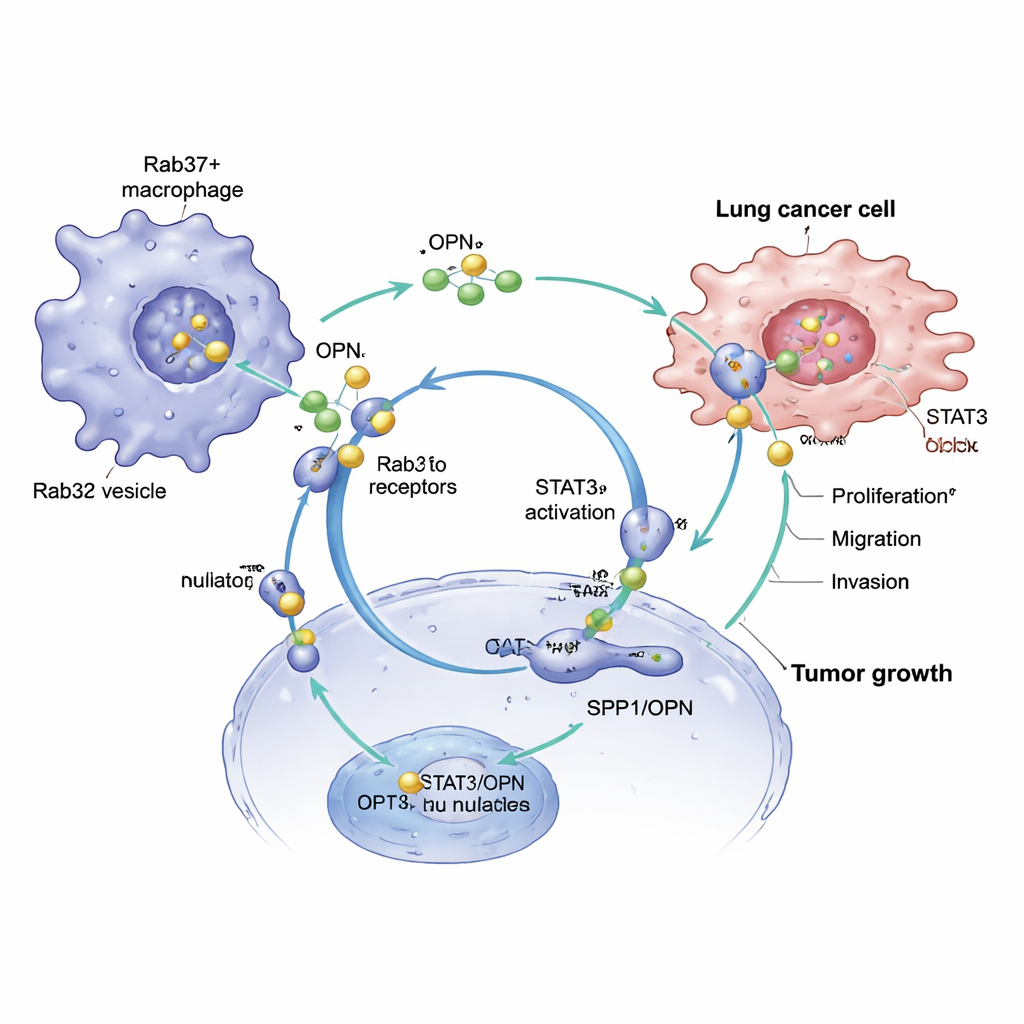
Od sygnałów immunologicznych do szybszego wzrostu guza
OPN działa nie tylko na makrofagi — komunikuje się także bezpośrednio z komórkami nowotworowymi. Gdy komórki raka płuca były eksponowane na płyn pobrany od makrofagów z aktywnym Rab37, rosły szybciej i stawały się bardziej ruchliwe oraz inwazyjne. Zablokowanie OPN w tym płynie osłabiało te efekty, natomiast dodanie oczyszczonej OPN przywracało je. Ta sama pętla Rab37–OPN–STAT3, która przeprogramowuje makrofagi, aktywuje też szlaki wzrostu i przeżycia w komórkach raka płuca, sprzyjając proliferacji, migracji i inwazji do otaczających tkanek. W ten sposób jedna wydzielona cząsteczka jednocześnie przekształca zachowanie układu odpornościowego i przyspiesza progresję guza.
Jak przekształcić odkrycie w możliwość terapeutyczną
Dla osób niebędących specjalistami główne przesłanie jest takie, że niektóre komórki odpornościowe w guzach płuca stają się „podwójnymi agentami”, a Rab37 jest kluczowym koordynatorem ich zdrady. Poprzez wspieranie wydzielania OPN przez makrofagi i utrzymywanie pętli sprzężenia zwrotnego napędzanej przez OPN, Rab37 tworzy stonowane, tolerancyjne środowisko, w którym guzy mogą rozwijać się i dawać przerzuty. Pacjenci, których guzy są pełne makrofagów Rab37+/OPN+, mają gorsze rokowanie, co oznacza, że ten typ komórek może służyć jako wskaźnik ostrzegawczy i cel terapeutyczny. Terapie blokujące OPN, zakłócające STAT3 lub ingerujące w funkcję transportową Rab37 mogą pomóc przywrócić makrofagom rolę przeciwnowotworową, czyniąc raka płuca bardziej podatnym na istniejące terapie, w tym immunoterapię.
Cytowanie: Yang, YE., Lin, YA., Ling, LL. et al. Rab37-mediated OPN secretion enriches SPP1+ macrophages through autocrine–paracrine signaling to drive lung tumor progression. Oncogenesis 15, 4 (2026). https://doi.org/10.1038/s41389-026-00596-3
Słowa kluczowe: rak płuca, mikrośrodowisko guza, makrofagi, osteopontyna, sygnalizacja STAT3