Clear Sky Science · pl
Degradacja HILPDA zależna od TRIM21 przezwycięża oporność na immunoterapię przeciw PD-1 w raku piersi, ograniczając palmitoilację PD-L1
Dlaczego niektóre immunoterapie przeciwnowotworowe przestają działać
Leki uwalniające układ odpornościowy, takie jak terapie anty–PD‑1, zrewolucjonizowały leczenie kilku rodzajów nowotworów, w tym agresywnych postaci raka piersi. Jednak wiele guzów albo w ogóle nie reaguje, albo z czasem znajduje sposoby ucieczki. Badanie to rozkłada na czynniki jeden z takich mechanizmów ucieczki w raku piersi potrójnie ujemnym i pokazuje, jak przebudowa metabolizmu lipidów w guzie — oraz ponowne użycie leku o nazwie fenretinid — może ponownie otworzyć drogę dla układu odpornościowego, gdy standardowa immunoterapia zawodzi. 
Ukryty sprzymierzeniec chroniący guzy
Naukowcy skupili się na mało znanym białku HILPDA, wcześniej powiązanym z mechanizmami gospodarowania tłuszczami przez komórki w warunkach stresu. Porównując mysie guzy piersi, które pozostały wrażliwe na terapię anty‑PD‑1, z guzami, które stały się oporne, odkryli, że poziomy HILPDA były znacznie wyższe w nowotworach opornych. Analizy dużych baz danych pacjentów oraz próbek guzów od kobiet z rakiem piersi potwierdziły, że HILPDA występuje częściej w guzach niż w prawidłowej tkance piersiowej, szczególnie w chorobie potrójnie ujemnej, i że pacjentki, których guzy wykazują wyższą ekspresję HILPDA, mają zwykle gorsze rokowanie. Guzy od osób, które nie odniosły korzyści z leków blokujących PD‑1, także miały więcej HILPDA, co łączy to białko bezpośrednio z niepowodzeniem terapii.
Jak guzy przekręcają krajobraz odporności przeciwko nam
Aby ustalić, co HILPDA faktycznie robi wewnątrz guzów, zespół zmodyfikował komórki raka piersi tak, by produkowały białko w nadmiarze lub go nie miały, a następnie hodował je z ludźmi komórkami odpornościowymi lub w myszach. Gdy HILPDA było wysokie, guzy przyciągały więcej limfocytów T regulatorowych, komórek supresorowych pochodzenia mieloidalnego oraz makrofagów typu M2 — typów komórek odpornościowych, które tłumią atak i pomagają nowotworom się ukryć. Jednocześnie liczba i aktywność cytotoksycznych limfocytów CD8 oraz komórek NK spadała, a ich zdolność do uwalniania toksycznych cząsteczek i sygnałów zapalnych była osłabiona. Wyciszenie HILPDA odwracało ten scenariusz: guzy miały mniej komórek supresyjnych, więcej aktywnych komórek zabójczych, wolniejszy wzrost i mniej przerzutów. Co istotne, gdy zwierzęta z guzami o niskim HILPDA otrzymały terapię anty‑PD‑1, ich guzy kurczyły się bardziej, a myszy żyły dłużej, pokazując, że HILPDA kontroluje skuteczność immunoterapii.
Produkcja tłuszczu, molekularna zbroja i ucieczka przed odpornością
Pogłębiając badania, naukowcy odkryli, jak HILPDA przebudowuje metabolizm guza, by utwardzić jego obronę immunologiczną. W komórkach nowotworowych HILPDA wiąże się z białkiem opiekuńczym HSP90, stabilizując czynnik transkrypcyjny KLF5, który napędza syntezę lipidów. To trio zwiększa wytwarzanie kwasów tłuszczowych, zwłaszcza palmitynianu, i napełnia komórki guza kroplami lipidowymi. Jeden z tych tłuszczów jest następnie dołączany do PD‑L1 — białka punktu kontrolnego na powierzchni guza, które wysyła komórkom odpornościowym sygnał „nie atakuj”. Zespół wykazał, że przyłączenie palmitynianu do określonego miejsca w PD‑L1 działa jak molekularny klej: pomaga PD‑L1 stabilnie osadzić się w błonie komórkowej i zapobiega jego rozkładowi. Zmutowanie tego jednego miejsca przyłączenia pozbawia PD‑L1 stabilności i osłabia jego zdolność osłaniania komórek nowotworowych, nawet gdy HILPDA jest obfite. Innymi słowy, produkcja tłuszczu napędzana przez HILPDA dostarcza chemicznej modyfikacji PD‑L1, która zmienia tarczę immunologiczną guza z kruchą w wzmocnioną stal.
Wbudowany hamulec, który można uruchomić
Każde przyspieszenie potrzebuje hamulca — tutaj rolę hamulca pełni inne białko o nazwie TRIM21. Autorzy odkryli, że TRIM21 rozpoznaje HILPDA i znakuję je „flagami” przekierowującymi do komórkowego systemu utylizacji. W guzach piersi u pacjentów poziomy TRIM21 zwykle były niskie, gdy HILPDA było wysokie, a niski TRIM21 wiązał się z gorszymi wynikami, co sugeruje, że ten naturalny system hamowania jest często osłabiony w nowotworach. Zespół poszukał następnie leków, które mogłyby wzmocnić TRIM21 i zidentyfikował fenretinid — retinoid już badany u ludzi. W modelach komórkowych i zwierzęcych raka piersi potrójnie ujemnego fenretinid zwiększał aktywność TRIM21, przyspieszał rozkład HILPDA, redukował syntezę lipidów i ochronną modyfikację PD‑L1 oraz spowalniał wzrost i rozprzestrzenianie się guza. Najbardziej uderzające było to, że połączenie fenretinidu z terapią anty‑PD‑1 uczyniło guzy bardziej podatnymi na atak immunologiczny, zwiększając liczbę limfocytów zabójczych i komórek NK oraz zmniejszając liczbę komórek supresyjnych w mikrośrodowisku guza. 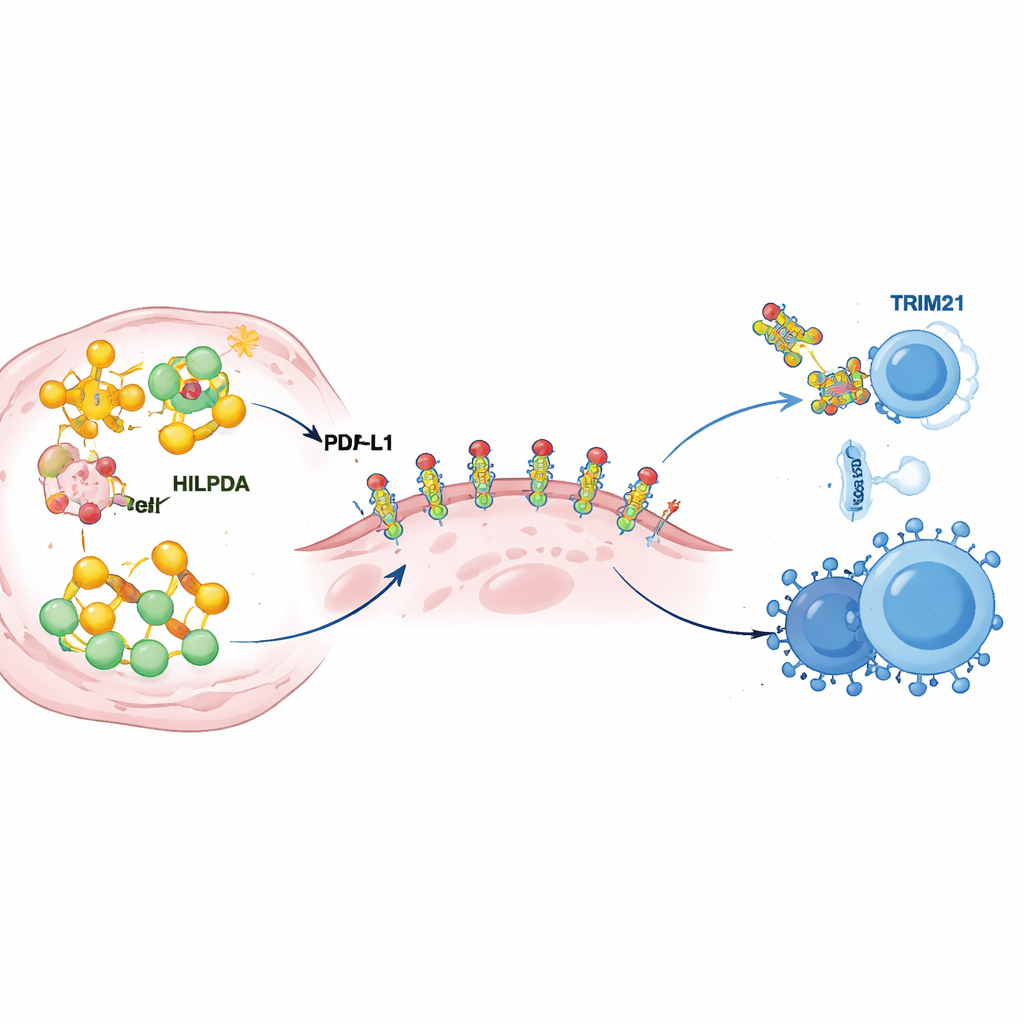
Co to oznacza dla przyszłej opieki onkologicznej
Praca ta ujawnia łańcuch zdarzeń, w którym zestresowane komórki raka piersi zwiększają HILPDA, przyspieszają syntezę tłuszczów i chemicznie wzmacniają PD‑L1 na swojej powierzchni, co pozwala im dalej tłumić komórki odpornościowe nawet w obliczu leków blokujących PD‑1. TRIM21 działa jako wewnętrzne zabezpieczenie, które może rozmontować HILPDA, ale w guzach często jest zbyt słabe. Odkrycie, że fenretinid potrafi reaktywować ten mechanizm ochronny, wskazuje praktyczną strategię łączenia leku metabolicznego z istniejącą immunoterapią, aby przezwyciężyć oporność. Jeśli wyniki potwierdzą się w badaniach klinicznych, celowanie w oś TRIM21–HILPDA–PD‑L1 mogłoby dać pacjentom z trudno leczalnym rakiem piersi potrójnie ujemnym drugą szansę na korzyść z terapii opartych na układzie odpornościowym.
Cytowanie: Wang, X., Li, G., Wu, J. et al. TRIM21-mediated degradation of HILPDA overcomes anti-PD-1 immunotherapy resistance in breast cancer by limiting PD-L1 palmitoylation. Oncogene 45, 1338–1356 (2026). https://doi.org/10.1038/s41388-026-03728-6
Słowa kluczowe: rak piersi potrójnie ujemny, oporność na immunoterapię, palmitoilacja PD-L1, metabolizm lipidów w guzie, fenretinid