Clear Sky Science · pl
Cereblon (CRBN) hamuje przerzuty raka prostaty poprzez negatywną regulację 6‑fosfoglukonianowej dehydrogenazy (6PGD)
Dlaczego to badanie ma znaczenie
Kiedy rak prostaty rozprzestrzenia się z prostaty do innych narządów, staje się znacznie trudniejszy do leczenia i często śmiertelny. To badanie ujawnia, jak mało znany białkowy „system kontroli jakości”, cereblon (CRBN), pomaga powstrzymać rozsiew raka prostaty, rozkładając enzym metaboliczny napędzający agresywne zachowanie. Zrozumienie tego wbudowanego hamulca sugeruje nowe sposoby spowolnienia lub zatrzymania przerzutów, zwłaszcza w trudno leczonych postaciach choroby.
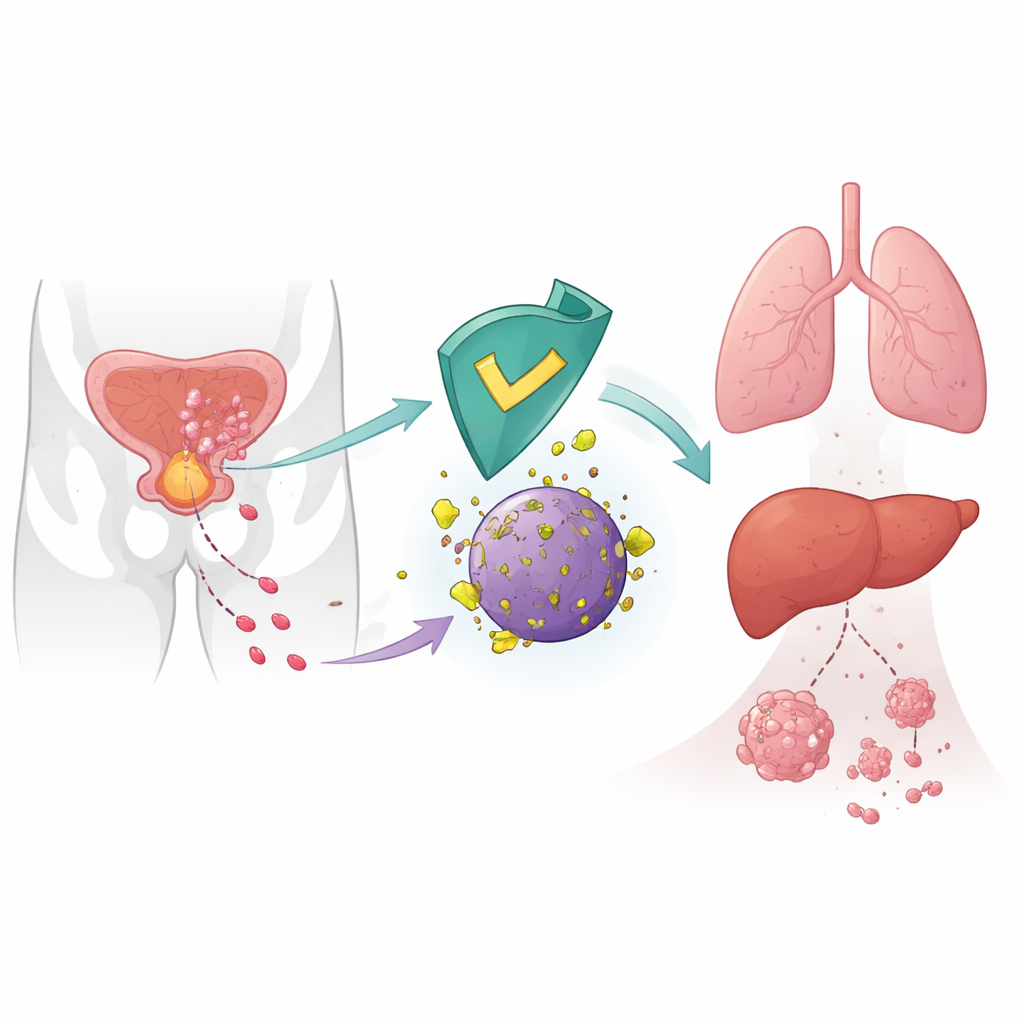
Wewnętrzny hamulec rozprzestrzeniania się raka
Komórki nowotworowe nie rozprzestrzeniają się losowo; przebudowują swoje wewnętrzne mechanizmy, by się poruszać, napadać i kolonizować odległe narządy. Autorzy skupili się na CRBN, białku najlepiej znanym jako cel leków takich jak talidomid używanych w nowotworach krwi. W zdrowych komórkach CRBN jest częścią molekularnej jednostki utylizacyjnej, która oznacza określone białka do zniszczenia. Wcześniejsze badania sugerowały, że niskie poziomy CRBN w guzach wiązały się ze gorszymi wynikami, lecz jego bezpośrednia rola w przerzutach była niejasna. Tu badacze wykazują, że CRBN działa jako naturalny supresor rozsiewu raka prostaty, kierując enzym metaboliczny 6‑fosfoglukonianową dehydrogenazę (6PGD) na rozkład.
Silnik metaboliczny, który przejmuje rak
6PGD uczestniczy w szlaku metabolicznym znanym jako utleniający szlak pentozofosforanowy, który pomaga komórkom wytwarzać NADPH — cząsteczkę dostarczającą zarówno materiałów budulcowych, jak i siły antyoksydacyjnej. Wiele guzów nasila ten szlak, by rosnąć szybciej i znosić stres. Zespół stwierdził, że próbki raka prostaty od pacjentów mają zwykle mniej CRBN i więcej 6PGD niż normalna tkanka prostaty, a ta nierównowaga jest szczególnie wyraźna w chorobie agresywnej. W liniach komórkowych raka prostaty obniżenie poziomu CRBN lub jego degradacja za pomocą zaprojektowanego związku powodowały wzrost poziomu białka 6PGD i aktywności enzymu, zwiększając NADPH. Przywrócenie CRBN miało odwrotny skutek — obniżało 6PGD i NADPH bez zmiany przekazu genu 6PGD, co wskazuje na kontrolę na poziomie białka.
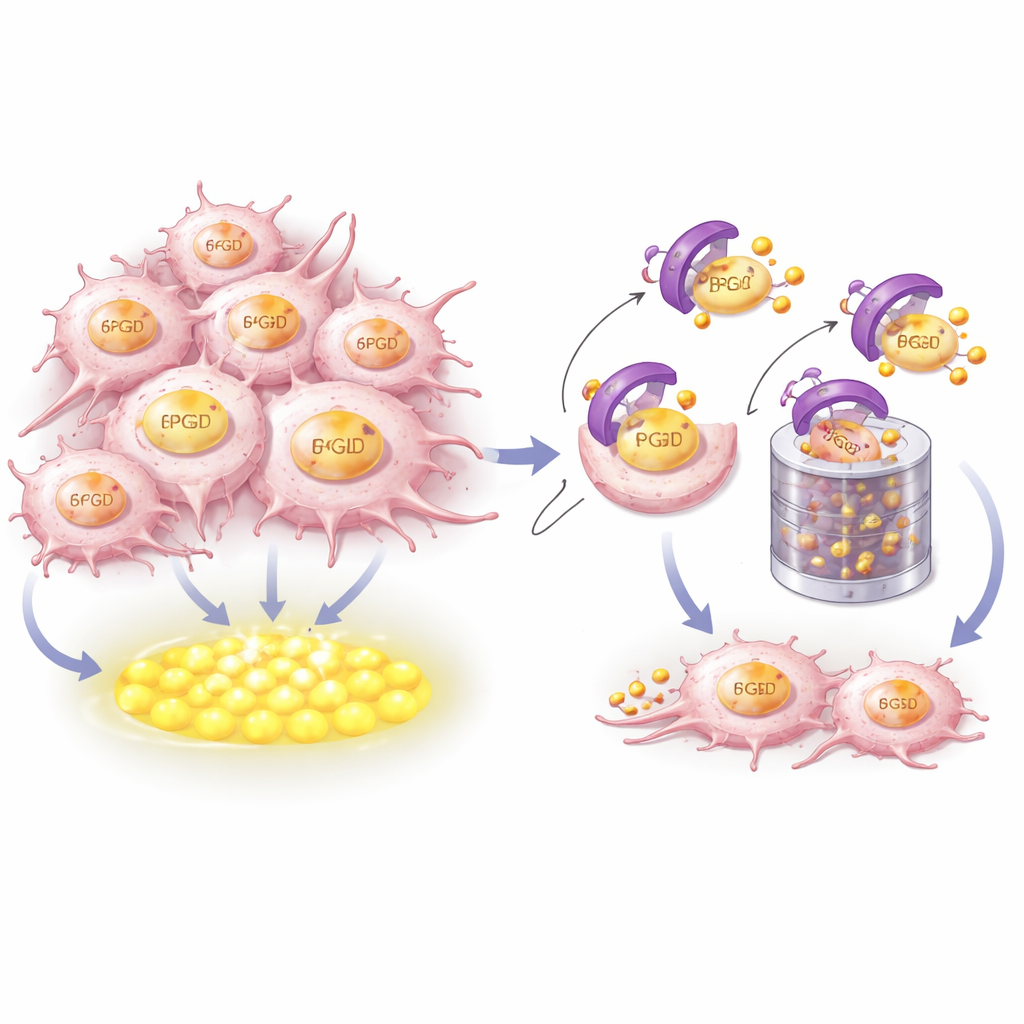
Jak CRBN rozpoznaje i niszczy źródło paliwa
Aby zrozumieć, jak CRBN kontroluje 6PGD, badacze połączyli modelowanie strukturalne z eksperymentami biochemicznymi. Pokaźne, że CRBN fizycznie chwyta krótką, silnie zachowaną helikalną sekwencję blisko końca ogonowego 6PGD. Kluczowe aminokwasy po obu białkach tworzą dopasowany interfejs dokujący. Gdy te punkty kontaktu zostały zmienione, CRBN nie mogło już wiązać 6PGD, przyłączać małych znaczników ubikwityny sygnalizujących degradację ani kierować go do komórkowego niszczyciela, proteasomu. Co ważne, powierzchnia rozpoznawcza jest odrębna od kieszeni, w którą wiążą się leki modulujące układ odpornościowy, co oznacza, że kontrola 6PGD przez CRBN jest elementem jego natywnej funkcji porządkowej, a nie efektem działania leków.
Od zmienionego metabolizmu do wędrujących komórek
Konsekwencje tego molekularnego uścisku odzwierciedlają się w zachowaniu komórek. W komórkach raka prostaty pozbawionych CRBN podwyższony 6PGD i NADPH szły w parze ze zwiększoną ruchliwością i inwazją przez sztuczne bariery — cechami potencjału przerzutowego. Gdy CRBN było nadmiernie produkowane, komórki stawały się mniej ruchliwe i inwazyjne, mimo że tempo ich wzrostu nie ulegało zmianie. Profilowanie aktywności genów pokazało, że CRBN zwiększa poziomy CDH1, związane ze ściśle upakowanymi komórkami nabłonkowymi, i obniża poziomy MMP1, powiązanego z degradacją tkanek i migracją. Co istotne, te zmiany wymagały bezpośredniego wiązania CRBN–6PGD i mogły zostać odwrócone przez zablokowanie aktywności enzymatycznej 6PGD, łącząc zmiany metabolizmu ze zmianami w zachowaniach przerzutowych.
Dane z modeli zwierzęcych i innych nowotworów
Zespół przetestował te hipotezy na myszach, wstrzykując komórki raka prostaty do krwiobiegu lub śledziony. Komórki genetycznie zmodyfikowane tak, by produkowały dodatkowe CRBN, tworzyły znacznie mniej ognisk przerzutowych w wątrobie i płucach niż komórki kontrolne, potwierdzając antyprzerzutową rolę in vivo. Myszy pozbawione CRBN wykazywały wyższe poziomy białka 6PGD w kilku narządach. Podobne wzorce zaobserwowano w liniach komórkowych glejaka, raka płuca i nerki: usunięcie CRBN zwiększało 6PGD i nasilało ruchliwość oraz inwazję komórek, podczas gdy genetyczne lub farmakologiczne zahamowanie 6PGD ograniczało to agresywne zachowanie. Te obserwacje sugerują, że hamulec CRBN–6PGD na przerzuty nie jest unikatowy dla raka prostaty.
Co to może znaczyć dla przyszłych terapii
Podsumowując, badanie proponuje, że CRBN pełni rolę metabolicznego strażnika, który powstrzymuje dopływ energii potrzebnej komórkom nowotworowym do rozluźnienia, migracji i wysiewania nowych guzów. Gdy CRBN jest utracone lub niskie, 6PGD się gromadzi, produkcja NADPH rośnie, a komórki częściej przechodzą przemiany sprzyjające przerzutom. Dla pacjentów otwiera to dwie możliwości: pomiar poziomów CRBN i 6PGD może pomóc wykrywać guzy o wysokim ryzyku przerzutów, a terapie zwiększające funkcję CRBN — lub selektywne tłumienie 6PGD w guzach ubogich w CRBN — mogą oferować nowe sposoby spowalniania lub zapobiegania rozsiewowi raka prostaty i innych nowotworów.
Cytowanie: Guchhait, K., Yoon, HS., An, HS. et al. Cereblon (CRBN) inhibits prostate cancer metastasis by negatively regulating 6-phosphogluconate dehydrogenase (6PGD). Oncogene 45, 1234–1246 (2026). https://doi.org/10.1038/s41388-026-03717-9
Słowa kluczowe: przerzuty raka prostaty, metabolizm nowotworów, cereblon, enzym 6PGD, szlak NADPH