Clear Sky Science · pl
L1TD1 sprzyja progresji śluzowatego gruczolakoraka jelita grubego przez zwiększanie stabilności mRNA ABCC3
Dlaczego ten śluzowy nowotwór ma znaczenie
Rak jelita grubego jest jedną z głównych przyczyn zgonów z powodu nowotworów na świecie. W jego obrębie wyróżnia się podtyp zwany śluzowatym gruczolakorakiem, którego guzy wypełnione są gęstym śluzem stanowiącym ponad połowę masy guza. Ta śluzowa bariera może pomagać komórkom nowotworowym ukrywać się przed chemioterapią i obroną organizmu. W badaniu postawiono podstawowe, ale kluczowe pytanie: co kontroluje produkcję tego śluzu i czy można ją zahamować, by spowolnić nowotwór i poprawić skuteczność terapii?
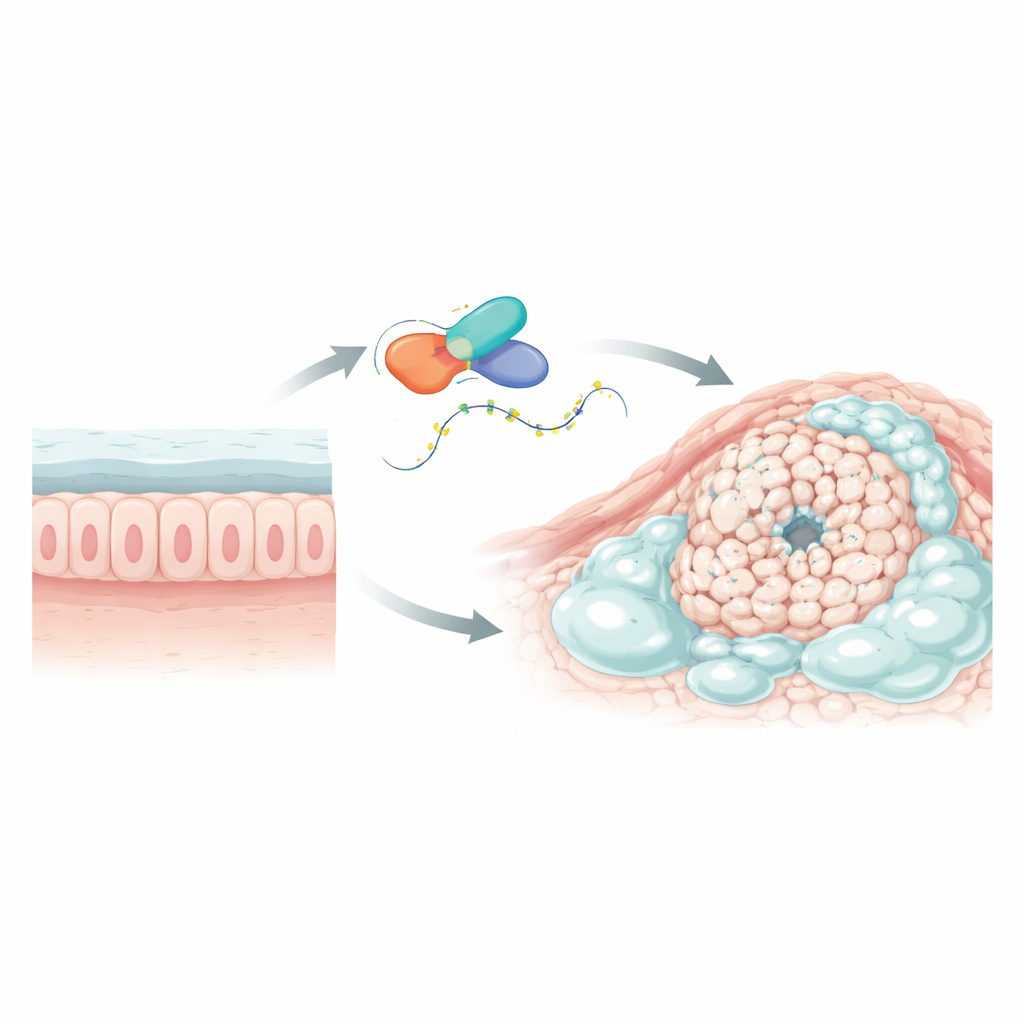
Wykrycie kluczowego „sprawcy” genowego
Naukowcy najpierw przeszukali duże bazy danych nowotworowych oraz dane z sekwencjonowania pojedynczych komórek, aby wskazać geny wykazujące odmienne zachowanie w guzach bogatych w śluz w porównaniu z typowymi rakami jelita grubego i okoliczną zdrową tkanką. Jeden gen, nazwany L1TD1, wyraźnie się wyróżniał. Był wyraźnie podwyższony w guzach śluzowatych, ale nie w zwykłych nowotworach, i miał wyższe poziomy w tkance guza niż w otaczającym zdrowym jelicie. L1TD1 koduje białko wiążące RNA, cząsteczkę przenoszącą informacje genetyczne z DNA do aparatu syntezy białek. Ponieważ białka wiążące RNA mogą precyzyjnie regulować czas życia komunikatów RNA i ich odczyt, L1TD1 był silnym kandydatem na tzw. regulatora mistrzowskiego w tych śluzowych nowotworach.
Jak L1TD1 napędza wzrost i rozsiew raka
Aby sprawdzić funkcję L1TD1, zespół przeprowadził eksperymenty na liniach komórkowych raka jelita grubego i modelach mysich. Gdy zwiększono poziomy L1TD1 w komórkach nowotworowych, komórki szybciej się dzieliły, poruszały sprawniej i agresywniej penetrowały bariery przypominające tkankę. Osłabienie ekspresji L1TD1 dawało efekt przeciwny — spowolnienie wzrostu i zmniejszenie inwazyjności. U myszy wstrzykniętych komórkami o wysokim poziomie L1TD1 guzy były większe i częściej dawały przerzuty do wątroby i jamy brzusznej. Guzy z wyższą ekspresją L1TD1 u pacjentów częściej były większe, mniej zróżnicowane i znajdowały się w bardziej zaawansowanych stadiach choroby, łącząc ten gen z gorszym przebiegiem klinicznym.
Włączanie produkcji śluzu i oporności na leki
Śluz okazał się kluczowy dla wpływu L1TD1. Komórki z wyższą ekspresją L1TD1 wytwarzały większe ilości głównych białek tworzących śluz, zwłaszcza MUC2 i MUC5AC, i wykazywały cechy komórek kubkowych, czyli fizjologicznych komórek wydzielających śluz w jelicie. Hodowle trójwymiarowe i barwienia tkanek od pacjentów i myszy potwierdziły, że wyższe L1TD1 idzie w parze z gęstszym i obfitszym śluzem. Co ważne, śluz nie był tylko biernym towarzyszem. Gdy badacze selektywnie zmniejszyli MUC2, dodatkowy wzrost, inwazja i oporność na chemioterapię napędzane przez L1TD1 w dużej mierze ustępowały. Komórki bogate w L1TD1 były trudniejsze do zniszczenia przy użyciu powszechnie stosowanego oksaliplatyny, a guzy zawierające takie komórki słabiej reagowały na leczenie u myszy, co podkreśla rolę śluzu jako tarczy, którą L1TD1 pomaga budować.
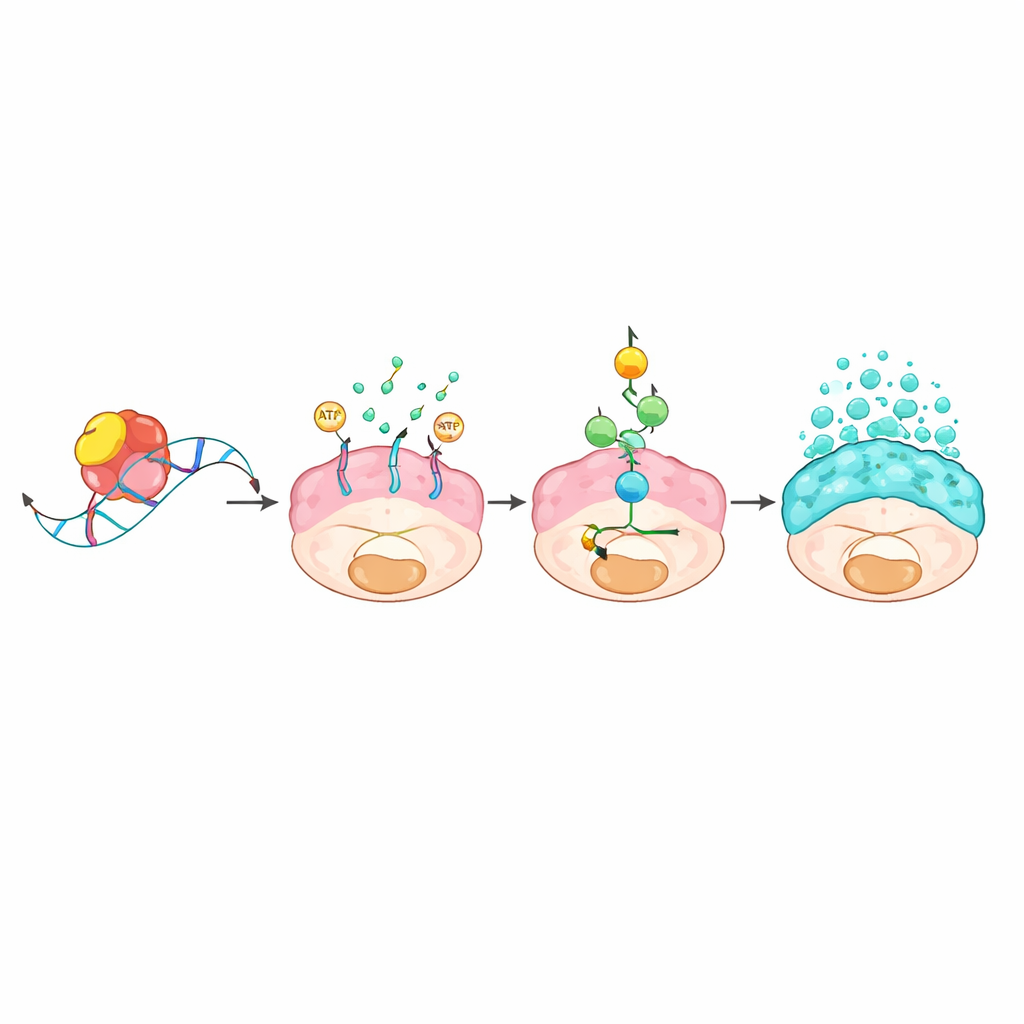
Molekularny łańcuch łączący kontrolę RNA z falą śluzu
Zespół następnie zapytał, jak białko wiążące RNA może wywołać tak dramatyczne zmiany. Poprzez wyizolowanie cząsteczek RNA fizycznie związanych z L1TD1 oraz porównanie aktywności genów z i bez L1TD1, zidentyfikowano gen transportera ABCC3 jako główny cel. L1TD1 przyłączał się do krótkiego motywu „GUGU” w końcu wiadomości RNA ABCC3, stabilizując ją, dzięki czemu komórka produkowała więcej białka ABCC3, znanego jako MRP3. Ten transporter osadzony w błonie komórkowej zużywa energię, wypompowując substancje z komórki. Powstały odpływ energii uruchamiał alarm metaboliczny z centrum w sensorze AMPK, który z kolei włączał klasyczną szlak wzrostu i stresu znany jako MAPK. Po aktywacji ta kaskada zwiększała produkcję i wydzielanie białek śluzowych oraz wzmacniała zdolność komórek nowotworowych do wzrostu, migracji i oporności na leki. Genetyczne zablokowanie ABCC3 lub zastosowanie eksperymentalnego związku przeciwko niemu, a także hamowanie szlaku MAPK, osłabiały produkcję śluzu i osłabiały guzy.
Co to znaczy dla pacjentów
Podsumowując, praca ujawnia stopniowy system kontroli dla śluzowatego raka jelita grubego: L1TD1 stabilizuje RNA ABCC3, ABCC3 odpompowuje energię komórkową, szlak AMPK–MAPK zostaje włączony, a guz reaguje nadprodukcją śluzu, stając się bardziej agresywny i odporny na leki. Dla pacjentów oznacza to kilka obiecujących kierunków. Poziomy L1TD1 i ABCC3 mogłyby pomóc zidentyfikować guzy o złym rokowaniu lub oporne na standardową chemioterapię. Co ważniejsze, leki przerywające interakcję L1TD1–ABCC3, blokujące aktywność pompy MRP3 lub celujące w dalsze ścieżki sygnałowe mogą przerzedzić barierę śluzową, spowolnić wzrost guza i zwiększyć skuteczność istniejących terapii wobec tej trudnej formy raka jelita grubego.
Cytowanie: He, H., Yuan, J., Wang, H. et al. L1TD1 promotes colorectal mucinous adenocarcinoma progression by enhancing ABCC3 mRNA stability. Oncogene 45, 1071–1086 (2026). https://doi.org/10.1038/s41388-026-03716-w
Słowa kluczowe: śluzowaty rak jelita grubego, L1TD1, ABCC3 MRP3, produkcja śluzu, oporność na chemioterapię