Clear Sky Science · pl
Wielofunkcyjna helikaza RNA DDX39A napędza postęp glejaka wielopostaciowego poprzez modulację alternatywnego składania WISP1, co indukuje immunosupresyjną polaryzację makrofagów
Dlaczego to badanie nad rakiem mózgu ma znaczenie
Glejaki wielopostaciowe należą do najgroźniejszych nowotworów mózgu, słyną z nawrotów po leczeniu i oporności na leki. To badanie ujawnia, jak jeden molekularny „przełącznik” w komórkach nowotworowych nie tylko sprzyja wzrostowi guza, ale także przekonuje pobliskie komórki układu odpornościowego, by zrezygnowały z walki i zaczęły chronić nowotwór. Śledząc ten łańcuch zdarzeń, autorzy identyfikują też istniejący lek przeciwpsychotyczny, który mógłby zostać ponownie zastosowany do zakłócenia tej szkodliwej sieci.
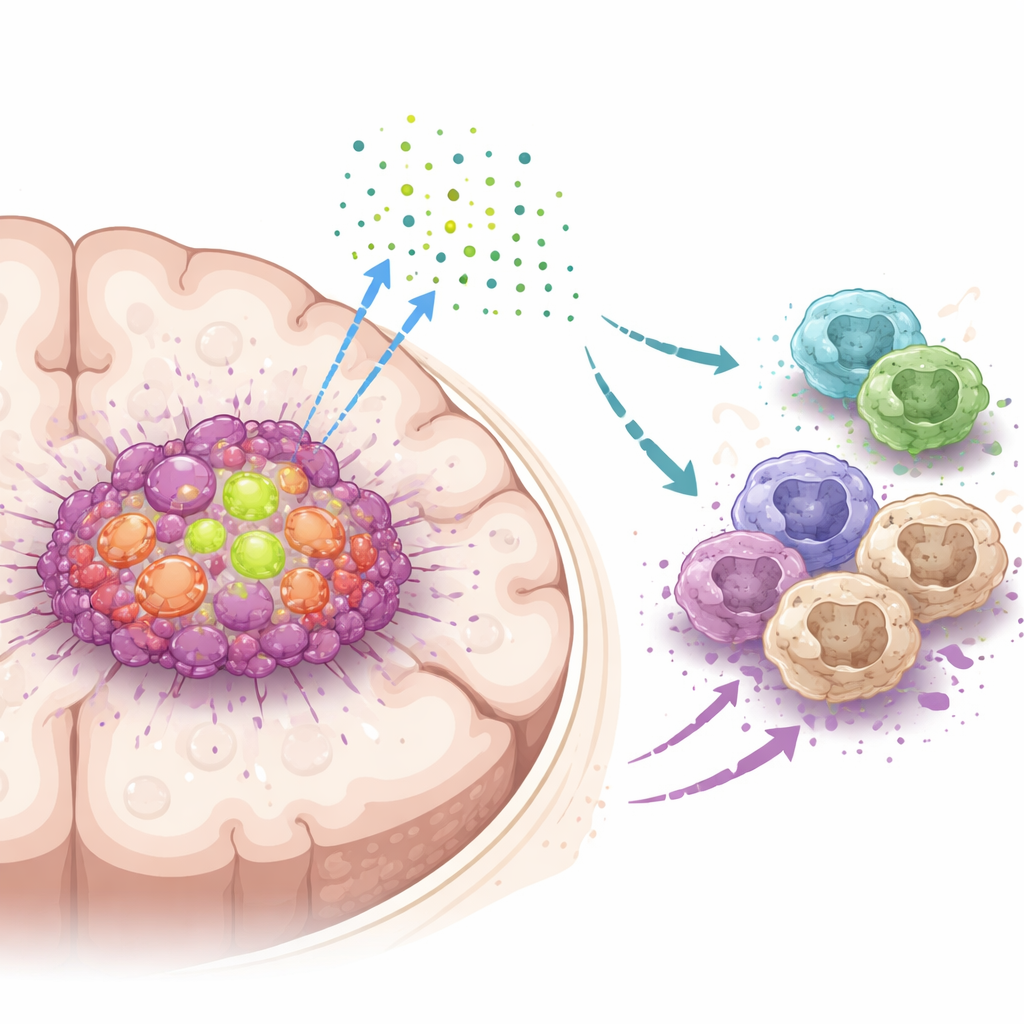
Kluczowy pomocnik wewnątrz komórek guza mózgu
Zespół skupił się na białku DDX39A, molekularnej maszynie pomagającej komórkom w przetwarzaniu RNA, roboczej kopii informacji genetycznej. Analiza dużych zbiorów danych pacjentów i próbek guzów wykazała, że DDX39A jest znacznie bardziej aktywna w glejakach niż w prawidłowej tkance mózgowej, a jej poziomy rosną wraz z zaawansowaniem guza. Analizy pojedynczych komórek pokazały, że DDX39A jest szczególnie obfita w szybko dzielących się komórkach nowotworowych oraz w pewnych komórkach odpornościowych zwanych makrofagami obecnymi w masie guza. Pacjenci, których guzy miały wyższe stężenia DDX39A, mieli gorsze rokowanie, co sugeruje bliski związek tego białka z agresywnym przebiegiem choroby.
Jak ten pomocnik napędza wzrost i rozprzestrzenianie się
Aby sprawdzić, co faktycznie robi DDX39A, badacze użyli narzędzi genetycznych do jego zahamowania w komórkach przypominających komórki macierzyste glejaka hodowanych w laboratorium oraz w modelach mysich nowotworów mózgu. Po obniżeniu poziomów DDX39A komórki nowotworowe rosły wolniej, mniej skutecznie naciekały otaczające tkanki i częściej ulegały zaprogramowanej śmierci. Komórki przypominające komórki macierzyste utraciły również dużą część zdolności do formowania nowych sfer nowotworowych, co jest oznaką upośledzenia ich samoodnawiania. U myszy guzy z obniżoną DDX39A były mniejsze, a zwierzęta żyły dłużej, potwierdzając, że to białko aktywnie napędza postęp guza, a nie tylko go oznacza.
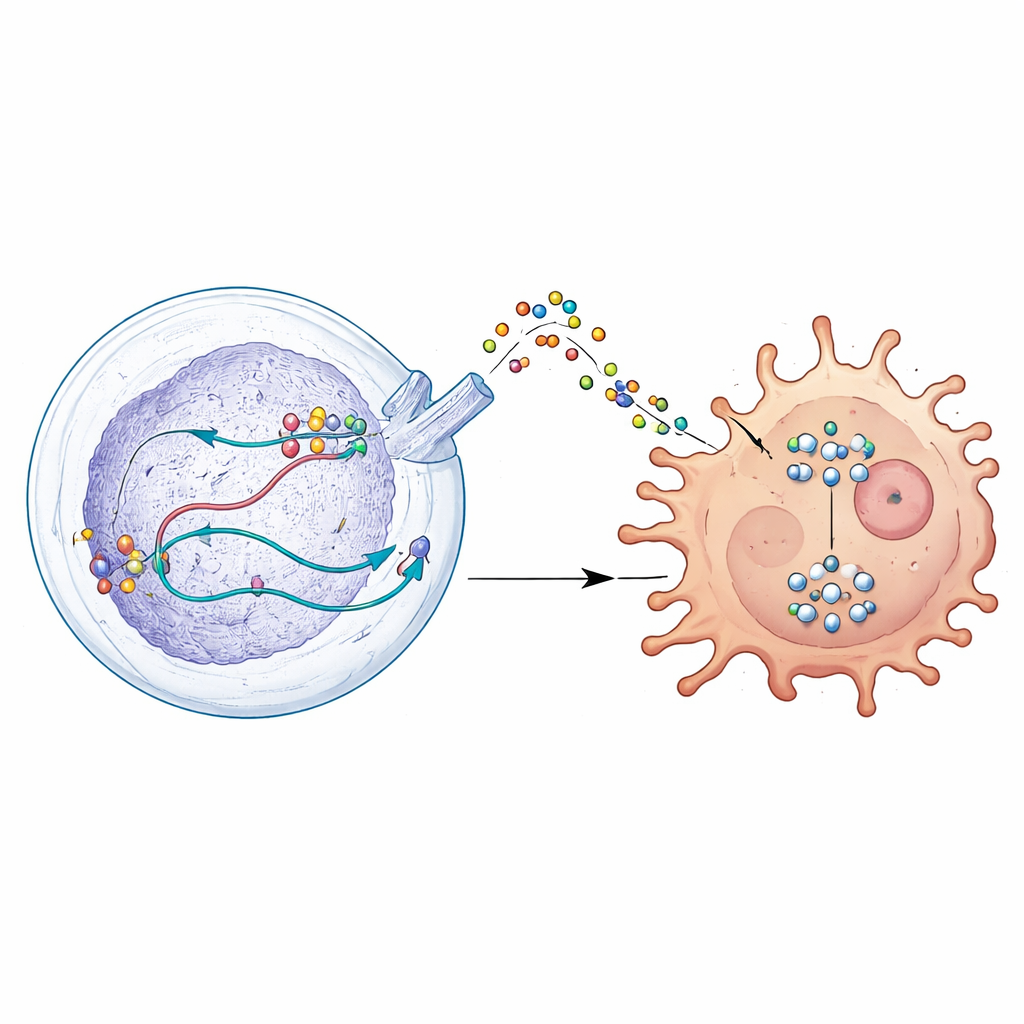
Tajny sygnał, który unieszkodliwia obrońców odpornościowych
Wnikliwsze badania ujawniły, że DDX39A zmienia sposób przetwarzania genu WISP1. Zamiast jedynie włączać lub wyłączać WISP1, DDX39A kształtuje jego RNA w sposób stabilizujący przekaz i zwiększający produkcję białka WISP1. Komórki nowotworowe uwalniają następnie WISP1 do otoczenia, gdzie działa on jak zwodniczy sygnał. Pobliskie makrofagi, które mogą albo atakować guzy, albo je wspierać, reagują na ten sygnał przechodząc w immunosupresyjny, sprzyjający guzowi stan. Ta zmiana jest napędzana przez aktywację szlaku kontrolującego wzrost komórkowy znanego jako AKT. Gdy DDX39A lub WISP1 zostały zmniejszone, aktywność tego szlaku osłabła, komórki nowotworowe stały się mniej agresywne, a makrofagi przesunęły się z powrotem w kierunku profilu bardziej przeciwnowotworowego.
Przekształcenie leku psychiatrycznego w broń przeciw nowotworowi
Posiadając mapę tego szlaku, badacze przeszukali bazy danych leków w poszukiwaniu molekuł, które mogłyby zaburzyć aktywność DDX39A. Skupili się na flufenazynie, długo stosowanym leku przeciwpsychotycznym, który przenika do mózgu. Modelowanie komputerowe i testy wiązania wykazały, że flufenazyna może bezpośrednio przyłączać się do DDX39A. W komórkach nowotworowych lek osłabił wiązanie DDX39A z RNA WISP1, obniżył poziomy WISP1 i zmniejszył sygnalizację AKT. Leczone komórki rosły mniej, mniej naciekały, tworzyły mniej sfer nowotworowych i częściej umierały. W modelach mysich flufenazyna spowolniła wzrost guza mózgu, zmniejszyła liczbę makrofagów wspierających guz i wydłużyła przeżycie, przy podawaniu dawek porównywalnych z tymi stosowanymi u ludzi w innych schorzeniach.
Co to znaczy dla przyszłego leczenia
Mówiąc prościej, badanie pokazuje, że komórki glejaka wykorzystują DDX39A do dopracowania przekazu (WISP1), który zarówno zwiększa ich własną wytrzymałość, jak i przeprogramowuje pobliskie komórki odpornościowe na ochroniarzy zamiast żołnierzy. Zablokowanie tego pomocnika, genetycznie lub za pomocą leku takiego jak flufenazyna, osłabia nowotwór na dwóch frontach: same komórki guza oraz ochronna osłona immunosupresyjnych makrofagów. Choć potrzeba znacznie więcej badań, zanim ta strategia będzie mogła być stosowana u pacjentów, praca otwiera obiecującą drogę do ponownego zastosowania znanego leku w celu uderzenia w nowo odkryty słaby punkt jednego z najbardziej uciążliwych nowotworów mózgu.
Cytowanie: Zhang, Y., Xue, Z., Zhang, N. et al. The multifunctional RNA helicase DDX39A drives glioblastoma progression by modulating WISP1 alternative splicing that induces an immunosuppressive macrophage polarization. Oncogene 45, 1026–1041 (2026). https://doi.org/10.1038/s41388-026-03715-x
Słowa kluczowe: glejak wielopostaciowy, składanie RNA, mikrośrodowisko guza, polaryzacja makrofagów, ponowne zastosowanie leków