Clear Sky Science · pl
ULK1 sprzyja postępowi przerzutów w modelach eksperymentalnych raka nabłonkowego jajnika
Dlaczego te badania mają znaczenie
Rak nabłonkowy jajnika często zostaje wykryty dopiero po cichym rozprzestrzenieniu się w jamie brzusznej, co czyni go jednym z najgroźniejszych nowotworów dotykających kobiety. Kluczowym etapem tego rozprzestrzeniania jest tworzenie się drobnych skupisk komórek nowotworowych, zwanych sferoidami, które unoszą się w płynie jamy brzusznej, przetrwają chemioterapię i zasiewają nowe guzy. W tym badaniu postawiono skoncentrowane pytanie o dużych implikacjach: czy komórkowy „wyłącznik przetrwania” zwany ULK1 pomaga tym skupiskom przetrwać i się rozprzestrzeniać, a jego wyłączenie może otworzyć nowe możliwości leczenia zaawansowanego raka jajnika?
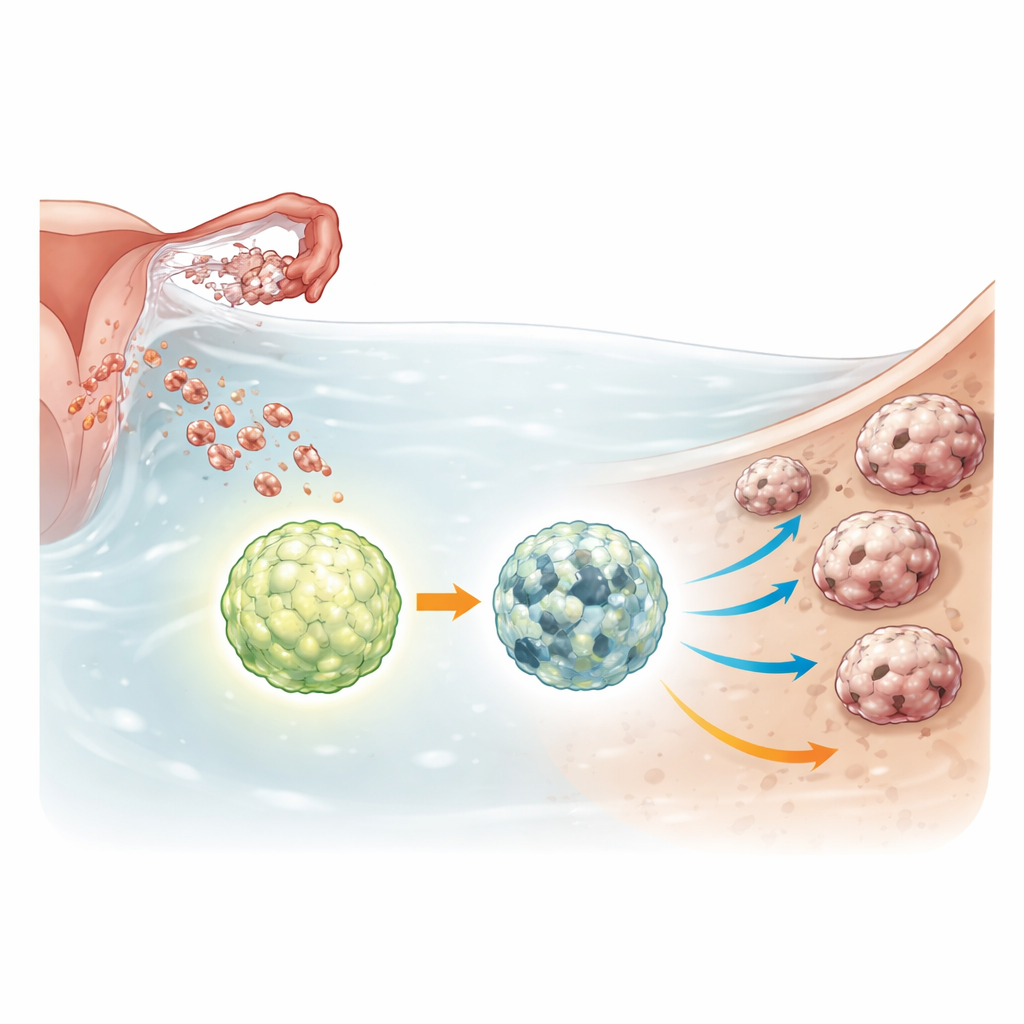
Wyłącznik przetrwania wewnątrz klastrów komórek nowotworowych
Sferoidy raka jajnika muszą znosić trudne warunki: niską dostępność składników odżywczych, brak przyczepności oraz ekspozycję na chemioterapię. Aby sobie z tym poradzić, nasilają proces recyklingu zwany autofagią, który rozkłada i ponownie wykorzystuje wewnętrzne składniki komórkowe, utrzymując komórki przy życiu w warunkach stresu. ULK1 jest głównym przełącznikiem uruchamiającym ten system recyklingu. Badacze użyli narzędzi do edycji genów, aby całkowicie usunąć ULK1 z kilku linii komórek raka jajnika oraz z nie-nowotworowej linii komórek jajowodu, reprezentującej wczesne, przednowotworowe stadium. Następnie porównali zachowanie komórek normalnych i pozbawionych ULK1, gdy hodowano je jako wolno pływające sferoidy lub jako trójwymiarowe mini-guzy zwane organoidami.
Co się dzieje, gdy wyłącznik zostaje wyłączony
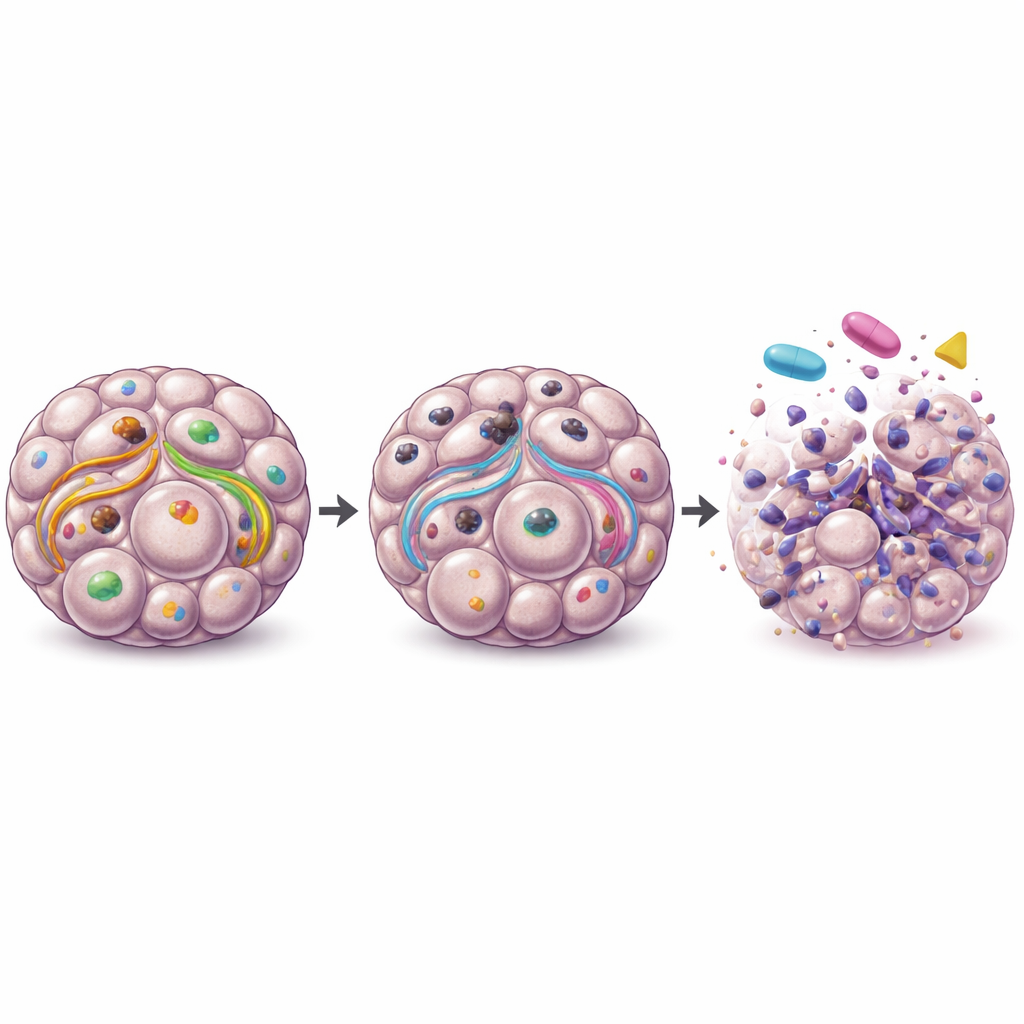
Gdy ULK1 został usunięty w komórkach raka jajnika, ich zdolność do prowadzenia autofagii wewnątrz sferoidów była silnie upośledzona, co wykazano za pomocą zmian w kluczowych białkach związanych z recyklingiem. Sferoidy pozbawione ULK1 zawierały mniej żywych komórek i wykazywały zwiększone oznaki programowanej śmierci komórkowej, co wskazuje, że klastry nowotworowe nie były już w stanie tak skutecznie przetrwać warunków stresowych. Co istotne, usunięcie ULK1 z nie-nowotworowych komórek prekursorowych nie wyłączyło w takim stopniu ich systemu recyklingu, co sugeruje, że komórki nowotworowe są bardziej zależne od ULK1 niż ich zdrowe odpowiedniki. Ta specyficzna dla raka zależność czyni z ULK1 atrakcyjny cel terapeutyczny.
Spowolnienie rozprzestrzeniania i osłabienie przyczółków guza
Ponad przetrwaniem w zawiesinie, sferoidy muszą przyczepić się do i wnikać w gładką wyściółkę jamy brzusznej, aby utworzyć nowe guzy. W modelach laboratoryjnych odwzorowujących ten wczesny etap przerzutów zespół wykazał, że sferoidy pozbawione ULK1 były wyraźnie gorsze w odsuwaniu i najeżdżaniu warstwy komórek mezotelialnych, które normalnie pokrywają narządy brzuszne. Hodowane jako organoidy zatopione w żelopodobnej macierzy, komórki nowotworowe bez ULK1 tworzyły również mniejsze, mniej masywne struktury guza. W modelach mysich, gdzie ludzkie komórki raka jajnika wstrzyknięto do jamy brzusznej, utrata ULK1 skutkowała mniejszą liczbą ognisk guzów i mniejszym nagromadzeniem płynu — oboma cechami zaawansowanej choroby — chociaż ogólne przeżycie zwierząt nie uległo poprawie.
Osłabienie kluczowych sygnałów i wzmocnienie efektów leków celowanych
Aby zrozumieć, jak ULK1 wspiera nowotwór poza autofagią, badacze zmapowali zmiany białkowe w sferoidach pozbawionych ULK1. Stwierdzili zaburzenia w głównych szlakach wzrostu i przeżycia komórki — w szczególności w szlakach MEK–MAPK oraz PI3K–AKT–mTOR. Szlaki te zwykle pomagają komórkom nowotworowym opierać się śmierci i dalej się dzielić. Gdy zespół leczył sferoidy pozbawione ULK1 lekami blokującymi MEK lub mTOR, klastry nowotworowe stały się znacznie bardziej wrażliwe, z wyraźnie zmniejszoną żywotnością i zdolnością do ponownego przyczepiania się. W przeciwieństwie do tego, usunięcie ULK1 nie zwiększyło skuteczności standardowych leków chemioterapeutycznych, takich jak karboplatyna, paklitaksel czy inhibitor PARP olaparib, a w niektórych warunkach wydawało się osłabiać ich działanie.
Wskazówki z próbek pacjentów i miniaturowych modeli pacjentów
Analizując duże publiczne zbiory danych dotyczące guzów jajnika, autorzy stwierdzili, że wyższa aktywność genu ULK1 wiązała się z gorszym długoterminowym przeżyciem i była szczególnie zwiększona w próbkach przerzutowych w porównaniu z guzami pierwotnymi i tkanką normalną. Aby przybliżyć badania do kliniki, przetestowali doustny lek blokujący ULK1, DCC-3116, na organoidach pochodzących od pacjentów hodowanych z próbek przerzutowych. W podzbiorze tych modeli pacjentów blokada ULK1 sama w sobie lub stosowanie leków przeciwko MEK lub mTOR pojedynczo zmniejszała przeżywalność organoidów, chociaż łączenie tych środków nie dało konsekwentnie dodatkowej korzyści. Inne organoidy pacjentów były oporne na wszystkie leczenia, co podkreśla, jak zróżnicowane mogą być raki jajnika i potrzebę biomarkerów pozwalających wytypować pacjentki, które mogłyby odnieść korzyść.
Co to oznacza dla przyszłej opieki
Podsumowując, wyniki przedstawiają ULK1 jako centralnego sojusznika rozprzestrzeniania się raka jajnika: napędza on wewnętrzny recykling utrzymujący przy życiu klastry sferoidów, wspiera ich zdolność do inwazji nowych miejsc i pomaga utrzymywać silne sygnały wzrostowe. Wyłączenie ULK1 osłabia te procesy, zmniejsza rozmiary eksperymentalnych guzów i zwiększa wrażliwość klastrów komórek nowotworowych na niektóre leki celowane, choć nie na standardową chemioterapię. Dla pacjentów praca ta sugeruje, że ULK1 mógłby stać się elementem strategii medycyny spersonalizowanej — szczególnie u osób z chorobą przerzutową o wysokiej aktywności ULK1 — gdzie inhibitory ULK1 łączono by z blokadami MEK lub mTOR, aby ograniczyć wzrost i rozprzestrzenianie się guza, pod warunkiem że dokładne testy pozwolą wytypować guzy najbardziej skłonne do odpowiedzi.
Cytowanie: Webb, J.D., Buensuceso, A., Tomas, E.J. et al. ULK1 promotes metastatic progression in experimental models of epithelial ovarian cancer. Oncogene 45, 1111–1127 (2026). https://doi.org/10.1038/s41388-026-03702-2
Słowa kluczowe: rak jajnika, przerzuty, autofagia, ULK1, terapia celowana