Clear Sky Science · pl
Powiązania retinoidów, receptorów kwasu retinowego i epigenetyki w raku piersi
Dlaczego witamina A ma znaczenie w raku piersi
Większość osób zna witaminę A jako składnik odżywczy ważny dla wzroku, ale jej aktywna postać w organizmie, kwas retinowy, pomaga także komórkom decydować, czy się dzielić, wyspecjalizować, czy zniszczyć w przypadku uszkodzenia. Artykuł przeglądowy omawia, jak kwas retinowy i jego komórkowe „stacje dokujące” są zmieniane w raku piersi, dlaczego obiecujące wyniki badań laboratoryjnych nie przełożyły się jeszcze na skuteczne leki dla pacjentek oraz jak nowe odkrycia dotyczące „oprogramowania” komórki nowotworowej — jej kodu epigenetycznego — mogą ożywić tę strategię terapeutyczną.
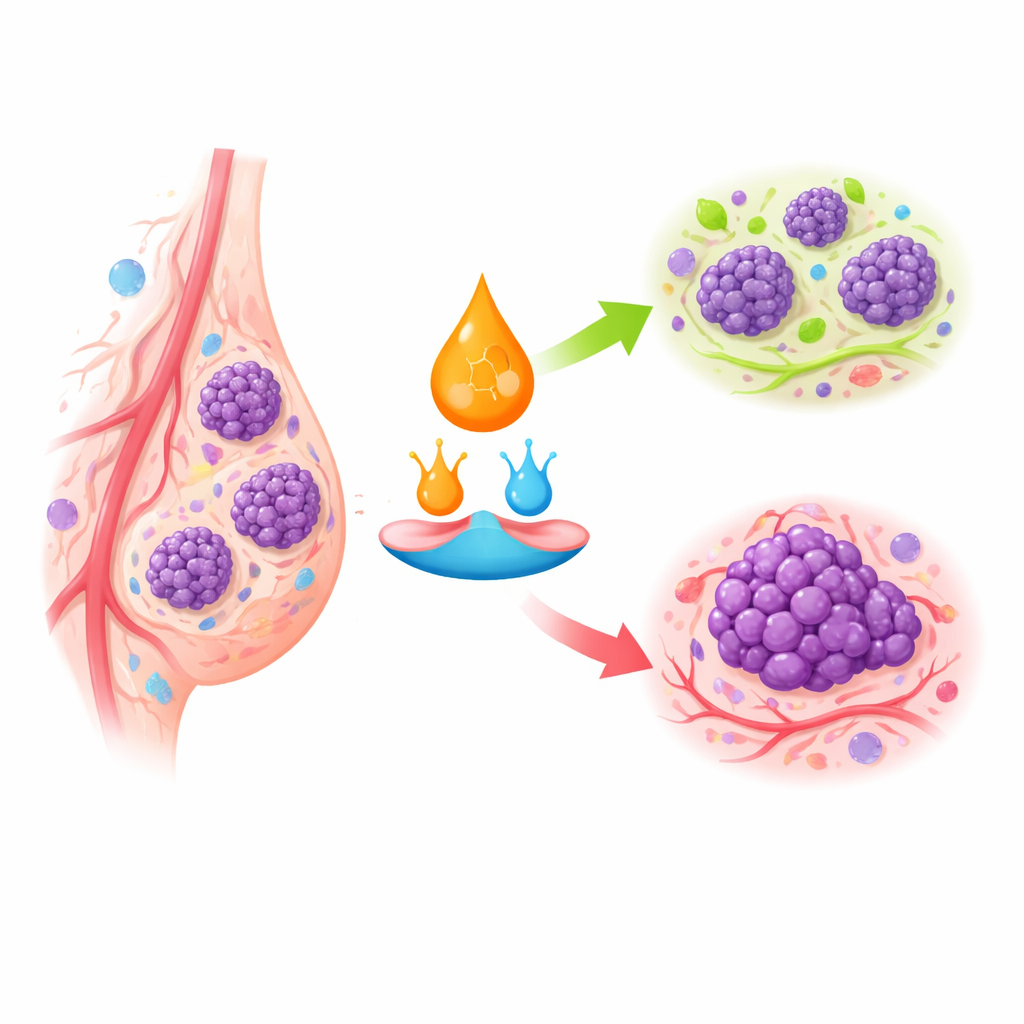
Komórkowe światła drogowe wzrostu i samozniszczenia
Kwas retinowy działa poprzez wiązanie się ze specyficznymi receptorami wewnątrz komórek, które następnie włączają lub wyłączają całe grupy genów. W zdrowej tkance piersi ten system skłania komórki do zaprzestania podziałów, dojrzewania do stabilnych postaci lub obumierania, gdy stają się nieprawidłowe. W raku piersi, zwłaszcza w bardziej agresywnych podtypach, kluczowe receptory są nieobecne lub wyciszone, a wewnętrzny transport kwasu retinowego jest przekierowywany. Zamiast trafiać do receptorów hamujących wzrost, może być skierowany na ścieżki sprzyjające przeżyciu i namnażaniu. Tłumaczy to, dlaczego niektóre guzy piersi słabo reagują na leki retinoidowe, mimo że te same leki są bardzo skuteczne w niektórych nowotworach krwi.
Ukryte wyłączniki w „oprogramowaniu” komórki nowotworowej
Autorzy koncentrują się na epigenetyce — chemicznych znacznikach na DNA i białkach pakujących je, które działają jak ustawienia oprogramowania dla genomu. W wielu rakach piersi te znaczniki blokują ważne receptory kwasu retinowego, szczególnie jeden zwany RARβ2, w pozycji „wyłączonej”, nie zmieniając przy tym sekwencji DNA. Dodatkowe grupy metylowe na DNA i zagęszczenie otaczającego białkowego szpulaż (chromatyny) zamykają ten receptor, podczas gdy inne enzymy przekształcają krajobraz chromatyny, sprzyjając wzrostowi i migracji. Niekodujące RNA, które nie tworzą białek, lecz wpływają na aktywność genów, dodatkowo przesuwają sygnalizację z dala od śmierci komórkowej i różnicowania. Razem te zmiany dają komórkom nowotworowym elastyczność w opieraniu się terapiom i dostosowywaniu się do stresu.
Przeprogramowywanie ścieżek sygnałowych
Co ważne, te epigenetyczne blokady są odwracalne. W modelach laboratoryjnych leki usuwające metylację DNA lub rozluźniające chromatynę mogą przywrócić ekspresję RARβ2 i innych elementów szlaku kwasu retinowego. W połączeniu z samym kwasem retinowym i standardową chemioterapią te „prymujące” środki skuteczniej zmniejszają guzy i redukują pulę komórek o cechach macierzystych, które uważa się za odpowiedzialne za nawroty. Ważny jest także sposób, w jaki kwas retinowy jest transportowany wewnątrz komórki: jeden białkowy nośnik kieruje go do receptorów hamujących wzrost, podczas gdy inny dostarcza go do szlaków pro‑wzrostowych. Zmiana równowagi między tymi nośnikami może przestawić działanie kwasu retinowego z „nawozu” na „hamulec”.
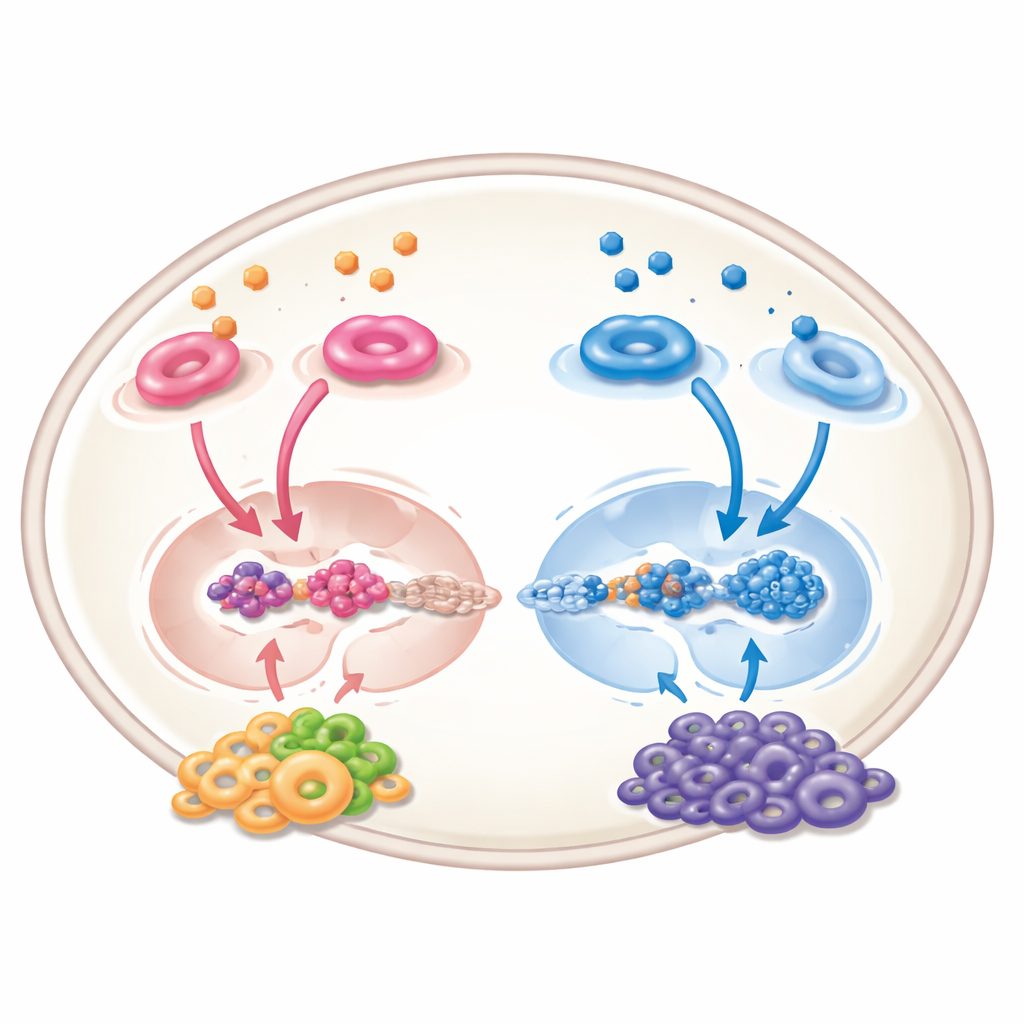
Ponad guz: efekt sąsiedztwa
Kwas retinowy nie działa wyłącznie na komórki nowotworowe; wpływa także na „sąsiedztwo” guza — naczynia krwionośne, komórki układu odpornościowego i komórki podporowe. W systemach eksperymentalnych może ograniczać powstawanie nowych naczyń, przesuwać komórki odpornościowe w kierunku bardziej aktywnego, zwalczającego nowotwór stanu oraz ograniczać komórki supresyjne, które normalnie tłumią obronę organizmu. Jednak obraz nie jest w pełni pozytywny: w niektórych komórkach zrębu otaczających guz aktywacja sygnalizacji kwasu retinowego może wręcz wspierać wzrost nowotworu, wzmacniając kanały komunikacji chemicznej przyciągające i podtrzymujące komórki złośliwe. Te przeciwstawne efekty oznaczają, że przyszłe terapie muszą być precyzyjnie dostrojone, by trafiać w odpowiednie typy komórek we właściwy sposób.
Projektowanie mądrzejszych badań klinicznych
Wczesne próby kliniczne leków retinoidowych w raku piersi w dużej mierze zakończyły się niepowodzeniem, ale przeprowadzono je zanim poznano dzisiejsze zrozumienie podtypów, biomarkerów i złożonej farmakologii. Autorzy argumentują, że nowe badania powinny wybierać pacjentki, których guzy wykazują molekularne cechy wrażliwości na retinoidy, takie jak zachowana ekspresja receptorów lub specyficzne wzorce metylacji DNA, oraz łączyć retinoidy z lekami odblokowującymi bariery epigenetyczne, celującymi w szlaki wzrostu lub wzmacniającymi odpowiedź immunologiczną. Ulepszone formulacje utrzymujące stabilne stężenia leku w organizmie, wraz z uważnym monitorowaniem zarówno guza, jak i otaczającej tkanki, będą kluczowe. Jeśli te przeszkody zostaną pokonane, terapie oparte na kwasie retinowym mogą jeszcze znaleźć miejsce jako precyzyjne narzędzia przeciw wybranym formom raka piersi.
Cytowanie: Szymański, Ł., Schenk, T., Ławiński, M. et al. Association of retinoids, retinoic acid receptors and epigenetics in breast cancer. Oncogene 45, 961–970 (2026). https://doi.org/10.1038/s41388-026-03699-8
Słowa kluczowe: kwas retinowy, rak piersi, epigenetyka, terapia różnicowania, mikrośrodowisko guza