Clear Sky Science · pl
Modelowanie dialogu między tkanką tłuszczową a rakiem: perspektywa trójwymiarowa
Dlaczego tłuszcz i rak są bliżej siebie, niż myślisz
Większość z nas postrzega tłuszcz jako dodatkową warstwę albo zapas energii, ale badania pokazują teraz, że to aktywny, „rozmowny” organ, który w zaskakujący sposób wpływa na nasze zdrowie. Ten artykuł przeglądowy bada, jak tkanka tłuszczowa i komórki nowotworowe się komunikują oraz jak nowe trójwymiarowe (3D) modele laboratoryjne pomagają naukowcom wierniej odtworzyć ten dialog niż kiedykolwiek wcześniej. Zrozumienie tej ukrytej rozmowy może poprawić zapobieganie nowotworom, testowanie leków i terapie, szczególnie w świecie, w którym nadwaga staje się powszechna. 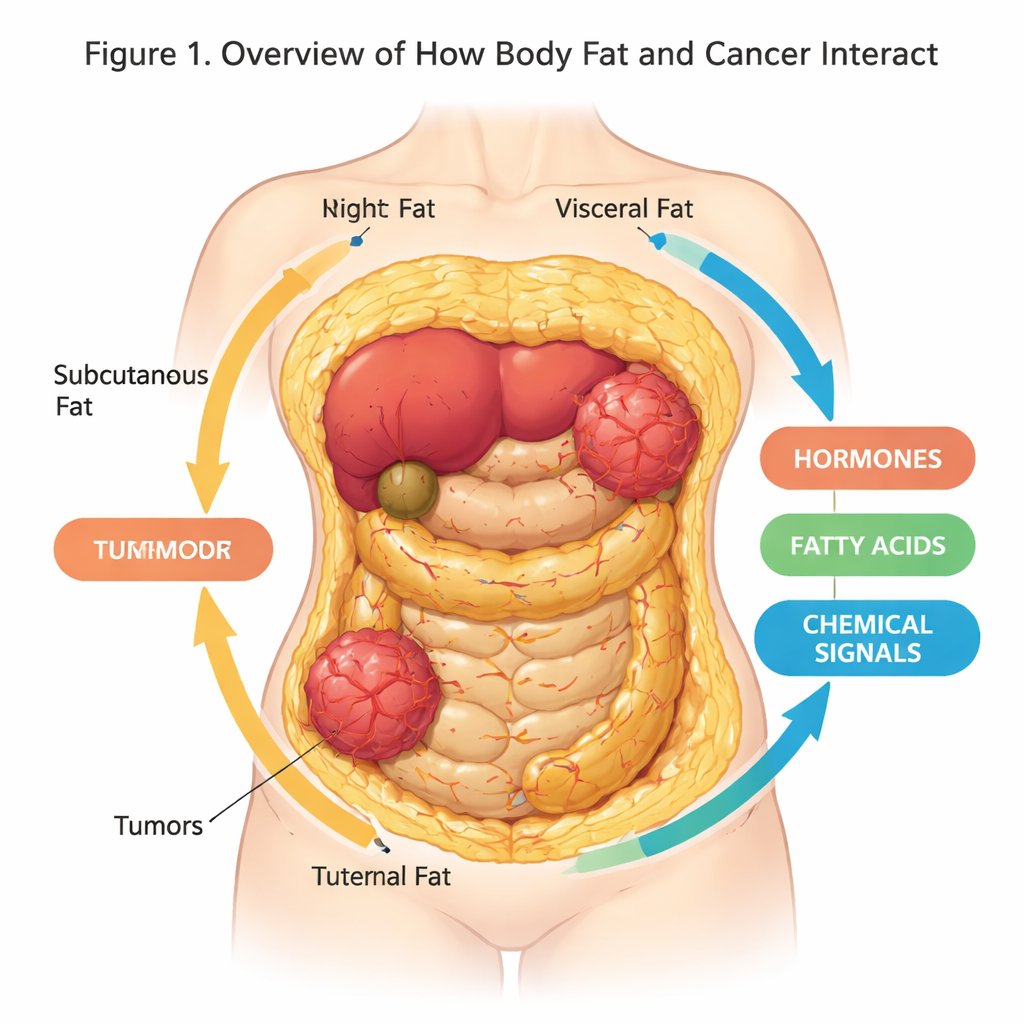
Tłuszcz jako żywy, „mówiący” organ
Tkanka tłuszczowa—nasz tłuszcz ciała—nie jest jedynie biernym miejscem magazynowania. To złożony organ złożony z komórek tłuszczowych, komórek układu odpornościowego, naczyń krwionośnych i komórek podtrzymujących, osadzonych w strukturalnej siatce zwanej macierzą zewnątrzkomórkową. Różne rodzaje tłuszczu występują w różnych miejscach: tłuszcz podskórny pod skórą, trzewny wokół narządów wewnętrznych oraz komórki tłuszczowe białe, brunatne i beżowe, które różnią się sposobem przechowywania energii lub jej spalania w postaci ciepła. Te komórki nieustannie wydzielają koktajl hormonów, kwasów tłuszczowych i białek sygnałowych, które wpływają na metabolizm, zapalenie i, jak wiadomo dziś, ryzyko oraz zachowanie nowotworów.
Otyłość, zapalenie i ryzyko raka
Gdy przybieramy na wadze, komórki tłuszczowe białe zwiększają objętość i liczbę, a tkanka ulega stresowi i zapaleniu. Ten „niezdrowy” tłuszcz uwalnia więcej cząsteczek zapalnych i kwasów tłuszczowych do krwiobiegu, jednocześnie gorzej radząc sobie z metabolizmem cukrów i tłuszczów. Duże badania epidemiologiczne wiążą otyłość z wyższym ryzykiem i gorszymi wynikami wielu rodzajów nowotworów, w tym piersi, jelita grubego, trzustki i macicy. Przegląd opisuje, jak dysfunkcyjny tłuszcz może karmić guzy dodatkowymi paliwami, usztywniać otaczającą tkankę i rekrutować inne typy komórek, które razem tworzą środowisko sprzyjające nowotworowi.
Dwukierunkowa rozmowa między tłuszczem a guzami
Nowotwór postrzega się dziś jako chorobę całego ekosystemu, a nie tylko zbuntowanych komórek. Komórki guzowe sięgają po wsparcie u pobliskiego tłuszczu, przeprogramowując komórki tłuszczowe, komórki odpornościowe i fibroblasty, aby wspomagały ich wzrost i rozprzestrzenianie. W zamian komórki tłuszczowe reagują rozkładem zgromadzonych lipidów i uwalnianiem kwasów tłuszczowych oraz hormonów, z których komórki raka mogą łatwo korzystać. Ten dialog może odbywać się na odległość za pośrednictwem krążących sygnałów lub lokalnie, tam gdzie guzy rosną obok tłuszczu, jak w piersi czy jamie brzusznej. Komórki nowotworowe mogą nawet doprowadzić do utraty pierwotnej tożsamości komórek tłuszczowych, przekształcając je w komórki bardziej przypominające tkankę bliznowatą lub komórki o cechach odpornościowych, które przekształcają tkankę i sprzyjają inwazji. 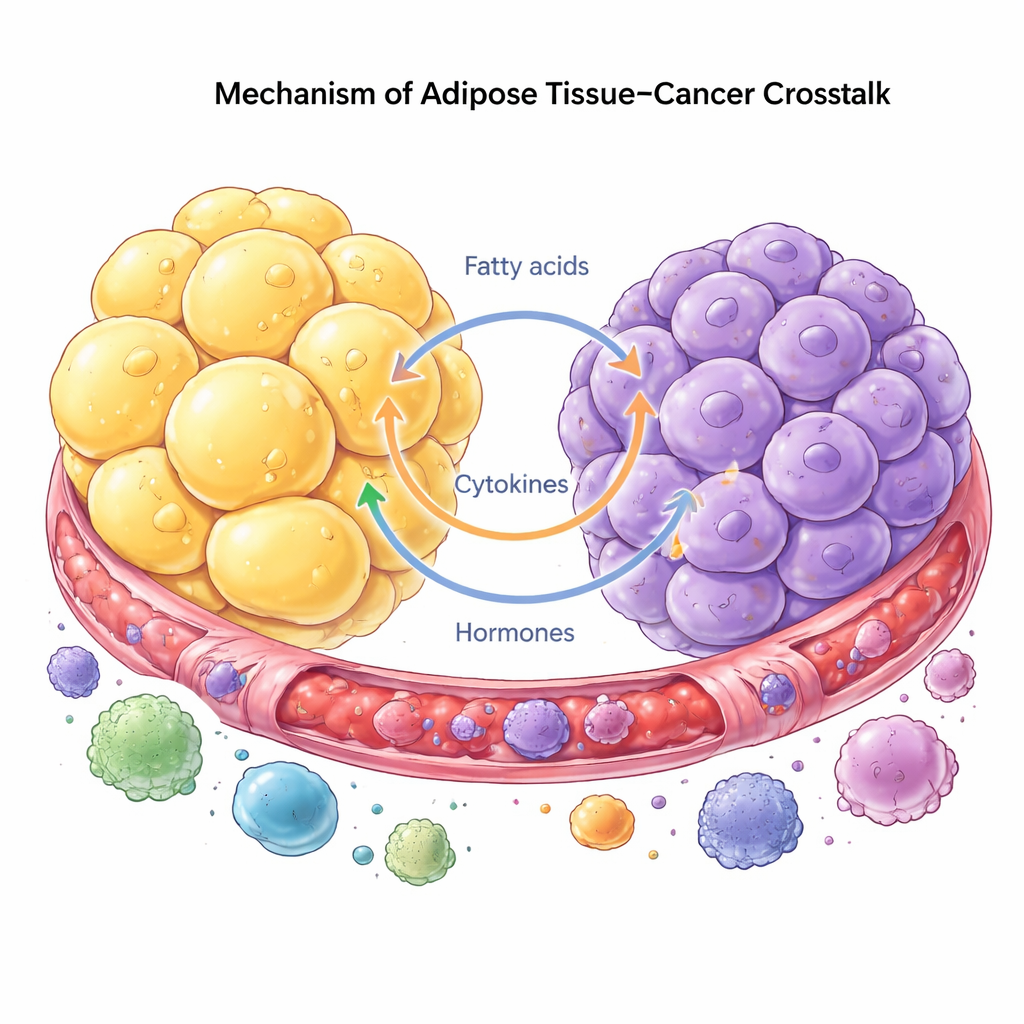
Budowanie miniaturowych tkanek w 3D
Tradycyjne hodowle komórkowe na płaskiej powierzchni (2D) i modele zwierzęce często nie oddają tych złożonych interakcji. Autorzy opisują nową generację systemów 3D, które bardziej przypominają prawdziwą tkankę. Sferoidy to proste skupiska komórek, które samoorganizują się w małe kuliste struktury; rusztowania (scaffolds) to materiały inżynieryjne zapewniające trójwymiarowe podłoże do wzrostu komórek; organoidy to miniaturowe, samoorganizujące się wersje tkanek; a assembloidy łączą wiele organoidów lub sferoidów w złożone „mini-organy”. Naukowcy wykorzystują te podejścia 3D do współhodowli komórek tłuszczowych i nowotworowych, badania, jak warunki podobne do otyłości zmieniają ich zachowanie, oraz testowania, jak leki mogą zakłócić szkodliwy dialog między nimi.
Obietnica i obecne luki
Każdy model ma swoje kompromisy. Sferoidy są tanie i przystosowane do wysokoprzepustowych badań, ale stosunkowo proste. Rusztowania pozwalają na precyzyjną kontrolę właściwości fizycznych, takich jak sztywność, która może wpływać na rozprzestrzenianie się raka, ale są bardziej technicznie wymagające. Organoidy i assembloidy oddają najwyższy poziom realizmu, z wieloma współdziałającymi typami komórek, lecz są kosztowne, trudne do standaryzacji i często pozbawione pełnej sieci naczyń krwionośnych lub elementów układu odpornościowego. Przegląd podkreśla, że współczesne systemy wciąż nie odtwarzają idealnie ludzkiej tkanki tłuszczowej i nowotworowej, zwłaszcza w zakresie pełnej macierzy zewnątrzkomórkowej, dojrzałych komórek tłuszczowych i udziału komórek odpornościowych.
Dokąd zmierza ta dziedzina badań
Autorzy konkludują, że udoskonalenie modeli 3D interakcji tłuszcz–rak jest niezbędne do dokładniejszego testowania leków i odkrywania mechanizmów, dzięki którym otyłość sprzyja nowotworom. W miarę jak te „mini-tkanki” stają się bardziej realistyczne—łącząc wiernie odwzorowany tłuszcz, komórki nowotworowe, naczynia krwionośne i komórki odpornościowe—mogą pomóc badaczom przewidywać, które terapie zadziałają u konkretnych pacjentów, opracować lepsze strategie blokowania wykorzystania tłuszczu przez nowotwór jako paliwa i ostatecznie ukierunkować terapie nie tylko na guzy, lecz także na niezdrowe środowiska, które je wspierają.
Cytowanie: Strusi, G., Suelzu, C.M. & Stebbing, J. Modelling adipose tissue-cancer crosstalk: a three-dimensional perspective. Oncogene 45, 905–913 (2026). https://doi.org/10.1038/s41388-026-03697-w
Słowa kluczowe: tkanka tłuszczowa, otyłość, mikrośrodowisko nowotworu, hodowla komórek 3D, metabolizm guza