Clear Sky Science · pl
YEATS2 promuje naprawę DNA i indukuje oporność na anoikę przez zwiększenie dostępności chromatyny, napędzając przerzuty raka prostaty
Dlaczego komórki nowotworowe, które nie chcą odpuścić, mają znaczenie
Gdy rak rozprzestrzenia się ze swojego pierwotnego miejsca do odległych narządów, leczenie staje się znacznie trudniejsze. Rak prostaty nie jest tu wyjątkiem: gdy utworzy nowe guzy w węzłach chłonnych lub kościach, przeżywalność gwałtownie spada. Aby się rozsiać, komórki nowotworowe muszą najpierw odczepić się od tkanki macierzystej i wejść do naczyń krwionośnych lub limfatycznych. Większość takich wędrowców ginie, ale niebezpieczna garstka zyskuje zdolność do przeciwdziałania śmierci komórkowej wywołanej odłączeniem, procesu zwanego anoiką. To badanie ujawnia, jak białko o nazwie YEATS2 pomaga komórkom raka prostaty przetrwać tę niebezpieczną podróż, wzmacniając ich zdolność do naprawy uszkodzeń DNA.
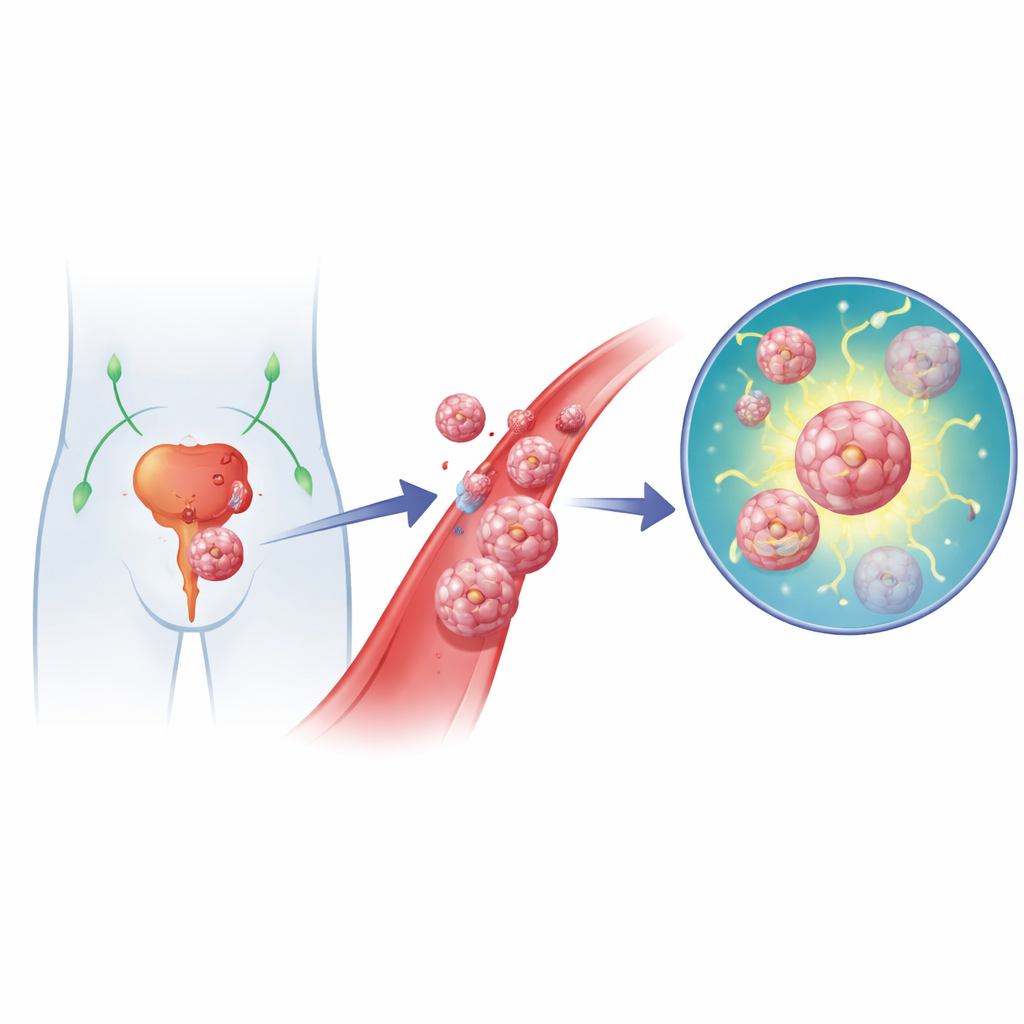
Komórki w ruchu
Naukowcy zaczęli od pytania, co odróżnia guzy przerzutowe raka prostaty od ich pierwotnych odpowiedników. Porównali dane genetyczne z publicznych baz nowotworowych z własnymi eksperymentami na komórkach raka prostaty, które zmuszono do przetrwania bez przyczepu, naśladując warunki panujące we krwi. Zarówno w próbkach pacjentów, jak i w hodowlach laboratoryjnych, niewielki zestaw genów konsekwentnie wyróżniał się jako zmieniony w komórkach przerzutowych i odpornych na anoikę. Wśród nich YEATS2 wykazywał silną regulację w górę i wyraźny związek z gorszymi wynikami: mężczyźni, których guzy miały więcej YEATS2, mieli krótsze przeżycie i szybszy postęp choroby.
Badanie podejrzanego
Aby zbadać rolę YEATS2, zespół opracował modele mysie przerzutów do węzłów chłonnych, wstrzykując komórki raka prostaty w poduszkę stopy zwierząt, a następnie pobierając zarówno guzy pierwotne, jak i pobliskie węzły chłonne. Komórki pobrane z przerzutów do węzłów chłonnych lepiej radziły sobie w zawiesinie, były bardziej ruchliwe i inwazyjne niż ich odpowiedniki z guza pierwotnego. Te komórki przerzutowe wykazywały też większe ilości YEATS2. Sztuczne zwiększenie poziomów YEATS2 w komórkach raka prostaty sprawiało, że były one trudniejsze do zabicia po odłączeniu oraz bardziej zdolne do migracji i inwazji w testach laboratoryjnych. Zahamowanie ekspresji YEATS2 dawało efekt odwrotny i znacząco zmniejszało przerzuty do węzłów chłonnych u myszy.
Naprawa DNA jako trik przetrwania
Odłączenie od otaczającej tkanki stresuje komórki nowotworowe, częściowo przez zwiększenie poziomu reaktywnych cząsteczek uszkadzających DNA. Używając znaczników przerw w DNA, autorzy pokazali, że komórki unoszące się w zawiesinie gromadzą więcej uszkodzeń DNA, zwłaszcza jeśli pochodzą z guzów pierwotnych, a nie z przerzutów. Nadekspresja YEATS2 zmniejszała te uszkodzenia, podczas gdy wyciszenie YEATS2 je nasilało i osłabiało przetrwanie w zawiesinie. Dalsze analizy dużych zestawów danych pacjentów ujawniły, że geny związane z odpowiedzią na uszkodzenia DNA i naprawą korelowały silnie z aktywnością YEATS2. Jeden z genów naprawczych, RAD50, wyłonił się jako kluczowy partner: był silnie eksprymowany w komórkach przerzutowych i odpornych na anoikę, jego poziom rósł przy zwiększeniu YEATS2 i pomagał przywrócić przeżywalność po ponownym wprowadzeniu do komórek pozbawionych YEATS2.
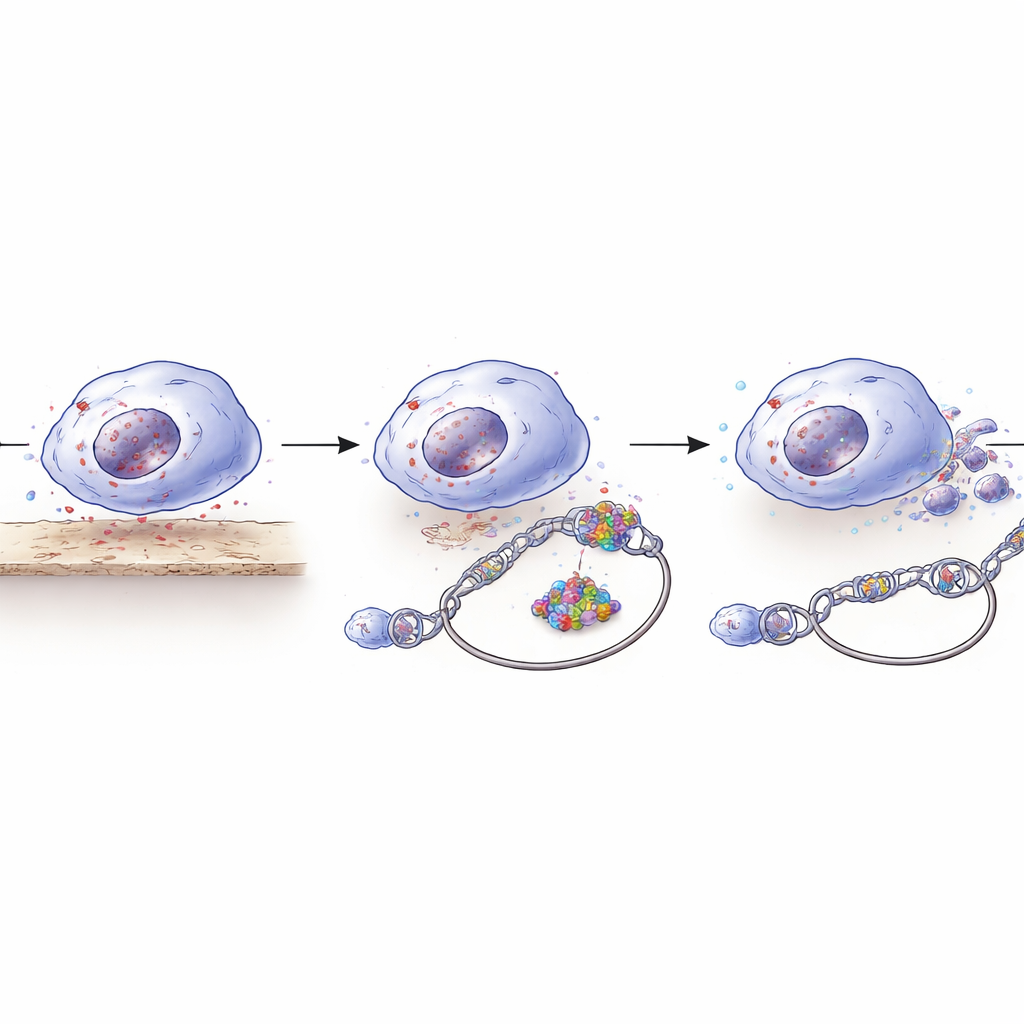
Otwieranie zakładek DNA
Jak YEATS2 podnosi poziom RAD50? YEATS2 jest częścią kompleksu białkowego, który zmienia stopień upakowania DNA, ułatwiając lub utrudniając odczyt pewnych genów. Zespół zastosował technikę mapującą „otwarte” versus „zamknięte” regiony DNA i stwierdził, że YEATS2 zwiększa dostępność regionu promotora RAD50. W tym rozluźnionym fragmencie DNA YEATS2 rozpoznawał chemiczny znacznik na histonach (acetylację H3K27) i dzięki swojej wyspecjalizowanej domenie YEATS przyciągał dodatkowe grupy acetylowe w pobliskich pozycjach. Te zmiany działały jak otwarcie zakładki i podkreślenie akapitu, pozwalając czynnikowi transkrypcyjnemu NR2C2 lepiej się wiązać i napędzać produkcję RAD50. Razem YEATS2 i NR2C2 tworzyły obwód pro-przetrwaniowy, który zwiększał zdolność naprawczą dokładnie wtedy, gdy odłączone komórki nowotworowe najbardziej tego potrzebowały.
Zamykanie drogi ucieczki
Ponieważ RAD50 jest częścią kompleksu MRN, kluczowego mechanizmu naprawy groźnych podwójnych pęknięć DNA, naukowcy zbadali, czy zakłócenie tej maszyny może osłabić przerzuty. Użyli Mirin, małocząsteczkowego inhibitora kompleksu MRN, oraz obniżyli poziomy jednego z partnerów RAD50, MRE11. Obie strategie zwiększały uszkodzenia DNA i zmniejszały zdolność komórek raka prostaty do kolonizacji płuc lub węzłów chłonnych u myszy, nawet gdy RAD50 był obficie obecny. Wyniki te sugerują, że przerzutowy rak prostaty w dużym stopniu polega na wzmocnionej naprawie DNA, aby przetrwać odłączenie i podróż.
Co to oznacza dla pacjentów
Mówiąc prosto, praca ta pokazuje, że niektóre komórki raka prostaty unikają śmierci, ucząc się skuteczniej łatać swoje DNA w najbardziej niebezpiecznej fazie podróży: gdy odrywały się od miejsca pochodzenia. YEATS2 działa jak molekularny ułatwiacz, otwierając właściwe strony książki genetycznej, żeby RAD50 i jego partnerzy naprawczy mogli być produkowani w dużych ilościach. Ta wzmocniona naprawa pozwala zbłąkanym komórkom przemieszczać się krwią lub układem limfatycznym bez umierania, zwiększając szanse na zaszczepienie nowych guzów. Celowanie w szlak YEATS2–NR2C2–RAD50 lub w sam kompleks naprawczy MRN może zatem zaoferować nowe sposoby powstrzymania rozsiewu raka prostaty, potencjalnie poprawiając rokowania u mężczyzn z zaawansowaną chorobą.
Cytowanie: Li, H., Song, Y., Cong, Y. et al. YEATS2 promotes DNA repair and induces anoikis resistance by enhancing chromatin accessibility to drive prostate cancer metastasis. Oncogene 45, 971–988 (2026). https://doi.org/10.1038/s41388-026-03696-x
Słowa kluczowe: przerzuty raka prostaty, naprawa DNA, odporność na anoikę, dostępność chromatyny, RAD50