Clear Sky Science · pl
POM121 O-GlcNAcylacja ułatwia przerzuty do kości w niedrobnokomórkowym raku płuca poprzez zwiększony import jądrowy c-MYC i przeprogramowanie ECM
Dlaczego to badanie ma znaczenie
Gdy rak płuca rozprzestrzenia się do kości, powoduje silny ból, złamania i znaczne skrócenie czasu przeżycia, a lekarze nadal dysponują niewieloma narzędziami, by zatrzymać ten śmiertelny etap. Badanie to analizuje mechanizmy wewnątrz komórek raka płuca, aby odkryć, jak niektóre z nich uzyskują przewagę pozwalającą im przedostać się z płuca do kości i tam prosperować. Śledząc ten proces aż do drobnej modyfikacji pojedynczego białka pełniącego funkcję strażnika bramki jądrowej, autorzy wyznaczają nowy ciąg zdarzeń, który może stanowić cel do lepszego przewidywania, zapobiegania lub leczenia przerzutów do kości u pacjentów z niedrobnokomórkowym rakiem płuca.
Marka cukrowa, która zmienia zachowanie raka
Naukowcy skupili się na modyfikacjach potranslacyjnych, drobnych chemicznych zmianach, które białka nabywają po syntezie. Jedną z takich zmian jest O-GlcNAcylacja — przyłączenie małej cząsteczki cukru w określonych miejscach białek. Korzystając z linii komórkowych raka płuca i modeli mysich, zespół porównał zwykłe komórki nowotworowe z podpopulacjami wielokrotnie selekcjonowanymi ze względu na zdolność kolonizowania kości. Okazało się, że te komórki „szukające kości” miały znacznie wyższy ogólny poziom O-GlcNAcylacji, wynikający ze zwiększonej aktywności enzymu OGT, który zakłada tę cukrową „metkę”. Spośród setek zmodyfikowanych białek na wyróżnienie zasłużył jeden: POM121, podstawowy składnik poru jądrowego, struktury kontrolującej ruch do i z jądra komórkowego.
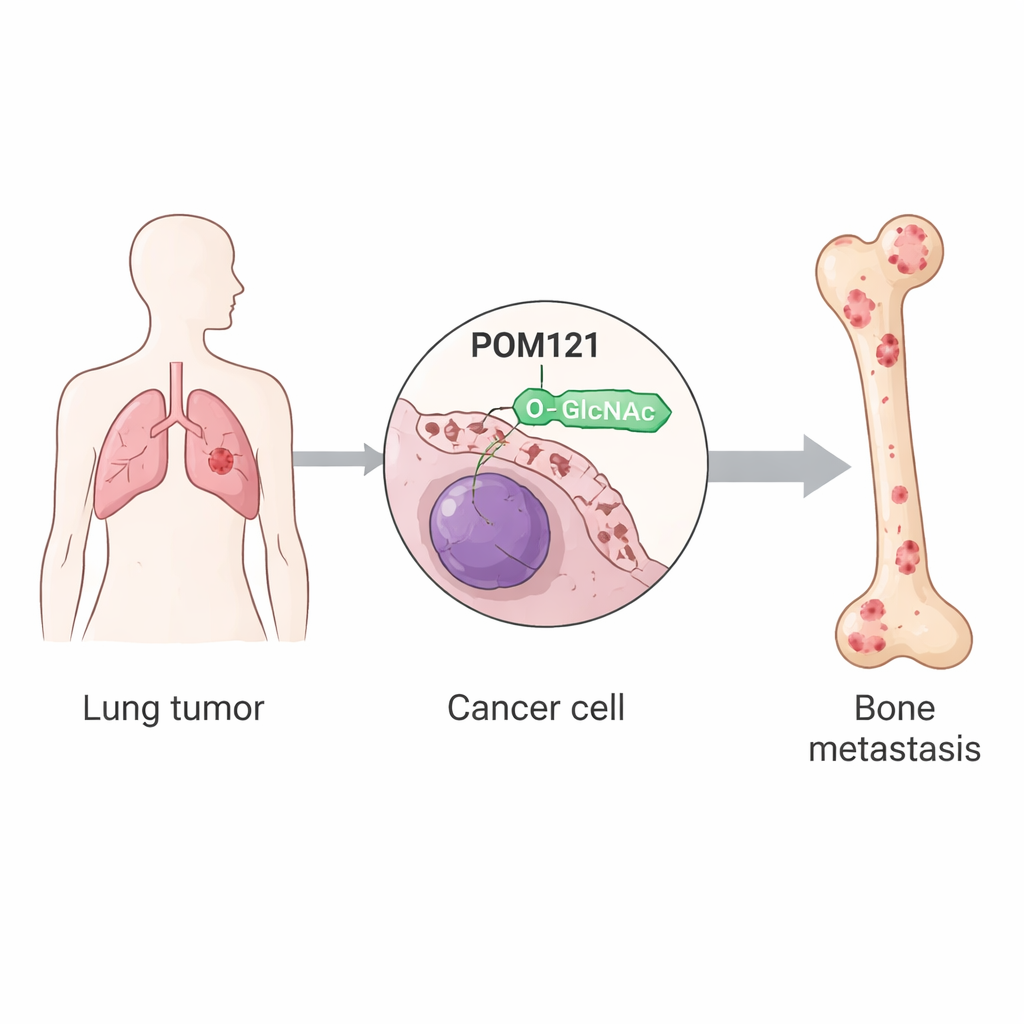
Strażnik jądrowy POM121 zostaje ustabilizowany
POM121 osadza się w błonie otaczającej jądro, tworząc część kanału, przez który musi przechodzić wiele białek sygnałowych. W komórkach raka płuca z przerzutami do kości POM121 nosiło intensywną O-GlcNAcylację w jednym miejscu aminokwasowym zwanym seryną 199. Gdy to miejsce zostało zmienione tak, że nie można go było modyfikować, białko stało się niestabilne i było szybko degradowane przez wewnątrzkomórkowe mechanizmy usuwania. Badanie pokazuje, że cukrowa „metka” chroni POM121 przed oznaczeniem do zniszczenia przez enzym TRIM21, który zwykle przyłącza ubikwitynowe etykiety „do wyrzucenia”. Przy obecności O-GlcNAc TRIM21 słabo się wiąże, ubikwitynacja spada, a POM121 gromadzi się przy porze jądrowym bez zmiany lokalizacji.
Otwarcie drzwi dla potężnego promotora nowotworu
Jaką rolę odgrywa bardziej stabilny POM121? Kluczową rolę odgrywa słynne białko promujące raka, czynnik transkrypcyjny c-MYC. c-MYC musi wejść do jądra, aby włączać geny, ale jego przejście zależy od składników poru jądrowego, takich jak POM121. Autorzy wykazali, że gdy POM121 był obfity i O-GlcNAcylowany, więcej c-MYC znajdowało się w jądrze; gdy poziomy POM121 zostały zredukowane lub jego cukrowa metka usunięta, import jądrowy c-MYC spadał gwałtownie. U myszy komórki raka płuca niosące niemodyfikowalny mutant POM121 tworzyły znacznie mniej i mniejsze przerzuty do kości, podczas gdy przywrócenie c-MYC w komórkach pozbawionych POM121 w dużej mierze przywracało ich zdolność kolonizacji kości. To umieszcza POM121 upstream (powstrzymuje przed) c-MYC w krytycznej ścieżce metastatycznej.
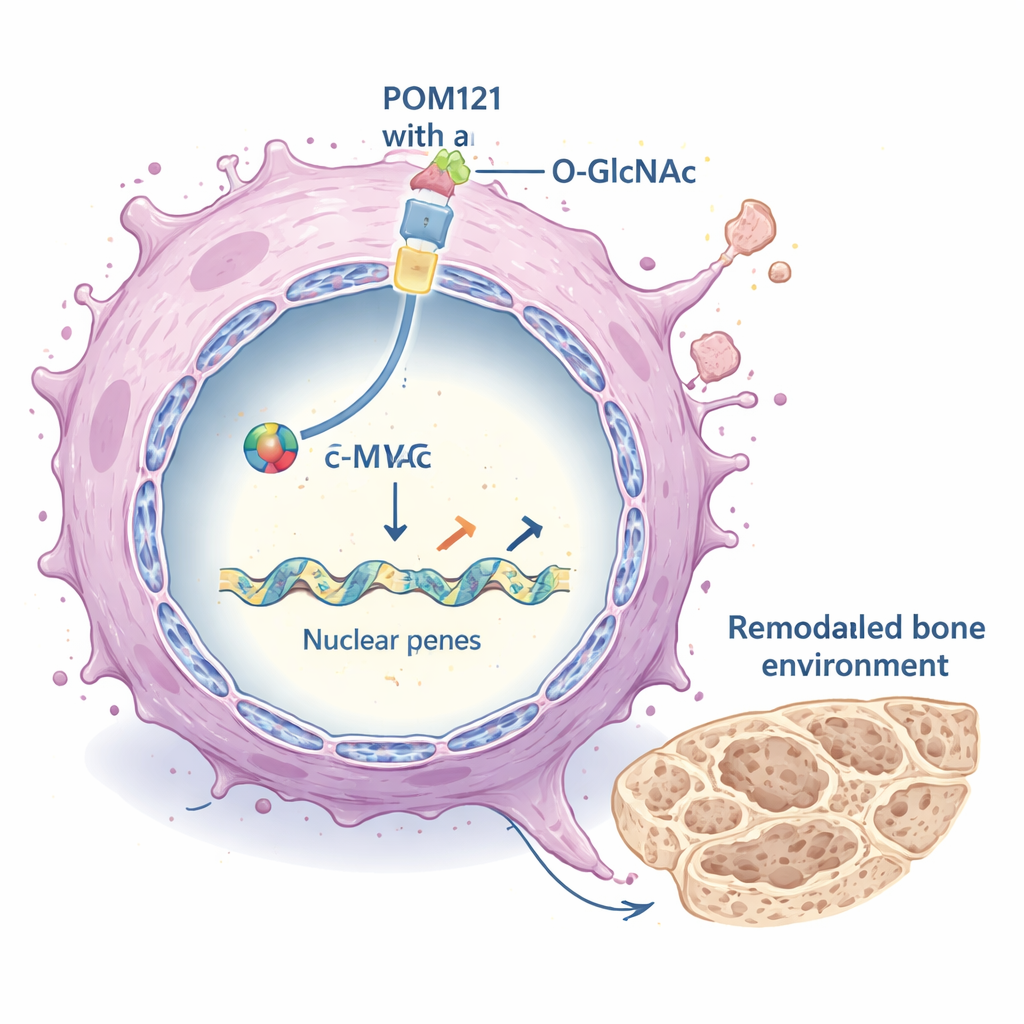
Przeprogramowanie otoczenia guza
Po wejściu do jądra c-MYC działa jako główny przełącznik dla wielu genów. W tym przypadku silnie aktywował zestaw genów kształtujących macierz zewnątrzkomórkową (ECM) — rusztowanie białkowe otaczające komórki. Geny ECM, obejmujące różne kolageny i enzymy przebudowujące strukturę tkanki, były wyciszone, gdy blokowano POM121 lub c-MYC, i aktywowane, gdy O-GlcNAcylacja i POM121 były wysokie. Zmieniona ECM z kolei wzmacniała główne szlaki wzrostu wewnątrz komórek nowotworowych, w szczególności kaskadę sygnalizacyjną PI3K–AKT–mTOR, wspierającą przetrwanie, wzrost i rozprzestrzenianie. Podobne wzorce obserwowano w kilku różnych modelach raka płuca, co sugeruje, że mechanizm nie jest ograniczony do jednej linii komórkowej.
Od odkrycia laboratoryjnego do wpływu na pacjentów
Analiza danych pacjentów wykazała, że wysokie poziomy OGT, POM121 i c-MYC, a także genów ECM, które regulują, wiązały się z gorszymi wynikami oraz z guzami płuca, które już dały przerzuty do kości. Podsumowując, praca opisuje oś OGT–POM121–c-MYC–ECM: zwiększona O-GlcNAcylacja stabilizuje jądrowego strażnika POM121, który transportuje więcej c-MYC do jądra, co następnie przeprogramowuje rusztowanie tkankowe i sygnały wzrostu na korzyść przerzutów do kości. Dla pacjentów oznacza to nowe rodzaje biomarkerów, które mogą wskazywać ryzyko rozprzestrzenienia do kości, oraz nowe strategie terapeutyczne — od blokowania działania OGT lub POM121 po hamowanie c-MYC lub remodelowanie ECM — które mogłyby w przyszłości pomóc powstrzymać rak płuca przed dotarciem do szkieletu.
Cytowanie: Ren, YZ., Zhao, MN., Du, FL. et al. POM121 O-GlcNAcylation facilitates bone metastasis in non-small cell lung cancer through enhanced c-MYC nuclear import and ECM reprogramming. Oncogene 45, 728–743 (2026). https://doi.org/10.1038/s41388-026-03687-y
Słowa kluczowe: przerzuty raka płuca do kości, POM121, O-GlcNAcylacja, c-MYC, macierz zewnątrzkomórkowa