Clear Sky Science · pl
Synaptyczne efekty interleukiny‑6 na ludzkie neurony dopaminergiczne pochodzące z iPSC
Dlaczego zapalenie ma znaczenie dla nastroju
Wiele osób z depresją wykazuje także oznaki niskiego stopnia stanu zapalnego we krwi, a te zmiany immunologiczne są silnie związane z objawami takimi jak utrata przyjemności, zmęczenie i spowolnienie ruchowe. W tym badaniu zadano konkretne pytanie: jak jeden z kluczowych sygnałów zapalnych, cząsteczka zwana interleukiną‑6, bezpośrednio wpływa na ludzkie komórki mózgowe wykorzystujące dopaminę — związek odpowiadający za motywację i nagrodę? Hodując w laboratorium ludzkie neurony produkujące dopaminę z komórek macierzystych, badacze mogli obserwować, jak te komórki reagują na zapalenie i czy odpowiedź ta różni się między osobnikami żeńskimi i męskimi.
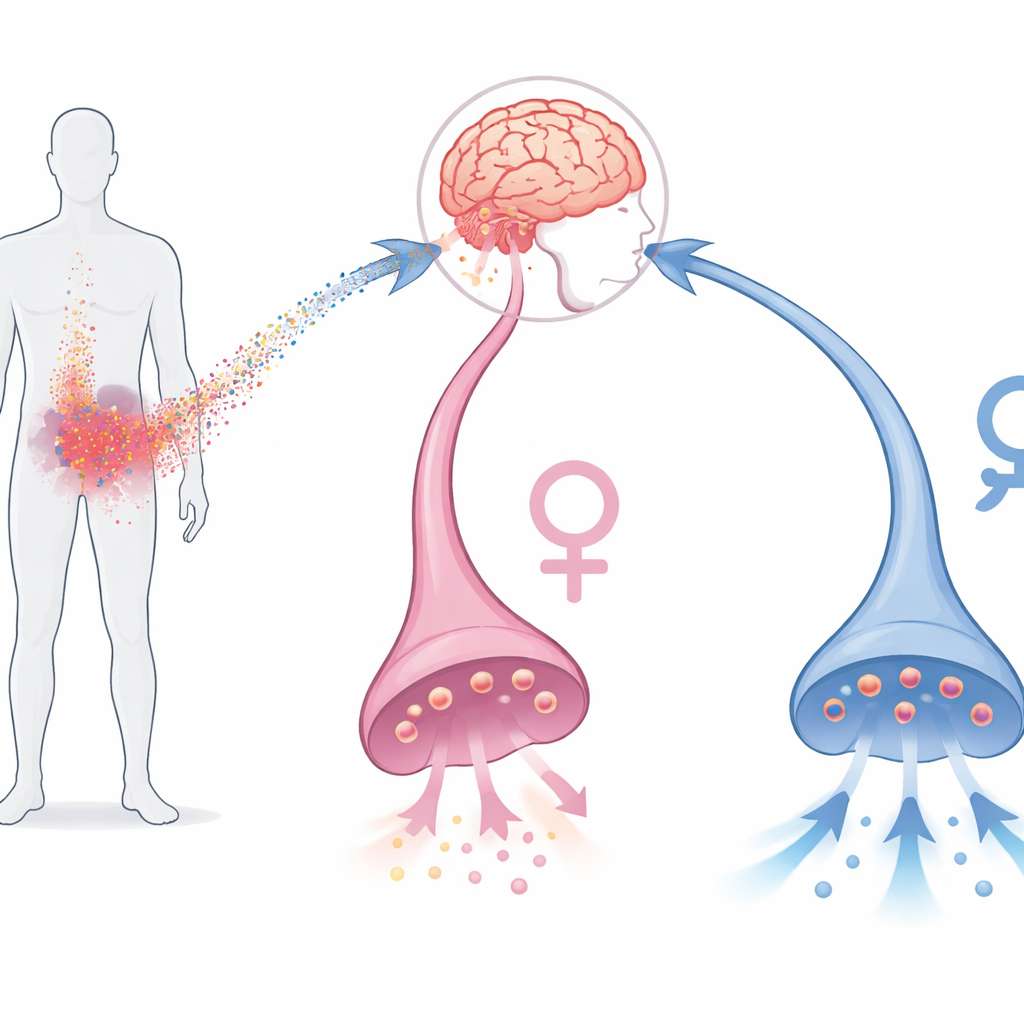
Od sygnałów z krwi do motywacji mózgu
Depresja jest powszechna, powoduje niepełnosprawność i często jest oporna na standardowe leki przeciwdepresyjne, szczególnie u osób, u których badania krwi wykazują wysoki poziom zapalenia. Wcześniejsze badania u ludzi i zwierząt pokazały, że bodźce zapalne mogą osłabiać aktywność obwodów nagrody w mózgu, zwłaszcza w rejonie zwanym prążkowiem brzusznym (ventral striatum), które w dużym stopniu zależy od dopaminy. Gdy poziom cząsteczek zapalnych jest eksperymentalnie podwyższany, ludzie i zwierzęta zwykle wykazują mniejszą motywację do pracy na rzecz nagrody. Interleukina‑6 jest jedną z takich cząsteczek i może docierać do neuronów dopaminowych w mózgu w warunkach stresu. Jednak dokładne mechanizmy, w jaki sposób zmienia ona komórki uwalniające dopaminę, pozostawały niejasne, zwłaszcza w ludzkich neuronach i z uwzględnieniem płci.
Budowanie ludzkich neuronów dopaminowych w naczyniu
Aby zbadać te mechanizmy, zespół przereprogramował komórki skóry lub krwi zdrowych mężczyzn i kobiet do indukowanych pluripotencjalnych komórek macierzystych, a następnie ukierunkował je do różnicowania w neurony dopaminergiczne śródmózgowia, typ zaangażowany w motywację. Po około ośmiu tygodniach dojrzewania te neurony miały oczekiwane markery i aktywność elektryczną. Naukowcy następnie wystawili komórki na działanie interleukiny‑6 przez 24 godziny i zmierzyli trzy kluczowe cechy: ile dopaminy uwalniają, jak często generują impulsy elektryczne oraz jak efektywnie poruszają się i dokują maleńkie pęcherzyki wypełnione dopaminą, by uwolnić swój ładunek.
Różne historie w komórkach żeńskich i męskich
Wyniki ujawniły uderzające rozdzielenie między neuronami pochodzącymi od kobiet i mężczyzn. W komórkach od kobiet interleukina‑6 wyraźnie osłabiała system dopaminowy: uwalnianie dopaminy spadło, częstotliwość wyładowań elektrycznych zmalała, a ruch pęcherzyków synaptycznych stał się bardziej ospały i rzadziej były one „zaparkowane” gotowe do uwolnienia przy zakończeniu nerwowym. W komórkach od mężczyzn te same sygnały zapalne powodowały tylko niewielkie spowolnienia, ale wyzwalały coś, co wyglądało na wrodzoną kompensację. Pęcherzyki poruszały się szybciej i stawały się liczniejsze na terminalach, a liczba presynaptycznych punktów kontaktowych wzrosła — zmiany, które mogłyby pomóc utrzymać wydzielanie dopaminy mimo zapalenia. Analizy ekspresji genów potwierdziły te funkcjonalne różnice, pokazując, że interleukina‑6 aktywowała silniejsze programy zapalne w neuronach pochodzenia żeńskiego niż męskiego.
Długa RNA niekodująca jako ukryty przełącznik
Zagłębiając się dalej, badacze skoncentrowali się na regulatorowej cząsteczce zwanej MIAT, długiej niekodującej RNA, która nie koduje białka, lecz może subtelnie modulować aktywność genów. Neurony dopaminowe męskie miały początkowo wyższe poziomy MIAT niż neurony żeńskie, a interleukina‑6 kierowała MIAT w przeciwne strony w obu płciach. Gdy zespół zastosował edycję genową, by usunąć MIAT w neuronach męskich, komórki straciły swoją ochronną, kompensacyjną odpowiedź. Po ekspozycji na interleukinę‑6 męskie neurony pozbawione MIAT wykazywały teraz zmniejszone uwalnianie dopaminy, wolniejsze wyładowania i mniej zadokowanych pęcherzyków — bardzo podobnie jak neurony żeńskie. MIAT wpływała także na geny kontrolujące recykling dopaminy i wrażliwość komórek na interleukinę‑6, co sugeruje, że działa jako molekularny węzeł kształtujący zdolność neuronów dopaminowych do radzenia sobie ze stresem zapalnym.
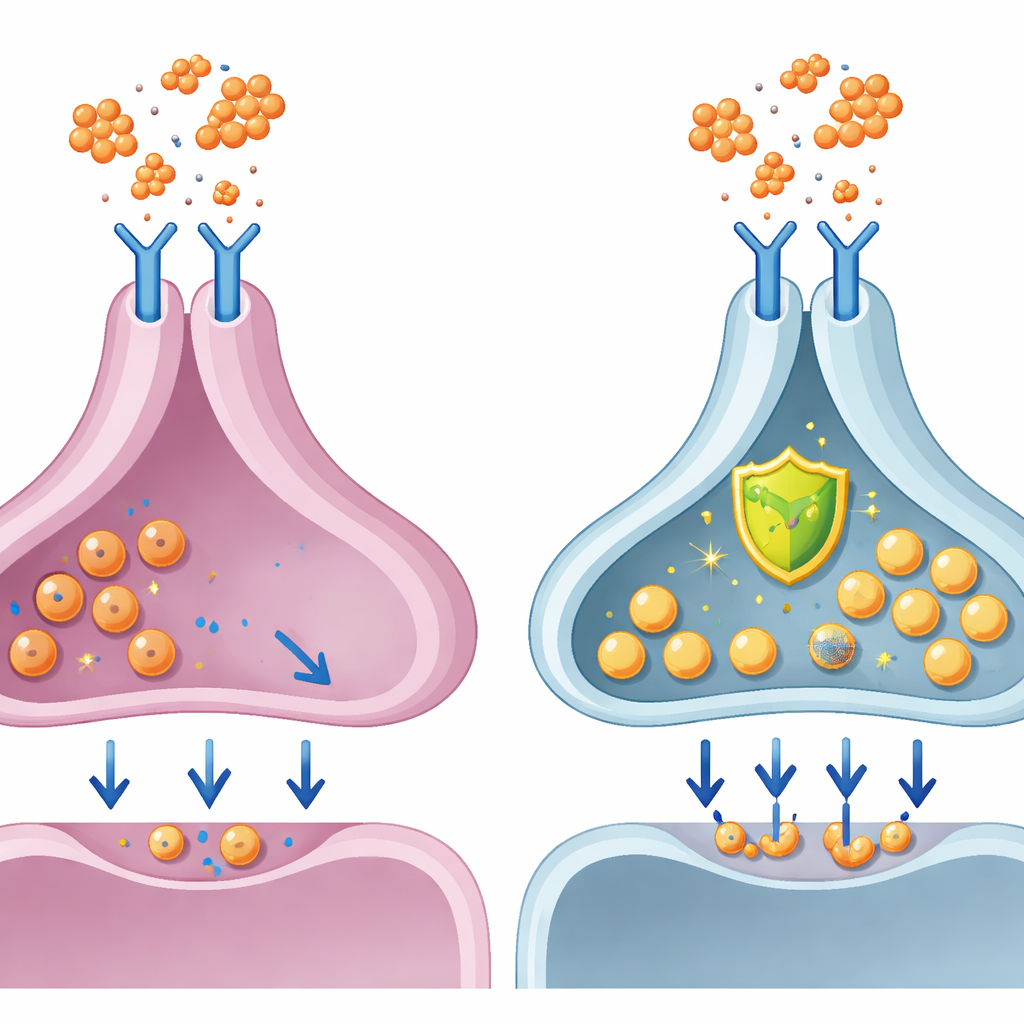
Blokowanie szkodliwej ścieżki
Ponieważ interleukina‑6 sygnalizuje poprzez dobrze poznany łańcuch białek zwany szlakiem JAK‑STAT, naukowcy sprawdzili, czy istniejący lek blokujący tę trasę może chronić neurony dopaminowe. Dodali baricytynib, inhibitor JAK już zatwierdzony do chorób zapalnych, wraz z interleukiną‑6. W neuronach dopaminowych pochodzenia żeńskiego baricytynib w dużej mierze odwrócił spadek uwalniania dopaminy, spowolnienie aktywności elektrycznej i problemy z pęcherzykami synaptycznymi. Sugeruje to, że ukierunkowanie tej ścieżki może bezpośrednio chronić ludzkie komórki dopaminowe przed dysfunkcją wywołaną zapaleniem, przynajmniej in vitro, i może pomóc wyjaśnić, dlaczego leki te bywają związane z poprawą nastroju i motywacji u niektórych pacjentów.
Co to oznacza dla osób z depresją
Łącznie praca ta pokazuje, że sygnały zapalne mogą osłabiać ludzkie neurony dopaminowe w sposób zależny od płci: neurony żeńskie częściej wykazują bezpośrednie uszkodzenie mechanizmów uwalniania dopaminy, podczas gdy neurony męskie skłaniają się ku zmianom adaptacyjnym pomagającym utrzymać funkcję. Niekodująca RNA MIAT wydaje się być kluczową częścią tej różnicy, a blokowanie sygnalizacji w dół szlaku za pomocą baricytynibu może ratować wrażliwe komórki. Dla pacjentów wyniki te wspierają koncepcję, że terapie ukierunkowane na zapalenie mogą być szczególnie pomocne u osób z depresją i podwyższonymi markerami zapalnymi, oraz że płeć i indywidualne profile molekularne mogą mieć znaczenie przy wyborze takich terapii.
Cytowanie: Huang, Y., Michalski, C., Zhou, Y. et al. Synaptic effects of interleukin-6 on human iPSC-derived dopaminergic neurons. Neuropsychopharmacol. 51, 934–945 (2026). https://doi.org/10.1038/s41386-025-02320-y
Słowa kluczowe: zapalenie i depresja, neurony dopaminowe, różnice płciowe, interleukina‑6, leczenie przeciwzapalne