Clear Sky Science · pl
RO4938581, negatywny modulator allosteryczny GABAA-α5 przywrócił fenotypy behawioralne i EEG w modelu myszy zespołu Dup15q
Dlaczego to badanie mózgu ma znaczenie
Zespół Dup15q to rzadka wada genetyczna, która często prowadzi do autyzmu, napadów oraz poważnych trudności w uczeniu się. Rodziny dysponują niewieloma opcjami poza opieką wspierającą, a brak jest leczenia adresującego zasadniczą biologię choroby. W tym badaniu wykorzystano myszy niosące ten sam dodatkowy fragment DNA co osoby z Dup15q, aby zbadać, co w mózgu idzie nie tak — oraz sprawdzić, czy silnie ukierunkowany, eksperymentalny lek może skorygować ten problem. Praca wskazuje na konkretny typ receptora mózgowego jako obiecujący, możliwy do przetestowania cel dla przyszłych precyzyjnych terapii.
Zbyt dużo hamowania w mózgu
Nasz mózg opiera się na delikatnej równowadze między sygnałami „idź”, które pobudzają neurony, a sygnałami „stop”, które je wyciszają. W zespole Dup15q dochodzi do duplikacji fragmentu chromosomu 15. Ten obszar zawiera trzy geny kodujące elementy kluczowego receptora „stop” w mózgu, zwanego receptorem GABAA, a w szczególności wariant zawierający podjednostkę alfa-5. Naukowcy zaprojektowali myszy z analogiczną duplikacją i stwierdzili, że zwierzęta te wytwarzały około 50% więcej receptorów zawierających alfa-5 w rejonach mózgu ważnych dla pamięci, emocji i ruchu, w tym w hipokampie i korze. Różne metody — od analizy ekspresji genów po obrazowanie receptorów — prowadziły do tego samego wniosku: ten konkretny system hamujący jest w modelu Dup15q nadmiernie rozbudowany.
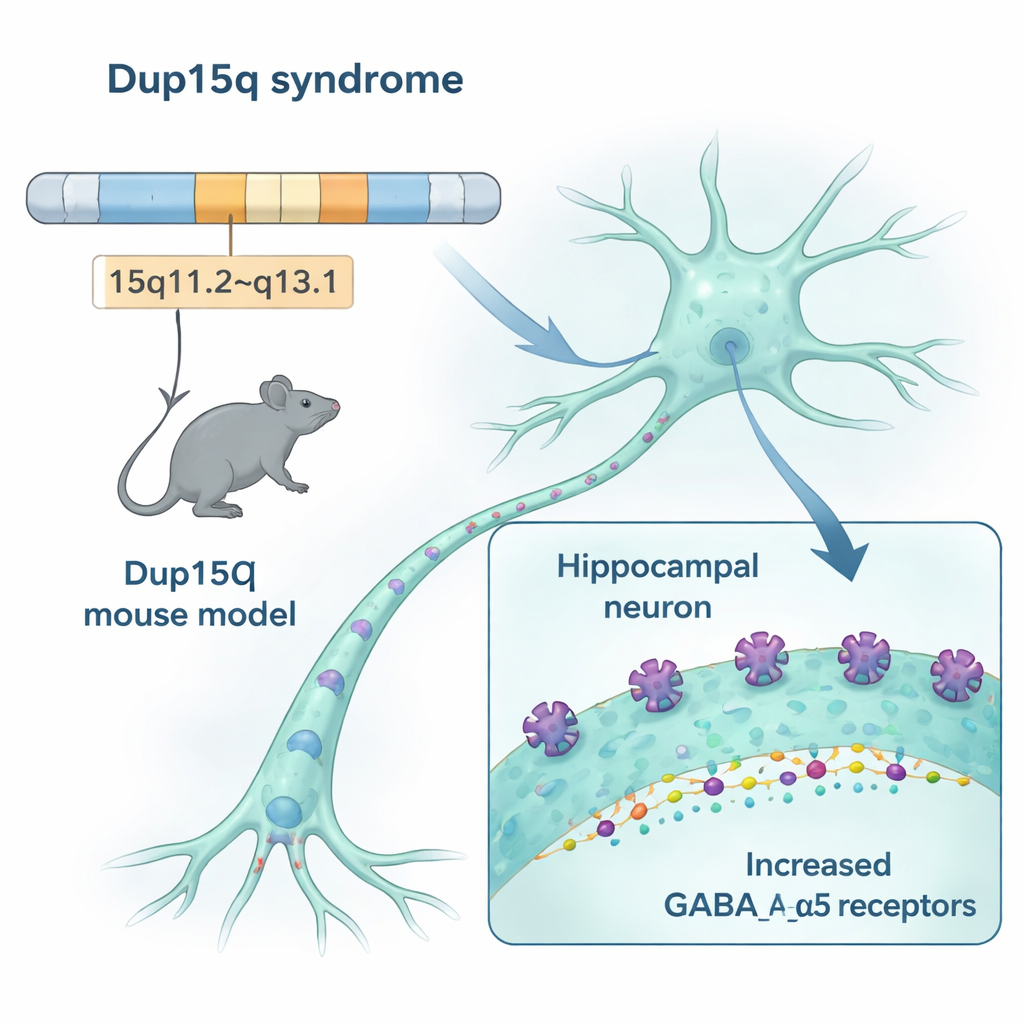
Jak dodatkowe receptory zmieniają sygnały mózgowe
Większa liczba receptorów hamujących ma znaczenie tylko wtedy, gdy rzeczywiście zmienia sposób, w jaki działają obwody. W cienkich preparatach mózgu z hipokampa zespół mierzył drobne prądy elektryczne wysyłane przez neurony hamujące na inne komórki. U myszy z Dup15q te prądy hamujące pojawiały się częściej, co sugeruje, że neurony doświadczały silniejszego, przewlekłego „hamulca”, choć amplituda pojedynczych sygnałów nie uległa zmianie. Osobny test funkcjonowania obwodów, zwany inhibicją par impulsów (paired-pulse inhibition), również pokazał, że sieci u tych myszy były silniej tłumione niż u zdrowych towarzyszy miotu. Razem dane wskazują, że dodatkowe receptory sprawiają, iż obwody hamujące stają się dominujące, przesuwając równowagę z dala od elastycznego przetwarzania informacji.
Behawior i fale mózgowe u dotkniętych myszy
Naukowcy zapytali następnie, czy ta zmieniona „okablowanie” przekłada się na zachowania odzwierciedlające symptomy ludzkie. W serii testów myszy Dup15q wykazywały oznaki różnic w interakcjach społecznych i komunikacji, a najbardziej wyraźnie — trudności z elastycznością poznawczą. W zadaniu labiryntu wodnego zarówno myszy kontrolne, jak i z Dup15q nauczyły się lokalizacji ukrytej platformy. Gdy jednak platformę przesunięto, myszy Dup15q wolniej porzucały starą lokalizację i przystosowywały się do nowej — laboratoryjny odpowiednik sztywnych rutyn często obserwowanych w autyzmie. Zespół zarejestrował również sygnały elektroencefalograficzne (EEG), sumujące rytmy wielu neuronów. Podobnie jak u osób z Dup15q, u myszy obserwowano nadmiernie silną aktywność w paśmie beta, szybki rytm często wzmacniany przez leki potęgujące receptory GABAA, co wzmacniało hipotezę o nadaktywności systemu hamującego.
Ukierunkowany lek, który poluzowuje hamulec
Aby sprawdzić, czy można znormalizować to nadmierne hamowanie, badacze użyli RO4938581, eksperymentalnego związku selektywnie osłabiającego receptory GABAA typu alfa-5 bez wpływu na inne warianty. W preparatach hipokampa lek zmniejszył ilość przenoszonego ładunku hamującego w neuronach Dup15q, przeciwdziałając nadmiarowi hamowania. Podawany doustnie codziennie przez kilka tygodni ten sam związek poprawił wyniki zwierząt w fazie odwrócenia zadania w labiryncie wodnym, pozwalając im przystosować się do przesuniętej platformy bardziej podobnie do myszy zdrowych. Poprawił też ich interakcje społeczne. W zapisie EEG jednorazowa dawka częściowo zredukowała wyolbrzymioną moc beta u myszy Dup15q, przesuwając ich rytmy mózgowe w kierunku typowego wzorca.
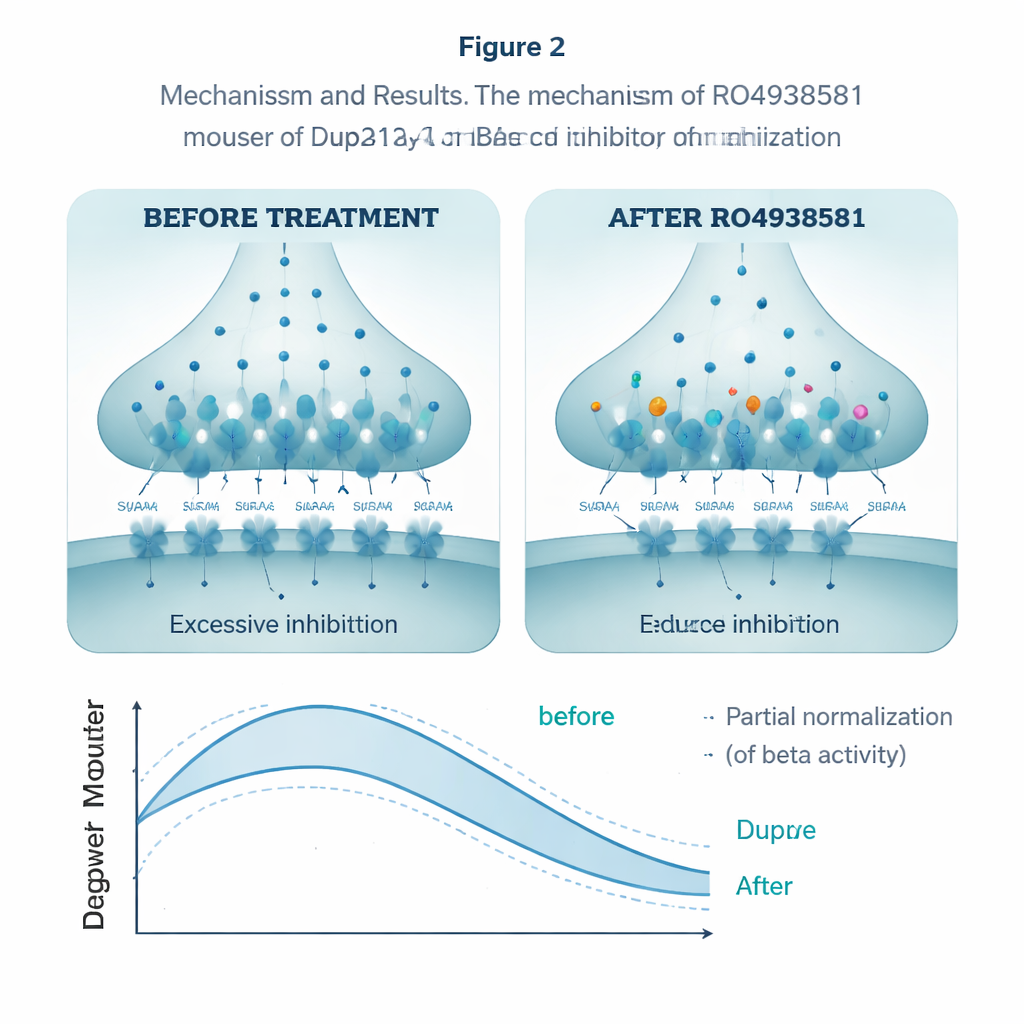
Co to może znaczyć dla przyszłych terapii
Dla rodzin żyjących z zespołem Dup15q te wyniki nie stanowią natychmiastowego lekarstwa, lecz dają konkretny trop. Praca wskazuje na jeden podtyp receptora — receptory GABAA zawierające jednostkę alfa-5 — jako zarówno nadprodukowany, jak i funkcjonalnie istotny w istotnym modelu zwierzęcym. Umiarkowane osłabienie tego receptora przy pomocy negatywnego modulatora, takiego jak RO4938581, nie naprawiło wszystkiego, ale poprawiło elastyczne uczenie się, zachowania społeczne oraz kluczowy biomarker EEG. To połączenie zmian w mózgu, zachowaniu i biomarkerze wzmacnia argument za testowaniem bezpieczniejszych, gotowych dla ludzi leków ukierunkowanych na alfa-5 jako precyzyjnych terapii dla Dup15q, a potencjalnie także pokrewnych zaburzeń neurorozwojowych.
Cytowanie: Nakagawa, R., Nani, F., Hipp, J.F. et al. RO4938581, a GABAA-α5 negative allosteric modulator rescued behavioral and EEG phenotypes of a mouse model of Dup15q syndrome. Mol Psychiatry 31, 1351–1360 (2026). https://doi.org/10.1038/s41380-025-03247-y
Słowa kluczowe: zespół Dup15q, receptor GABAA alfa-5, zaburzenie neurorozwojowe, moc beta w EEG, model myszy