Clear Sky Science · pl
Kaskadowa inercyjna mikrofluidyka do szybkiej, wieloskalowej wzbogacania komórek nowotworowych i nietkniętych skupisk w kierunku lepszej diagnostyki złośliwości
Dlaczego sortowanie komórek nowotworowych w płynach ma znaczenie
Gdy nowotwór się rozsiewa, komórki nowotworowe często przedostają się do płynów otaczających narządy. U osób z rakiem płuca może to obejmować płyn gromadzący się wokół płuc, zwany wysiękiem opłucnowym. Ukryte w tym płynie są rzadkie pojedyncze komórki nowotworowe oraz zwarte skupiska komórek. Uważa się, że te skupiska są szczególnie groźne, ponieważ silnie wiążą się z agresywnym przebiegiem choroby i gorszymi wynikami. Tymczasem obecne metody laboratoryjne mają trudność z delikatnym i wydajnym wyłapywaniem zarówno pojedynczych komórek, jak i skupisk z dużych objętości płynu pacjenta. W badaniu przedstawiono nową technologię opartą na układzie scalonym, która potrafi szybko i ostrożnie separować te komórki z wysięków opłucnowych, otwierając drogę do bardziej wiarygodnej diagnostyki nowotworowej i lepszego zrozumienia mechanizmów rozsiewu nowotworu.
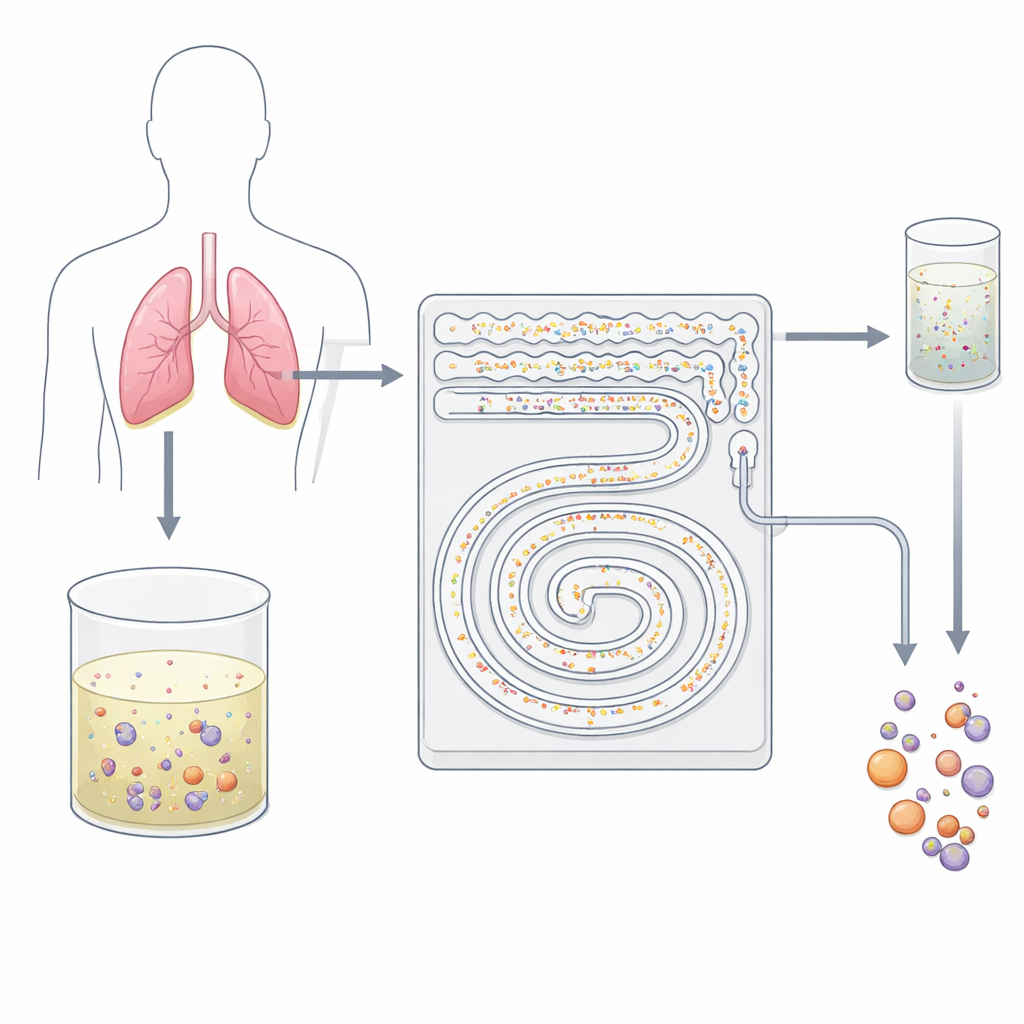
Delikatne sito do komórek na chipie
Naukowcy zaprojektowali plastikowe urządzenie wielkości dłoni, wyżłobione w drobne kanały działające jak inteligentny, dwustopniowy filtr. Zamiast używać lepkich przeciwciał czy agresywnego przesiewania, chip wykorzystuje zachowanie komórek w szybko płynącym płynie. Gdy ciecz przepływa przez zakrzywione mikrokanały, niewidoczne siły przesuwają cząstki o różnych rozmiarach do odmiennych linii przepływu. Zespół wykorzystuje ten efekt, znany ogólnie jako inercyjna mikrofluidyka, do separacji małych komórek krwi od większych komórek nowotworowych i ich skupisk bez dotykania czy znakowania. Ponieważ wszystko dzieje się w ciągłym, zamkniętym przepływie, urządzenie może przetwarzać dziesiątki mililitrów płynu w ciągu kilku minut — coś, czego tradycyjna cytologia na szkiełku nie realizuje łatwo.
Pierwszy etap: oczyszczenie tłumu
W pierwszym etapie urządzenia wysięk opłucnowy — po usunięciu nadmiaru płynu i zawieszeniu komórek — jest napędzany przez układ równoległych, wijących kanałów. Tam wirowy, zakrzywiony przepływ popycha małe białe krwinki ku ściankom kanałów, podczas gdy większe komórki nowotworowe i skupiska pozostają bliżej środka strumienia. Małe komórki kierowane są do odpływów z odpadami, co znacząco rozrzedza tło. Ten etap o dużej przepustowości może działać z szybkością około 8 mililitrów na minutę, co oznacza, że typową próbę kliniczną o objętości 50 mililitrów można przetworzyć w około sześć i pół minuty bez zapychania. To, co wychodzi z pierwszego etapu, to znacznie czystsza mieszanina, wzbogacona w potencjalnie złośliwe komórki i gotowa do dokładniejszej separacji.
Drugi etap: rozdzielenie pojedynczych komórek od skupisk
Częściowo wzbogacona próbka trafia następnie do ukośnie ułożonego kanału spiralnego, który zawiera powtarzający się wzór wąskich i szerokich sekcji. W tym etapie kilka sił przepływowych równoważy się w różny sposób dla obiektów o różnych rozmiarach, kierując je do odmiennych pasów w pobliżu wewnętrznej lub zewnętrznej ścianki spirali. Pojedyncze komórki przypominające nowotworowe, które są mniejsze, ustawiają się w jednej pozycji bocznej, podczas gdy masywniejsze skupiska przemieszczają się do innej pozycji bliżej wewnętrznej ścianki. Poprzez umieszczenie odpływów w odpowiednich miejscach, chip fizycznie dzieli te strumienie: jeden odpływ zbiera głównie pojedyncze komórki nowotworowe, inny zbiera nietknięte skupiska, a kolejne odpływy usuwają pozostałe małe komórki. Co ważne, skupiska pozostają w całości, unikając uszkodzeń i rozpadu często obserwowanych przy tradycyjnych metodach filtracji.
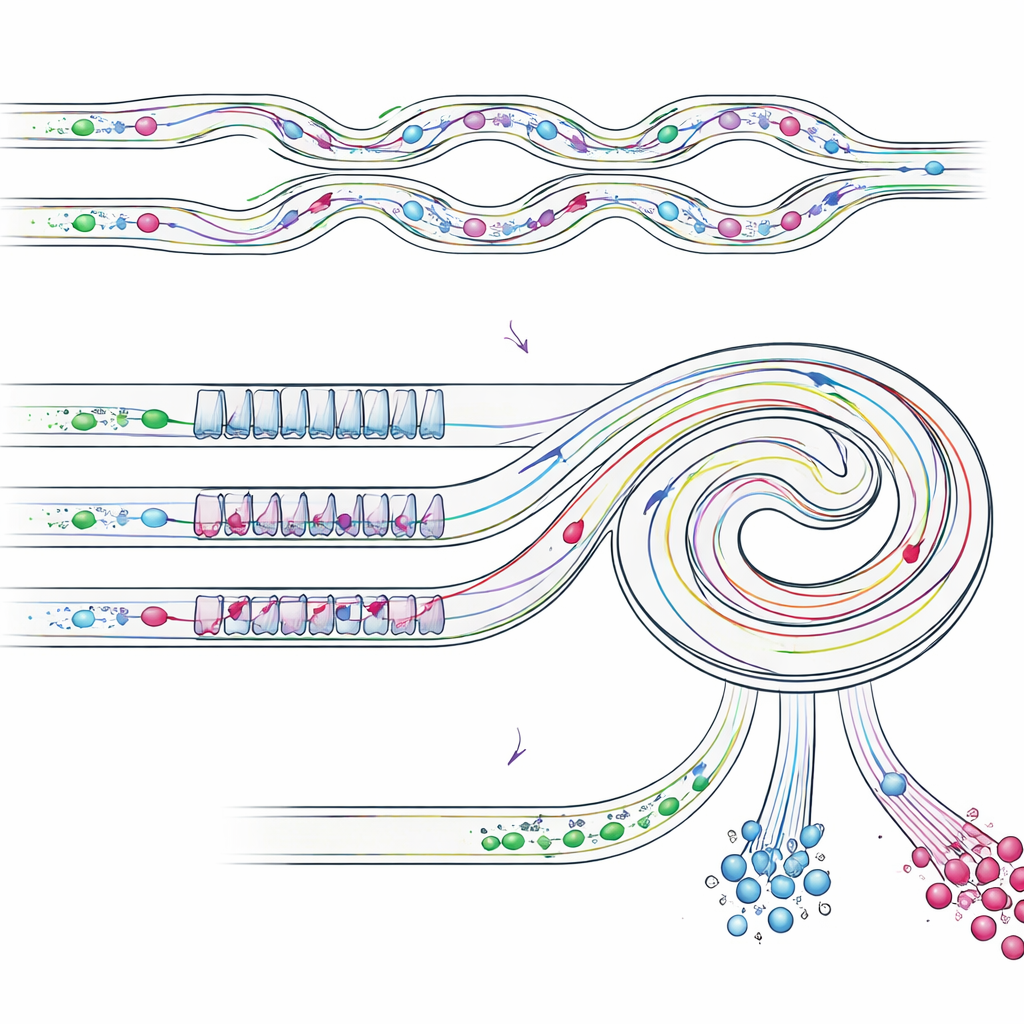
Testy urządzenia
Aby sprawdzić skuteczność projektu, zespół najpierw użył plastikowych kulek o znanych rozmiarach, aby naśladować komórki krwi, pojedyncze komórki nowotworowe i skupiska. Wykazali, że kaskadowy chip odzyskiwał ponad 87% kulek „pojedynczych komórek” oraz około 92% kulek „skupisk”, jednocześnie usuwając większość mniejszych kulek „komórek krwi”. Następnie przeszli do prawdziwych komórek raka płuca (komórki A549) zmieszanych z białymi krwinkami. W tych testach urządzenie odzyskało około 82% komórek nowotworowych ogółem, z około 76% czystością we wzbogaconej frakcji i niemal 80% czystością dla skupisk komórkowych. Wreszcie przetworzyli rzeczywiste próbki wysięku opłucnowego od trzech pacjentów z rakiem płuca. Zaczynając od płynu, w którym komórki nowotworowe i skupiska stanowiły mniej niż 1% wszystkich komórek, chip wyprodukował frakcje, w których pojedyncze komórki złośliwe stanowiły około 68% wszystkich komórek, a skupiska stanowiły około 35% komórek w dedykowanym strumieniu odpływowym.
Co to może oznaczać dla pacjentów
Wykorzystując jedynie przepływ płynu i geometrię kanałów, to urządzenie może szybko i delikatnie wyłapać zarówno pojedyncze komórki nowotworowe, jak i nietknięte skupiska z dużych objętości płynu pacjenta bez chemicznych znaczników czy skomplikowanych instrumentów. Wzbogacone komórki nadają się do standardowych testów, takich jak barwienie immunofluorescencyjne i mikroskopia, co pozwala na płynną integrację z istniejącymi procedurami szpitalnymi. Chociaż obecne badanie obejmowało małą liczbę pacjentów i wymaga większych prób, by potwierdzić wpływ na diagnostykę i rokowanie, praca demonstruje silną koncepcję: szybkie, bezznakowe „koncentrator komórek”, który ujawnia zarówno liczbę, jak i stan skupiskowy komórek nowotworowych w wysiękach opłucnowych. W perspektywie długoterminowej takie narzędzia mogą uszczegółowić ocenę złośliwości, wspierać dobór spersonalizowanego leczenia i oferować jaśniejsze okno na mechanizmy przerzutowania nowotworów.
Cytowanie: Zhu, Z., Ren, H., Zhang, Z. et al. Cascading inertial microfluidics for high-throughput, multi-scale enrichment of tumor cells and intact clusters towards enhanced malignancy diagnosis. Microsyst Nanoeng 12, 101 (2026). https://doi.org/10.1038/s41378-026-01235-y
Słowa kluczowe: płynna biopsja, mikrofluidyczne sortowanie komórek, skupiska komórek nowotworowych, wysięk opłucnowy, diagnostyka raka