Clear Sky Science · pl
Projekt zautomatyzowanego systemu wsadowej mikroiniekcji komórek opartego na pęsetach magnetycznych dla embrionów danio pręgowanego
Dlaczego małe jajeczka ryb są istotne
Zanim nowe leki lub terapie genowe trafią do ludzi, naukowcy często testują je na małych, szybko rosnących zwierzętach. Embriony danio pręgowanego są chętnie wybierane, ponieważ są przejrzyste i rozwijają się szybko, co pozwala badaczom obserwować tworzenie się organów w czasie rzeczywistym. Aby jednak zmieniać ich geny lub dostarczać leki, trzeba wstrzyknąć każde delikatne jajeczko mikroskopijną igłą — zadanie zwykle powolne, męczące i silnie zależne od umiejętności operatora. Artykuł przedstawia nowy system robotyczny, który potrafi automatycznie wstrzykiwać partie embrionów danio szybciej, delikatniej i bardziej niezawodnie niż człowiek, otwierając drogę do większych i bardziej spójnych eksperymentów.
Nowy sposób obchodzenia się z kruchymi komórkami
Tradycyjna mikroiniekcja wymaga wyszkolonego operatora, który pod mikroskopem manewruje szklaną igłą, lokalizuje każdy embrion, ustawia go we właściwej orientacji i przebija bez uszkadzania kluczowych struktur. To szczególnie trudne, bo embriony są miękkimi sferami z ważnymi obszarami, których należy unikać, by utrzymać je przy życiu. Istniejące systemy robotyczne pomogły zautomatyzować transport i przebijanie, ale zazwyczaj nie potrafią kontrolować rotacji każdego embrionu w trzech wymiarach. W efekcie igła może wejść pod ryzykownym kątem, co obniża wskaźniki przeżywalności i ogranicza liczbę embrionów, które można bezpiecznie przetworzyć. Zespół autorów postanowił zbudować w pełni zintegrowaną platformę, która w płynnym ciągu operacji będzie transportować, obracać, wstrzykiwać i uwalniać embriony bez konieczności częstych zmian obiektywu czy ręcznych regulacji.
Magnesy, mikrokanaliki i delikatna kontrola
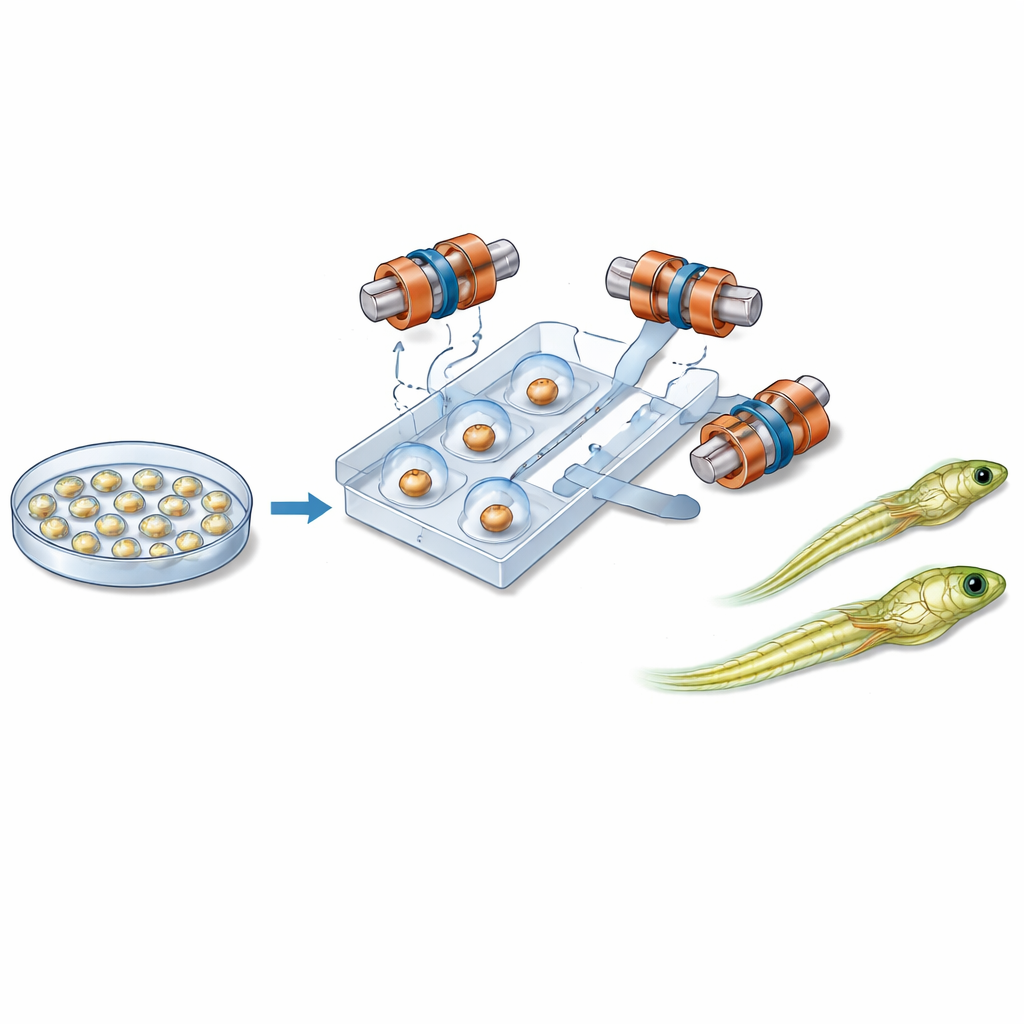
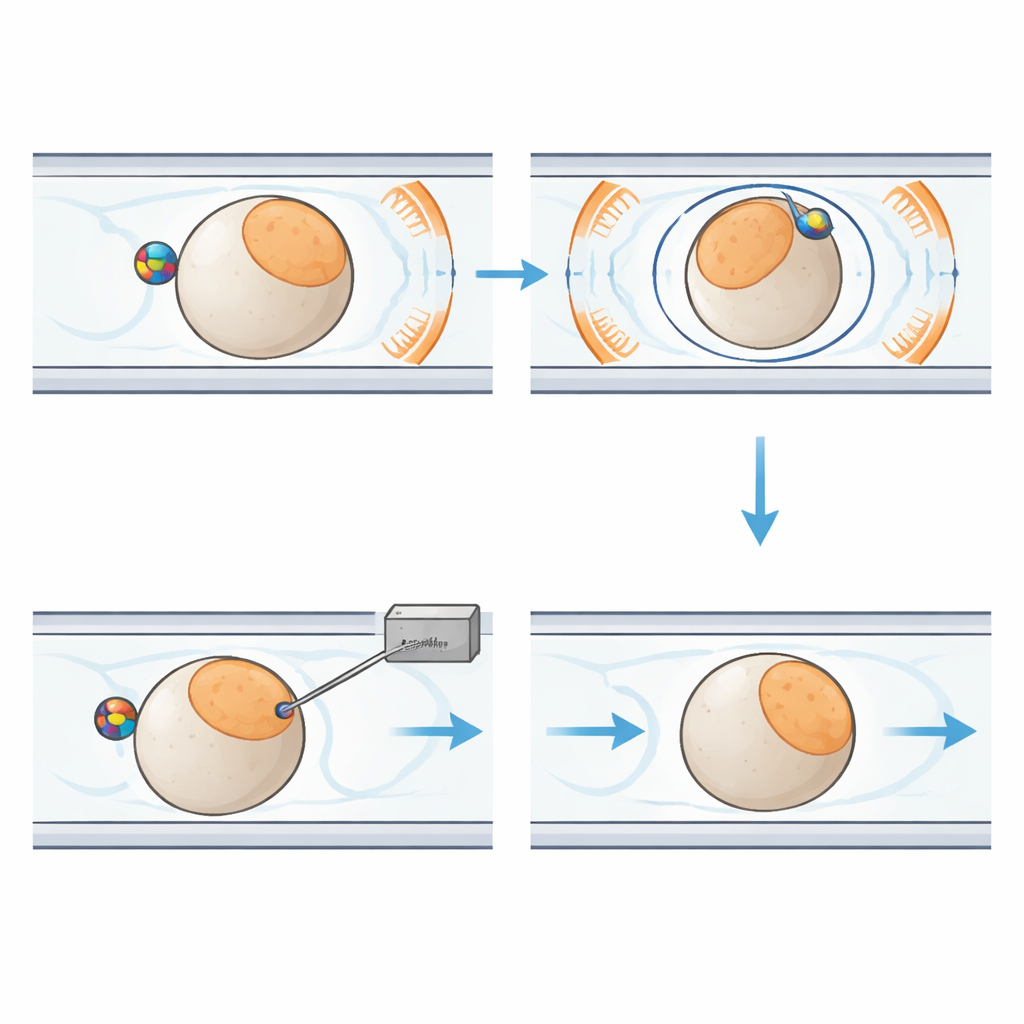
Rdzeniem nowego systemu jest plastikowy chip wielkości dłoni zawierający wąskie kanały, które prowadzą pojedyncze embriony po ustalonej ścieżce. Obok każdego embrionu znajduje się mała magnetyczna kulka. Wokół chipu umieszczono sześć precyzyjnie rozmieszczonych cewek generujących jednorodne pole magnetyczne w trzech wymiarach. Zmieniając w czasie kierunek tego pola, system wprawia kulkę w obrót. Dzięki tarciu między kulką a powierzchnią embrionu cała komórka obraca się razem z nią, jak dwa zazębiające się tryby. Pozwala to robotowi przechylić embrion poza płaszczyznę obrazu lub obracać go w jej obrębie, aż wrażliwy obszar znajdzie się bezpiecznie poza drogą nadchodzącej igły. Ciecz i delikatne ciśnienie powietrza przesuwają i przytrzymują embriony, podczas gdy osobny moduł steruje igłą iniekcyjną i mikroskopijnym przepływem materiału genetycznego.
Wyraźne widzenie na małym polu widzenia
Aby umożliwić tę precyzyjną choreografię, badacze zaprojektowali także zaawansowany system widzenia komputerowego, nazwany microscopic manipulation perception network. Analizuje on obrazy z kamery mikroskopowej w czasie rzeczywistym, aby wykrywać każdy embrion, lokalizować cienki koniec igły i rozróżniać dwa przeciwne „bieguna” jajeczka, gdzie leżą kluczowe struktury rozwojowe. Sieć wykorzystuje nowoczesne techniki głębokiego uczenia — takie jak podwójne ścieżki ekstrakcji cech, moduły uwagi podkreślające istotne detale oraz wieloskalowe łączenie informacji obrazowej — aby radzić sobie z zatłoczonym, słabo oświetlonym środowiskiem wewnątrz mikrofluidycznego chipu. W testach na tysiącach obrazów poprawnie wykrywała obiekty i segmentowała obszary embrionów z dokładnością około 98–99%, dostarczając niezawodnego sprzężenia zwrotnego potrzebnego do sterowania zarówno magnetyczną rotacją, jak i pozycjonowaniem igły.
Potwierdzenie działania na żywych danio
Zespół porównał swój zautomatyzowany system z doświadczonymi operatorami używając po 100 embrionów danio na stronę. Robot wykonał iniekcje w około 33,8 sekundy na embrion, ponad dwa razy szybciej niż praca ręczna, i skutecznie nakłuł każdą komórkę. Ustawił też każdy embrion z średnim błędem kątowym zaledwie 2,1 stopnia, czyli mniej więcej o połowę mniejszym niż operatorzy ludzie. Co najważniejsze, 88% embrionów wstrzykniętych przez robota przeżyło do wyklucia jako larwy, w porównaniu z 66% po iniekcji ręcznej. Pod mikroskopem fluorescencyjnym larwy z systemu zautomatyzowanego świeciły na zielono, co pokazało, że wprowadzony materiał genetyczny został przyjęty i wyrażony zgodnie z planem. Obracając embriony magnetycznie zamiast ściskać je narzędziami mechanicznymi, system zminimalizował odkształcenia i uszkodzenia przy utrzymaniu wysokiej wydajności przetwarzania.
Co to oznacza dla przyszłych badań
W praktyce praca ta pokazuje, że starannie zaprojektowane połączenie mikrokanalików, kontroli magnetycznej i inteligentnej analizy obrazu może wstrzykiwać delikatne embriony ryb szybciej i z lepszym wskaźnikiem przeżywalności niż wykwalifikowana osoba używająca tradycyjnych narzędzi. Ponieważ danio pręgowany są kluczową platformą do badania rozwoju, chorób i działania leków, niezawodny, wysokoprzepustowy injector mógłby przyspieszyć duże przeszukiwania genetyczne i długoterminowe badania biologiczne, wcześniej ograniczone pracą ręczną. Przy odpowiednich zmianach w konstrukcji chipu i ustawieniach sterowania ta sama strategia mogłaby zostać zaadaptowana do innych typów komórek i małych organizmów, pomagając przekształcić delikatne zabiegi komórkowe z rzemiosła kilku specjalistów w zautomatyzowany, standaryzowany proces.
Cytowanie: Guo, X., Wang, F., Zhao, A. et al. Design of an automated cell batch microinjection system based on magnetic tweezers for zebrafish embryos. Microsyst Nanoeng 12, 113 (2026). https://doi.org/10.1038/s41378-026-01230-3
Słowa kluczowe: embriony danio pręgowanego, mikroiniekcja, pęsety magnetyczne, mikroprzepływy, robotyczna manipulacja komórkami