Clear Sky Science · pl
PEGylowane nanoschematy Cu-dopowane WS2 do celowanej multimodalnej terapii nowotworowej
Dlaczego inteligentniejsze terapie nowotworowe mają znaczenie
Wiele osób z rakiem piersi nadal doświadcza surowych metod leczenia, które mogą uszkadzać zdrowe tkanki, nie zatrzymując jednocześnie w pełni guza. W tym badaniu opisano nowy rodzaj drobnych, zaprojektowanych arkuszy — tak małych, że niewidocznych gołym okiem — przeznaczonych do przemieszczania się po ciele, lokalizowania guzów piersi i atakowania ich kilkoma skoordynowanymi mechanizmami jednocześnie. Poprzez połączenie ciepła, reakcji chemicznych i klasycznego leku przeciwnowotworowego w jednym, ukierunkowanym nośniku, badacze dążą do uczynienia terapii zarówno bardziej skuteczną, jak i mniej szkodliwą dla reszty organizmu. 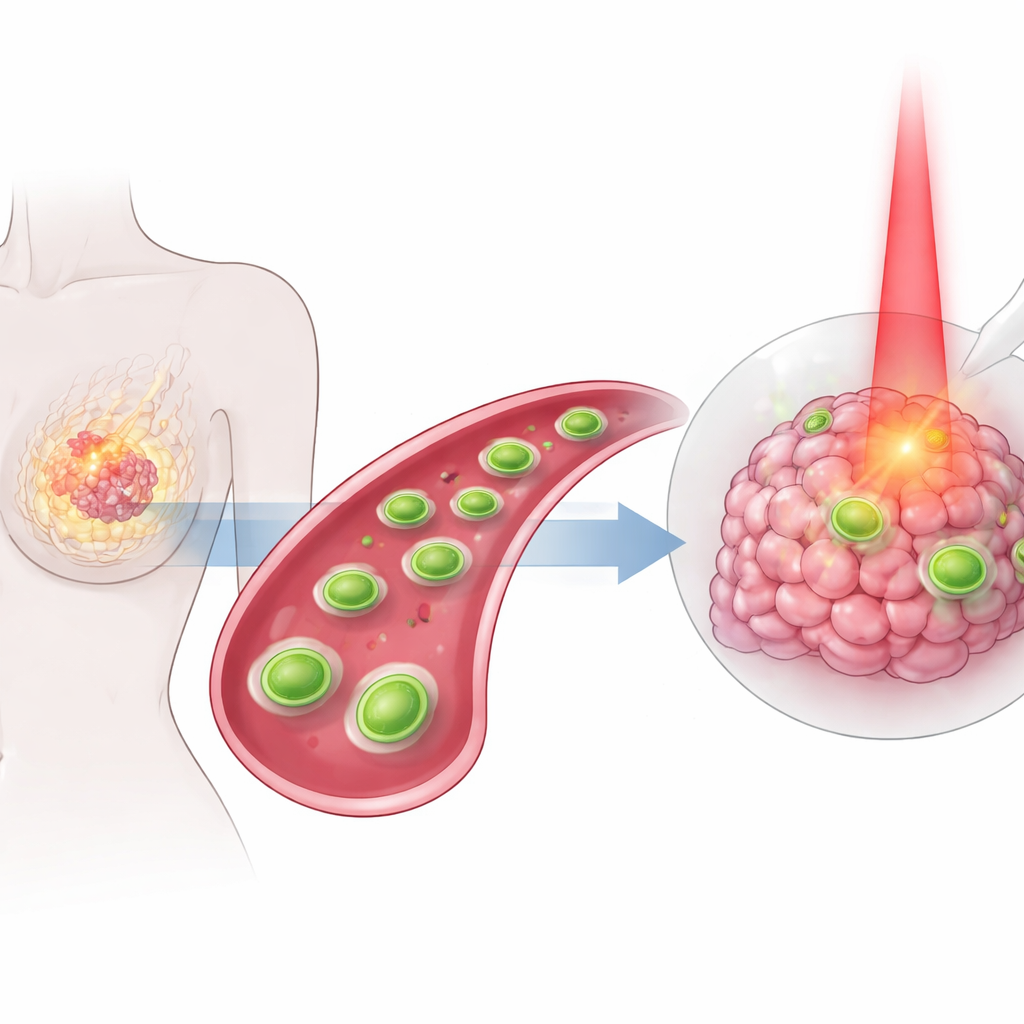
Drobne arkusze zaprojektowane do przenoszenia i uwalniania terapii
Rdzeń podejścia stanowi ultracienki materiał złożony z wolframu i siarki, uformowany w nanoskopijne arkusze. Arkusze te naturalnie absorbują światło bliskiej podczerwieni i zamieniają je na ciepło. Zespół najpierw wytworzył te arkusze, a następnie celowo zgrubiał ich powierzchnię, aby mogły utrzymywać inne użyteczne składniki. Atomy miedzi zostały zakotwiczone na arkuszach w silnie zdyspergowany sposób, a nałożono miękką, elastyczną powłokę przypominającą molekularny „płaszcz”, która pomaga cząstkom dobrze mieszać się w płynach ustrojowych i unikać aglomeracji. Na końcu przyłączono kwas foliowy — witaminę, którą wiele komórek nowotworowych intensywnie pobiera — jako urządzenie celujące, i załadowano powierzchnię popularnym lekiem chemioterapeutycznym doksorubicyną. Efekt końcowy to maleńka, warstwowa platforma, która może krążyć we krwi, rozpoznawać komórki guza i przenosić znaczną porcję terapii.
Jak światło, chemia i lek współdziałają
Gdy te cząstki dotrą do guza, dzieje się kilka rzeczy równocześnie. Po naświetleniu obszaru guza łagodnym czerwonym laserem arkusze wolframowo-siarkowe wydajnie się nagrzewają, podnosząc lokalną temperaturę na tyle, by stresować i uszkadzać komórki nowotworowe, nie przegrzewając reszty organizmu. Równocześnie atomy miedzi na arkuszach reagują z naturalnymi cząsteczkami nadtlenku, które występują w wyższych stężeniach w guzach. Ta reakcja przekształca nadtlenek w bardzo reaktywne, krótkotrwałe utleniacze, które uszkadzają składniki komórkowe od środka. Guzy zwykle mają też nieco bardziej kwaśne środowisko niż zdrowa tkanka; w tym „ostrzejszym” środowisku, oraz pod wpływem nagrzewania laserem, wiązanie między arkuszem a doksorubicyną osłabia się, co pozwala uwalniać więcej leku dokładnie tam, gdzie jest potrzeba. Te trzy efekty — ciepło, atak chemiczny i skupiona chemioterapia — zostały zaprojektowane tak, by wzajemnie się wzmacniać. 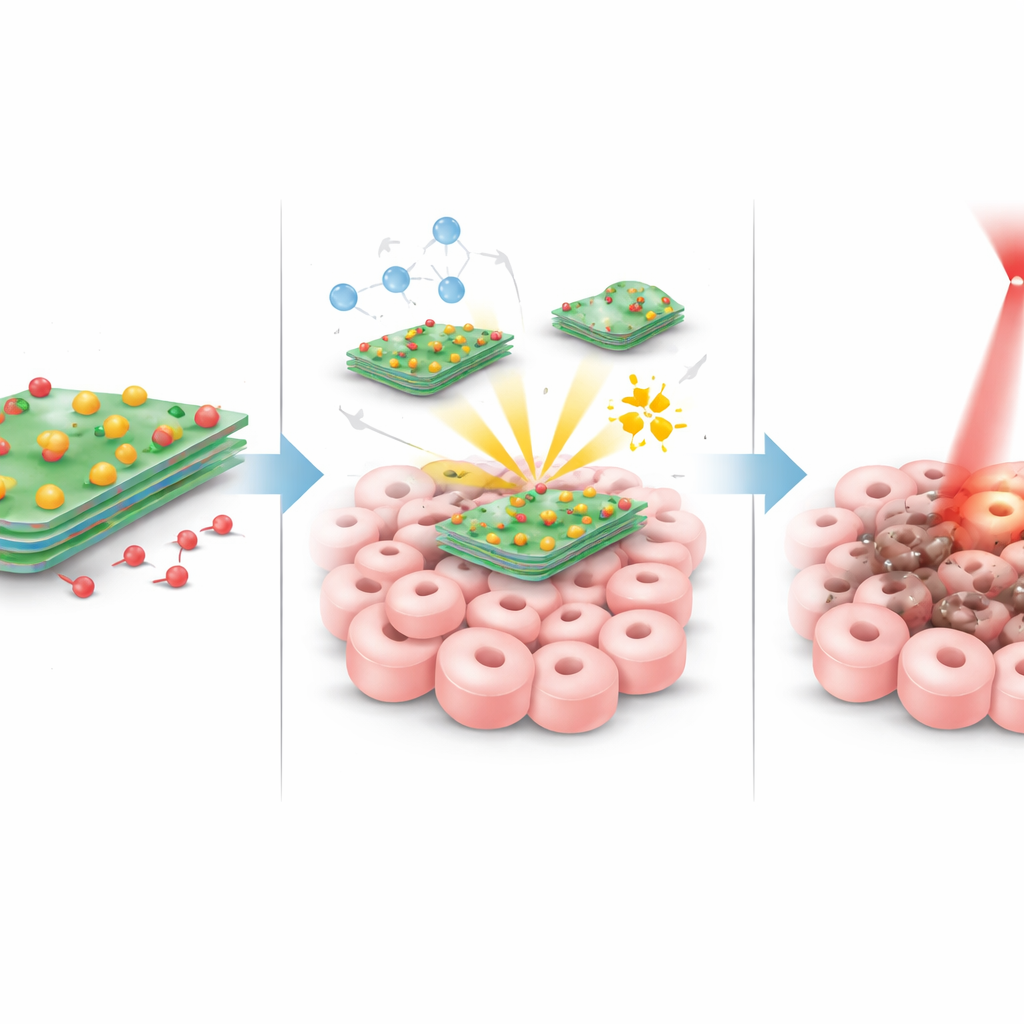
Dane z badań komórkowych i z myszy z guzami
W hodowlach komórkowych powlekane arkusze same w sobie wykazywały niewielką szkodliwość dla komórek prawidłowych, co sugeruje dobrą podstawową tolerancję. Jednak po załadowaniu doksorubicyną i wystawieniu na światło lasera w obecności nadtlenku powodowały silne obumieranie komórek raka piersi, znacznie większe niż jakiekolwiek pojedyncze leczenie. Badacze wykazali również, że cząstki generują wyrzut reaktywnych utleniaczy wewnątrz komórek guza, potwierdzając aktywność chemii miedzi. U myszy z guzami piersiowymi cząstki z powłoką z kwasu foliowego kumulowały się znacznie silniej i dłużej w tkance guza niż cząstki nieukierunkowane. Gdy myszy otrzymały pełne połączenie — cząstki celowane plus naświetlanie czerwonym światłem — ich guzy znacznie się zmniejszyły, czas przeżycia się wydłużył, a masa ciała i zdrowie narządów pozostały w dużej mierze normalne, co wskazuje na ograniczone skutki uboczne w porównaniu ze standardowym leczeniem lekowym.
Co to może znaczyć dla przyszłej opieki onkologicznej
Łącznie wyniki sugerują, że te zaprojektowane arkusze działają jak wielofunkcyjne narzędzie do terapii nowotworowej: wyszukują guzy, je nagrzewają, zatruwają od wewnątrz za pomocą reaktywnej chemii i dostarczają sprawdzony lek bardziej precyzyjnie, oszczędzając przy tym dużą część reszty organizmu. Prace są wciąż na etapie badań na zwierzętach, a ważne pytania pozostają dotyczące długoterminowego bezpieczeństwa, rozkładu i optymalnej produkcji takich cząstek do zastosowań u ludzi. Jednak projekt pokazuje, jak połączenie kilku umiarkowanych terapii w jednym inteligentnym opakowaniu dostosowanym do środowiska guza może dać znacznie silniejszy efekt ogólny. Jeśli przyszłe badania potwierdzą ich bezpieczeństwo i skuteczność, takie wielofunkcyjne nanoplatformy mogą uczynić terapię raka piersi bardziej ukierunkowaną, wydajną i mniej obciążającą dla pacjentów.
Cytowanie: Li, D., Wen, C., Wu, H. et al. PEGylated Cu-doped WS2 hybrid nanosheets for targeted multimodal cancer therapy. Microsyst Nanoeng 12, 121 (2026). https://doi.org/10.1038/s41378-026-01218-z
Słowa kluczowe: terapia raka piersi, nanomedycyna, leczenie fototermiczne, celowane dostarczanie leków, terapia chemodynamiczna