Clear Sky Science · pl
Robotyczny system transportu komórek oparty na modelowaniu oporu mikropipety
Przenoszenie maleńkich komórek bez mikroskopu
Współczesna biologia często opiera się na zaskakująco prostej czynności: podniesieniu pojedynczej komórki szklaną rurką i umieszczeniu jej w innym miejscu. Jest to niezbędne przy zabiegach rozrodczych, zamrażaniu embrionów, terapiach opartych na komórkach oraz w badaniach podstawowych. Dziś zazwyczaj wymaga to masywnego mikroskopu i wysoko wykwalifikowanego operatora monitorującego każdy ruch. Artykuł opisuje nowy system robotyczny, który potrafi przenosić pojedyncze komórki między kroplami cieczy bez jakiegokolwiek obrazu mikroskopowego, otwierając drogę do w pełni zamkniętych, zautomatyzowanych „fabryk komórek”, które mogą działać szybciej, taniej i z mniejszym uszkodzeniem delikatnych komórek.
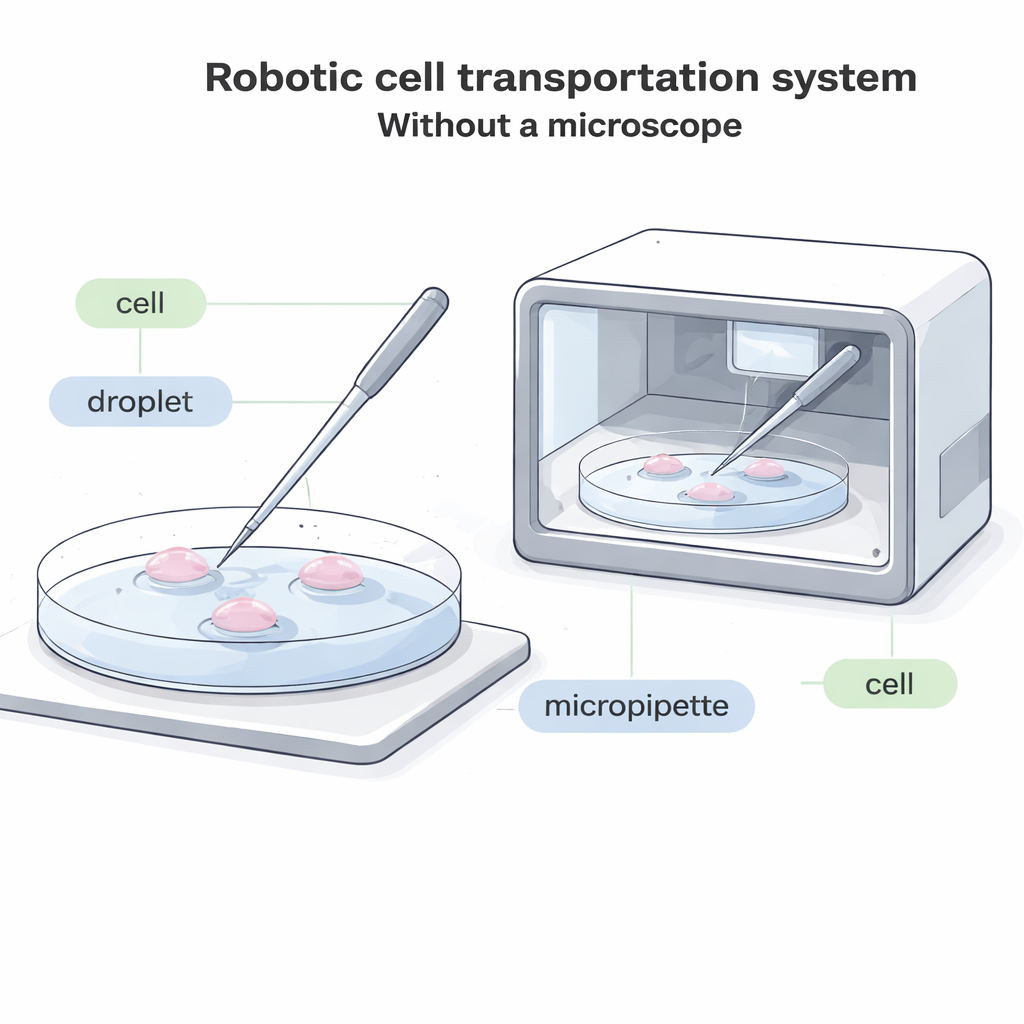
Dlaczego manipulacja komórkami wymaga przemodelowania
W typowych laboratoriach operator patrzy przez mikroskop i używa cienkiej szklanej rurki, zwanej mikropipetą, aby opaść na dno naczynia, delikatnie zassać jedną komórkę, przenieść ją do nowej kropli płynu, a następnie wypchnąć. Proces ten jest wolny, wizualnie wymagający i trudny do zautomatyzowania. W wielu przyszłych systemach — na przykład kompaktowych, zamkniętych urządzeniach hodujących embriony lub inne komórki w szczelnym pudełku — po prostu nie ma miejsca na tradycyjny mikroskop. W innych przypadkach komórki są znakowane świecącymi barwnikami, które mogą blaknąć lub ulegać uszkodzeniu pod wpływem światła, więc ograniczenie intensywnej obserwacji mikroskopowej jest istotne. Istniejące systemy „na ślepo”, które nie opierają się na obrazach, działają jedynie dla wyjątkowo dużych komórek, pozostawiając większość powszechnych typów komórek bez dobrego zautomatyzowanego rozwiązania.
Szczególna słomka z wbudowanym ogranicznikiem
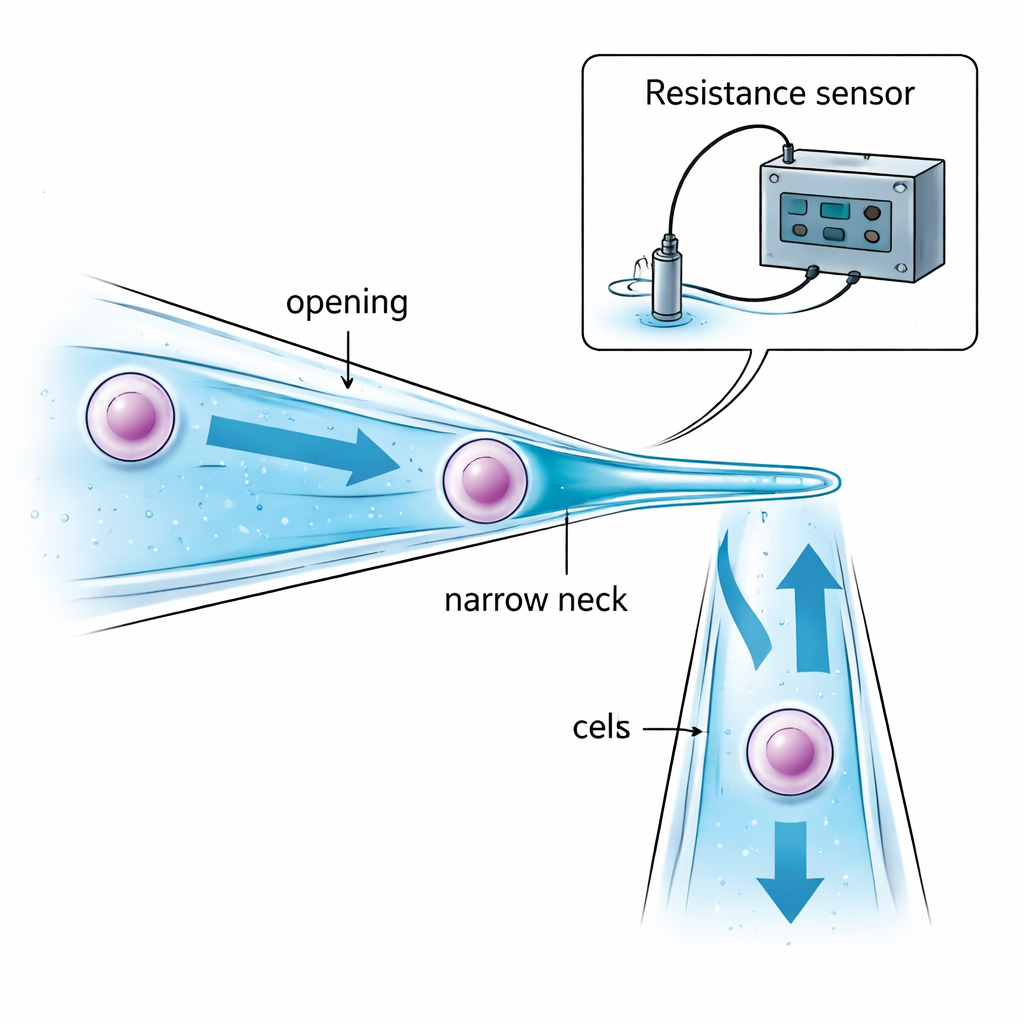
Autorzy rozwiązują problem przez przeprojektowanie samej mikropipety. Zamiast prostej szklanej rurki o jednakowej średnicy tworzą mikropipetę z wąską szyjką. Jej ujście jest nieco większe niż docelowa komórka, tak by komórka mogła być wciągnięta do środka. Głębiej w rurce jej przekrój stopniowo zmniejsza się do „szyjki”, która jest mniejsza niż komórka. Gdy ssanie ciągnie komórkę w stronę tego zwężenia, komórka zostaje zatrzymana i trzymana wewnątrz rurki — zamiast wisieć na końcu i być wystawioną na kontakt z olejem lub powietrzem między kroplami. Staranny dobór rozmiaru ujścia, rozmiaru szyjki i odległości między nimi zapewnia, że komórka może być pewnie schwytana bez nadmiernego ściskania, a także że przenoszona jest tylko niewielka objętość cieczy z jednej kropli do drugiej, co redukuje zanieczyszczenie.
Słuchanie sygnałów elektrycznych zamiast patrzenia
Bez mikroskopu robot nadal musi wiedzieć trzy rzeczy: kiedy szklany koniec jest dostatecznie blisko dna naczynia, kiedy komórka została pomyślnie złapana w szyjce i kiedy została w pełni uwolniona w nowej kropli. Zespół rozwiązuje to przez monitorowanie drobnych zmian w oporze elektrycznym cieczy wewnątrz i wokół mikropipety. W miarę jak skośna pipeta zbliża się do dna naczynia, szczelina cieczy między nimi maleje, a opór elektryczny wzrasta w przewidywalny sposób, sygnalizując bezpieczne lądowanie tuż przed kontaktem. Gdy komórka blokuje wąską szyjkę, droga elektryczna przez ciecz jest zacieśniona i opór nagle skacze; gdy komórka jest wypychana, opór spada równie gwałtownie. Modele matematyczne tych oporów: „szczeliny”, „zasysania” i „wtrysku” pozwalają komputerowi interpretować te sygnały w czasie rzeczywistym i decydować, kiedy zatrzymać ssanie lub nacisk, wszystko bez informacji wzrokowej.
Testy robota
Aby sprawdzić skuteczność podejścia w praktyce, badacze zbudowali pełny układ robotyczny łączący kontrolę ruchu, kontrolę ciśnienia, pomiar oporu i komputer główny. Testowali go na małych komórkach nowotworowych znanych jako komórki HeLa (około 10 mikrometrów średnicy) oraz na znacznie większych żeńskich komórkach świni (około 150 mikrometrów). System był w stanie wiarygodnie wykrywać lądowanie, chwyt i uwolnienie wyłącznie na podstawie sygnałów oporu dla szerokiego zakresu rozmiarów pipet. W bezpośrednich porównaniach robot przenosił komórki HeLa z 90-procentową skutecznością — lepiej niż wcześniejsza metoda z wykorzystaniem obrazu — i transportował komórki jajowe świni z 95-procentową skutecznością, przewyższając standardowe podejście mikroskopowe. Czas operacji na komórkę był porównywalny lub krótszy niż w metodach sterowanych przez ludzi, głównie dlatego, że wąska szyjka eliminuje potrzebę wielokrotnego precyzyjnego dostrajania ssania w celu ustawienia komórki.
Utrzymywanie komórek przy życiu i skalowanie
Każdy robot pomocniczy w laboratorium biologicznym musi unikać uszkadzania obsługiwanych komórek. Po transporcie za pomocą nowego systemu zarówno komórki HeLa, jak i komórki jajowe świni były hodowane przez dzień i barwione barwnikiem, który świeci tylko w żywych komórkach. Wskaźniki przeżywalności dla nowej metody były porównywalne lub bliskie wynikom transferu prowadzonego tradycyjnie pod mikroskopem oraz komórek kontrolnych bez manipulacji, co wskazuje, że delikatne mechaniczne ściskanie w wąskiej szyjce nie obniża zauważalnie żywotności komórek, gdy progi są prawidłowo ustawione. Patrząc w przyszłość, autorzy sugerują, że to samo czujnikowanie oparte na oporze i kontrola ciśnienia mogą zostać wbudowane w kompaktowe chipy mikroprzepływowe. Pozwoliłoby to wielu kanałom działać równolegle, umożliwiając wysokoprzepustowe, w pełni zamknięte systemy obsługi komórek odpowiednie do zautomatyzowanej medycyny rozrodczej, terapii komórkowych i długoterminowych urządzeń do hodowli komórek, gdzie mikroskopy trudniej zastosować.
Co to oznacza dla przyszłej pracy z komórkami
Dla niespecjalistów główny przekaz jest taki, że przenoszenie pojedynczych komórek nie musi już zależeć od osoby obserwującej przez mikroskop. Poprzez staranne ukształtowanie szklanej rurki i „słuchanie”, jak prąd przepływa przez otaczającą ciecz, robot może wyczuć, kiedy wylądował, złapał komórkę i ją uwolnił — wszystko w ciemności i w ciasnych przestrzeniach. Ułatwia to projektowanie zamkniętych, samodzielnie działających systemów hodowli komórek, które chronią delikatne próbki, upraszczają procedury kliniczne i zbliżają manipulacje komórkowe o jakości laboratoryjnej do zautomatyzowanej, fabrycznej pracy.
Cytowanie: Zhao, Q., Liu, M., Zhu, R. et al. Robotic cell transportation system based on micropipette resistance modeling. Microsyst Nanoeng 12, 65 (2026). https://doi.org/10.1038/s41378-026-01193-5
Słowa kluczowe: manipulacja komórkami, mikropipeta, robotyka, microfluidyka, automatyzacja