Clear Sky Science · pl
Strategie kontroli organizacji przestrzennej komórek w mikro-fizjologicznych systemach
Tworzenie miniaturowych tkanek w laboratorium
Nasze narządy funkcjonują tak dobrze, ponieważ komórki nie są rozrzucone przypadkowo — są starannie ułożone w przestrzeni. Artykuł bada, jak naukowcy uczą się odtwarzać tę złożoną organizację wewnątrz „organów na chipie” i innych miniaturowych, hodowanych w laboratorium tkanek. Sterując tym, gdzie znajdują się różne komórki i jak ze sobą oddziałują, badacze mogą tworzyć bardziej realistyczne modele serca, mózgu, jelit, naczyń krwionośnych, a nawet ekosystemów człowiek–mikrob. Zaawansowane systemy obiecują bezpieczniejsze testy leków, mniej doświadczeń na zwierzętach oraz lepsze narzędzia do badania chorób i opracowywania spersonalizowanych terapii.
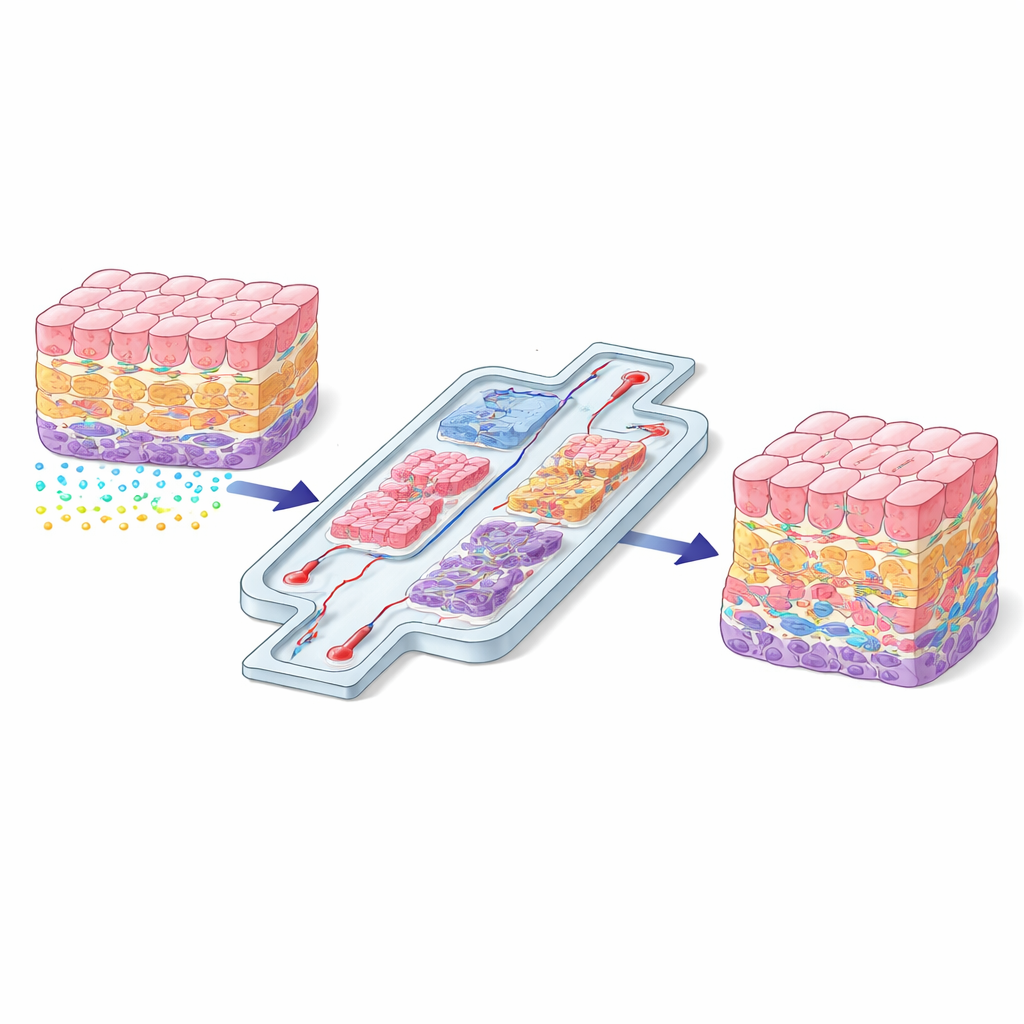
Dlaczego pozycja komórki ma znaczenie
W organizmie każda komórka żyje w określonej „dzielnicy” z własnym zestawem struktur podporowych, sygnałów chemicznych i sił fizycznych. Komórka wątroby blisko naczynia krwionośnego odbiera inne sygnały niż komórka położona głęboko wewnątrz narządu. Różnice te wpływają na to, jak komórki rosną, w co się różnicują i jak reagują na uraz czy leki. Gdy naukowcy hodują komórki na płaskich, plastikowych naczyniach, ta przestrzenna „konwersacja” jest w dużej mierze utracona i komórki często zachowują się nienaturalnie. Autorzy artykułu twierdzą, że odtwarzanie realistycznej organizacji przestrzennej nie jest opcjonalnym ulepszeniem, lecz podstawowym wymogiem, jeśli hodowane w laboratorium tkanki mają naśladować prawdziwe narządy.
Dwa główne sposoby rozmieszczania komórek
Autorzy dzielą obecne strategie na dwie szerokie rodziny: kontrolę bezpośrednią i pośrednią. Metody bezpośrednie fizycznie umieszczają komórki lub przegrody dokładnie tam, gdzie są potrzebne. Przykłady obejmują bio-drukowanie 3D, które nakłada warstwy komórek i miękkich żeli jak biologiczna drukarka 3D; mikrofluidyczne chipy, które formują tkanki w połączone komory i kanały; oraz metody fizycznego „uwięzienia”, które przesuwają komórki na miejsce przy użyciu światła, dźwięku, magnesów lub pól elektrycznych. Te podejścia sprawdzają się, gdy istotna jest precyzyjna geometria — na przykład przy odtwarzaniu bariery krew–mózg, warstwowej ściany naczynia krwionośnego czy drogi przepływu od jelita do wątroby.
Pozwalanie komórkom „czytać” otoczenie
Metody pośrednie zamiast tego przekształcają otoczenie i pozwalają komórkom robić resztę. Naukowcy stroją tu „krajobraz”, który komórki odbierają: skład otaczającego żelu, sztywność i teksturę powierzchni oraz gradienty rozpuszczonych substancji, takich jak czynniki wzrostu czy leki. Odpowiednio rozmieszczone cząsteczki podporowe mogą sprawić, że określone typy komórek osiedlą się w konkretnych regionach. Inteligentne hydrożele, które zmiękczają się lub uwalniają sygnały w odpowiedzi na przebudowę przez komórki, sprzyjają samoorganizującym się strukturom, takim jak sieci naczyń krwionośnych czy kryptowate i kosmki jelitowe. Urządzenia mikrofluidyczne mogą generować stabilne gradienty chemiczne, które powodują, że komórki macierzyste przyjmują różne tożsamości wzdłuż kanału, lub że komórki nowotworowe i komórki odpornościowe przemieszczają się do odrębnych stref, ujawniając mechanizmy rozprzestrzeniania się chorób.
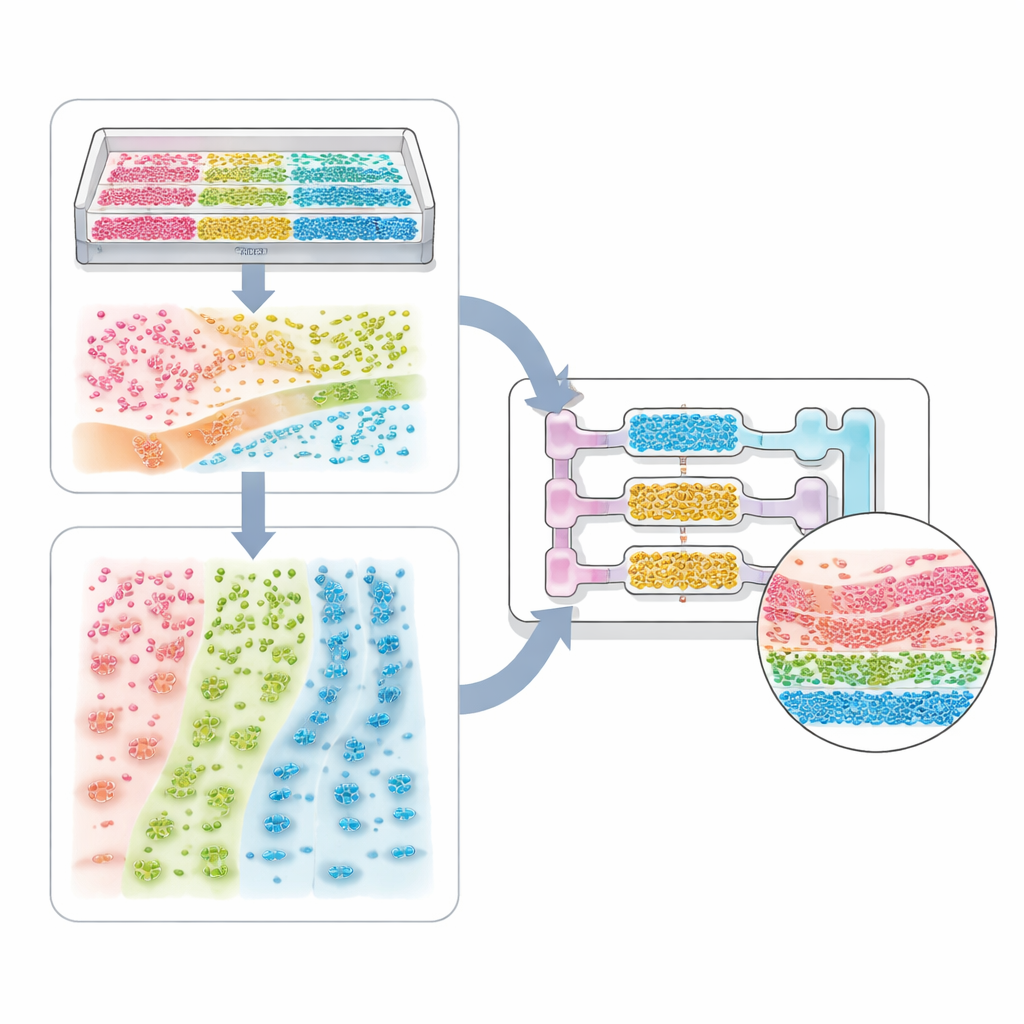
Od systemów jednorodnych do modeli całego organizmu
Przegląd opisuje spektrum zastosowań. Na najprostszym końcu znajdują się systemy z pojedynczym typem komórek, gdzie wzory rowków lub gradienty sztywności mogą sprawić, że komórki serca będą bić synchronicznie, a neurony wydłużać zorientowane włókna. Bardziej złożone modele tkankowe mieszają kilka typów komórek — na przykład komórki nowotworowe, komórki podporowe i komórki śródbłonka — aby tworzyć sferoidy i organoidy z wewnętrznymi rdzeniami i powłokami. Mikrokanalowe chipy i bio-drukowanie dodają wtedy granice i przepływ, pozwalając odtworzyć pęcherzyki płucne, filtry nerek, strefy wątroby oraz obwody wielonarządowe śledzące, jak lek jest wchłaniany, transformowany i usuwany. Te same pomysły odnoszą się do systemów gospodarz–mikrob, gdzie rozmieszczenie bakterii wzdłuż ściany jelita lub przezwarstwienie śluzowe może decydować, czy chronią nas, czy wywołują chorobę.
Sprawdzanie, czy wzory są prawdziwe
W miarę jak systemy stają się bardziej złożone, naukowcy potrzebują wiarygodnych metod potwierdzania, że komórki trafiają tam, gdzie powinny, i zachowują się zgodnie z zamierzeniem. Artykuł podkreśla metody obrazowania, które pozwalają obserwować żywe komórki w ruchu i zmianie w czasie, oraz zaawansowane techniki barwienia i sekwencjonowania mapujące, które geny, białka i metabolity pojawiają się w poszczególnych lokalizacjach. Czujniki osadzone na chipach mogą śledzić tlen, składniki odżywcze, kwasowość i siły mechaniczne, wiążąc lokalne warunki z odpowiedziami komórek. Razem te narzędzia pomagają badaczom zweryfikować, że projekt jest nie tylko przekonujący wizualnie, lecz także funkcjonalnie zgodny z rzeczywistą tkanką.
Dokąd zmierza ta praca
Autorzy konkludują, że najpotężniejsze systemy będą łączyć strategie bezpośrednie i pośrednie: używając chipów i bio-drukarek do ustalenia ogólnego układu, a następnie warstwując regulowane żele, tekstury i gradienty, które pozwolą tkankom dojrzewać i przebudowywać się z czasem. Zauważają też praktyczne przeszkody — takie jak skalowanie produkcji, zmniejszanie zmienności między laboratoriami oraz kwestie etyczne związane ze złożonymi modelami tkanek ludzkich. Mimo to przesłanie jest jasne: opanowanie organizacji przestrzennej to klucz do przekształcenia mikro-fizjologicznych systemów w wiarygodne zamienniki ludzkich organów, otwierając nowe możliwości badania rozwoju, testowania terapii i dopasowywania medycyny do indywidualnych pacjentów.
Cytowanie: Truong, H.D., Ge, Z., Chng, E. et al. Strategies to control cellular spatial organization in microphysiological systems. Microsyst Nanoeng 12, 85 (2026). https://doi.org/10.1038/s41378-025-01141-9
Słowa kluczowe: organ-on-a-chip, organizacja przestrzenna komórek, bio-drukowanie 3D, mikrofluidyczne modele tkanek, mikro-fizjologiczne systemy