Clear Sky Science · pl
Jednorurowa platforma punktowa oparta na CRISPR do szybkiego, specyficznego i czułego wykrywania HPV 16 bez wstępnej amplifikacji
Dlaczego wykrycie jednego typu wirusa ma znaczenie
Rak szyjki macicy często wiąże się z infekcją ludzkimi wirusami brodawczaka (HPV), ale nie wszystkie typy HPV niosą takie samo ryzyko. Lekarze potrzebują więc testów, które niezawodnie rozróżniają te bardzo podobne wirusy, zwłaszcza wysokiego ryzyka typu HPV16. Problem polega na tym, że współczesne testy genetyczne czasami mylą bliskich krewnych, co prowadzi do fałszywych alarmów lub przeoczonych przypadków. W tym badaniu przedstawiono nową metodę testowania, która wyraźnie poprawia zarówno dokładność, jak i praktyczność, dążąc do wprowadzenia precyzyjnego subtypowania HPV do klinik i punktów opieki.
Sprytne molekularne zamki i klucze
Naukowcy opracowali test w jednej probówce, który nazwali CASTSA, łączący dwie potężne koncepcje: precyzję CRISPR, systemu celowania genów zaadaptowanego od bakterii, oraz wzmacnianie sygnału metodą PCR, standardową technikę kopiowania DNA. W CASTSA białko CRISPR o nazwie Cas12a jest kierowane do sekwencji genetycznej HPV16 przez krótki RNA‑„klucz”. Gdy znajdzie dokładne dopasowanie oraz pobliski krótki wzorzec, którego wymaga, Cas12a przecina wirusowe DNA w przewidywalnym miejscu. To nacięcie tworzy charakterystyczny wolny koniec jednej nici DNA, który służy jako unikalny punkt startowy dla amplifikacji. Inne typy HPV, nawet o bardzo podobnych sekwencjach, są albo nie przecinane, albo nie tworzą odpowiedniego punktu startowego, więc nie są amplifikowane.
Jak małe nacięcie daje silny sygnał
Aby przekształcić nacięcie CRISPR w wykrywalny sygnał, zespół zaprojektował specjalny starter DNA zwany starterem specyficznym dla końca. Ten starter przyłącza się prawidłowo tylko do nici powstałej w wyniku cięcia Cas12a, następnie składa się w pętlę jak spinka do włosów i pomaga zbudować stabilną matrycę do PCR. Dodatkowe „uniwersalne” sekwencje starterów przyczepiają się potem i napędzają konwencjonalną reakcję PCR w czasie rzeczywistym. Kluczowe jest to, że amplifikacja zachodzi tylko wtedy, gdy Cas12a najpierw wykona swoje zadanie i gdy starter poprawnie się złoży, tworząc dwie warstwy kontroli. Taka architektura znacząco zmniejsza szansę, że częściowo dopasowane, niecelowe DNA zostanie przypadkowo amplifikowane, rozwiązując powszechny problem wcześniejszych testów opartych na CRISPR, które polegały na oddzielnym etapie wstępnej amplifikacji.
Wszystko w jednej probówce, z mniejszą liczbą błędów
Kluczowy postęp praktyczny polega na tym, że cięcie CRISPR i amplifikacja PCR zachodzą razem w tej samej zamkniętej probówce, co eliminuje konieczność otwierania probówek między etapami — główne źródło zanieczyszczeń w wielu procedurach laboratoryjnych. Autorzy starannie dostroili warunki reakcji, szczególnie poziomy magnezu, tak aby zarówno Cas12a, jak i enzym kopiujący DNA działały dobrze bez sprzyjania reakacjom niepożądanym. Wykazali, że ich jednoprożeniowe (one‑pot) ustawienie potrafi wiarygodnie odróżnić HPV16 od kilku innych typów wysokiego ryzyka, w tym HPV18, 33, 45 i 52, mimo iż te wirusy dzielą silnie konserwowane regiony genetyczne. W porównaniu ze standardowym PCR w czasie rzeczywistym, czy z testami CRISPR, które najpierw amplifikują DNA, a dopiero potem przeprowadzają wykrywanie CRISPR, CASTSA generowało znacznie mniej mylących sygnałów z typów pozastargetowych.
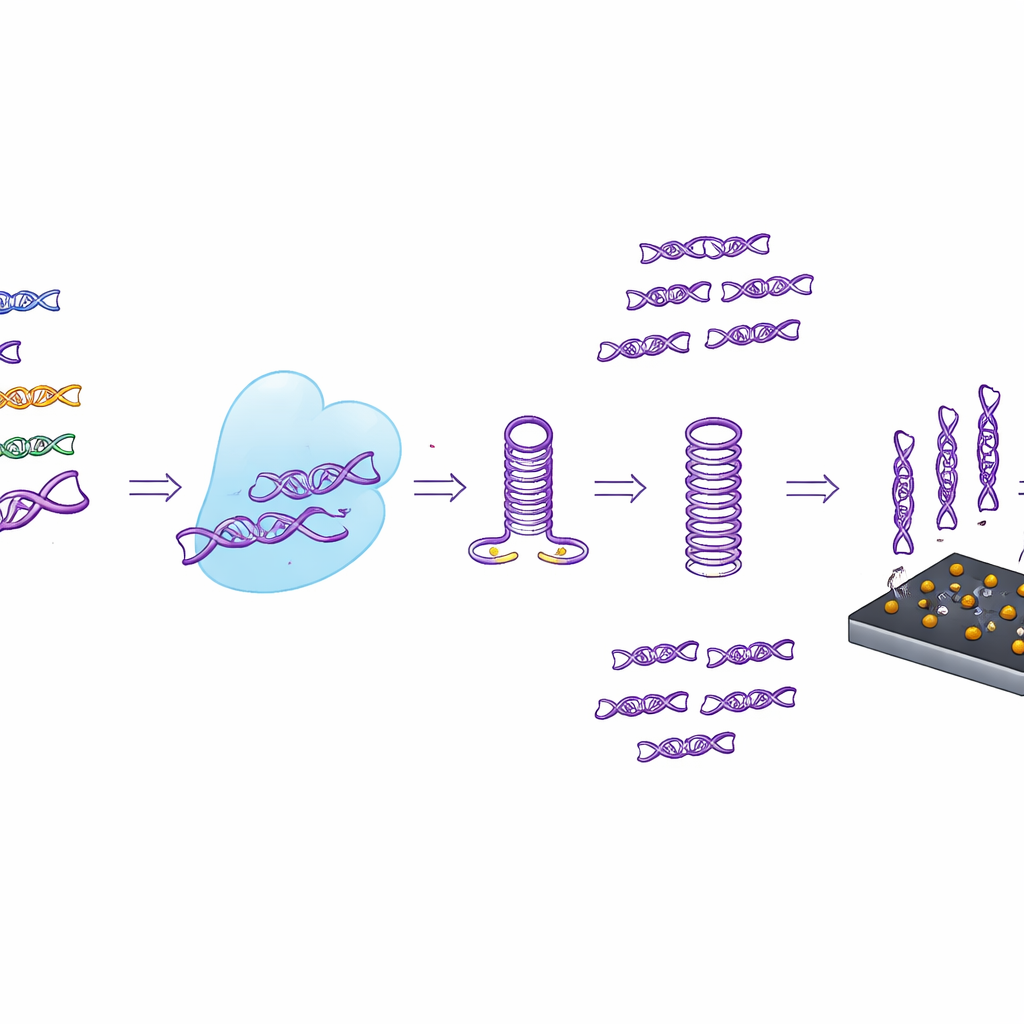
Od probówki do przenośnego czujnika
Zamiast polegać wyłącznie na odczytach fluorescencyjnych, badacze połączyli CASTSA z kompaktowym sensorem elektrochemicznym wykonanym z grafenu wywołanego laserowo. Ta porowata, wysoko przewodząca powierzchnia węglowa jest ozdobiona nanocząstkami złota, które niosą nici chwytające zaprojektowane tak, aby wiązać tylko produkty amplifikacji CASTSA z HPV16. Gdy te produkty przyczepią się, prąd elektryczny przepływający przez sensor zmienia się w mierzalny sposób. Dzięki użyciu układu z czterema elektrodami — trzech punktów pomiarowych i jednego wbudowanego kontrolnego tła — urządzenie może odjąć szum wynikający z niespecyficznego przywierania. W próbach zintegrowany system wykrył zaledwie 18 kopii docelowego fragmentu HPV16 na reakcję, przewyższając czułość samej fluorescencji i zachowując doskonałą powtarzalność.
Jak to może zmienić testowanie HPV
Aby sprawdzić działanie metody w praktyce, zespół przetestował 20 próbek klinicznych znanych z obecności HPV16 oraz 10 próbek od zdrowych dawców. CASTSA, zarówno w formie fluorescencyjnej, jak i po sparowaniu z sensorem na bazie grafenu, całkowicie zgadzała się ze standardowymi szpitalnymi testami PCR. Jednocześnie wykazała lepszą zdolność ignorowania innych wysokiego ryzyka typów HPV, które często powodują niejasności. Dla pacjentów może to oznaczać mniej niejednoznacznych wyników i pewniejsze decyzje dotyczące dalszej diagnostyki i leczenia. Szerzej, strategia CASTSA — najpierw rozpoznanie przez CRISPR, potem amplifikacja, wszystko w jednej zamkniętej probówce — oferuje wzorzec dla wysoce specyficznych, o niskim ryzyku zanieczyszczeń testów genetycznych, które można dostosować do wielu patogenów i mutacji, szczególnie w miejscach wymagających szybkich, wiarygodnych odpowiedzi.
Cytowanie: Chen, Y., Chen, Y., Zhang, C. et al. One-pot CRISPR-based point of care platform for rapid, specific and sensitive detection of HPV 16 without pre-amplification. Microsyst Nanoeng 12, 81 (2026). https://doi.org/10.1038/s41378-025-01130-y
Słowa kluczowe: Wykrywanie HPV16, Diagnostyka CRISPR, Testy oparte na PCR, elektrochemiczny biosensor, test punktowy