Clear Sky Science · pl
Syntetyczna śmiertelność inhibicji MCL-1 i terapii CAR-T w agresywnych chłoniakach B‑komórkowych
Dlaczego to ma znaczenie dla leczenia raka
Agresywne chłoniaki B‑komórkowe to szybko rosnące nowotwory krwi, które często nawracają po leczeniu. Nawet potężne nowe metody, takie jak terapia CAR‑T, która przeprogramowuje własne komórki odpornościowe pacjenta do ataku na nowotwór, zawodzą u około połowy pacjentów w dłuższej perspektywie. W badaniu tym zbadano sposób, aby tę słabość przekuć w zaletę: zastosowanie leku celującego w kluczowe białko podtrzymujące życie komórek chłoniaka, aby jednocześnie zabić guzy i uczynić pozostałe komórki bardziej podatnymi na eliminację przez komórki CAR‑T.
Problem uporczywych komórek chłoniaka
Agresywne chłoniaki B‑komórkowe często są napędzane nadmierną aktywnością genu MYC, który pobudza szybkie podziały komórek i pomaga im ukrywać się przed układem immunologicznym. Standardowe terapie, a nawet terapia CAR‑T, mogą pozostawiać małe ogniska komórek chłoniaka, które tolerują leki i później powodują nawroty. Te „przetrwałe” i oporne komórki żyją w mikrośrodowisku guza pełnym supresyjnych komórek odpornościowych, które tłumią działanie zabójczych limfocytów T. Autorzy postawili pytanie, czy zablokowanie MCL‑1, białka, od którego komórki chłoniaka zależą, by uniknąć samozniszczenia, może ujawnić ukrytą słabość tego systemu.
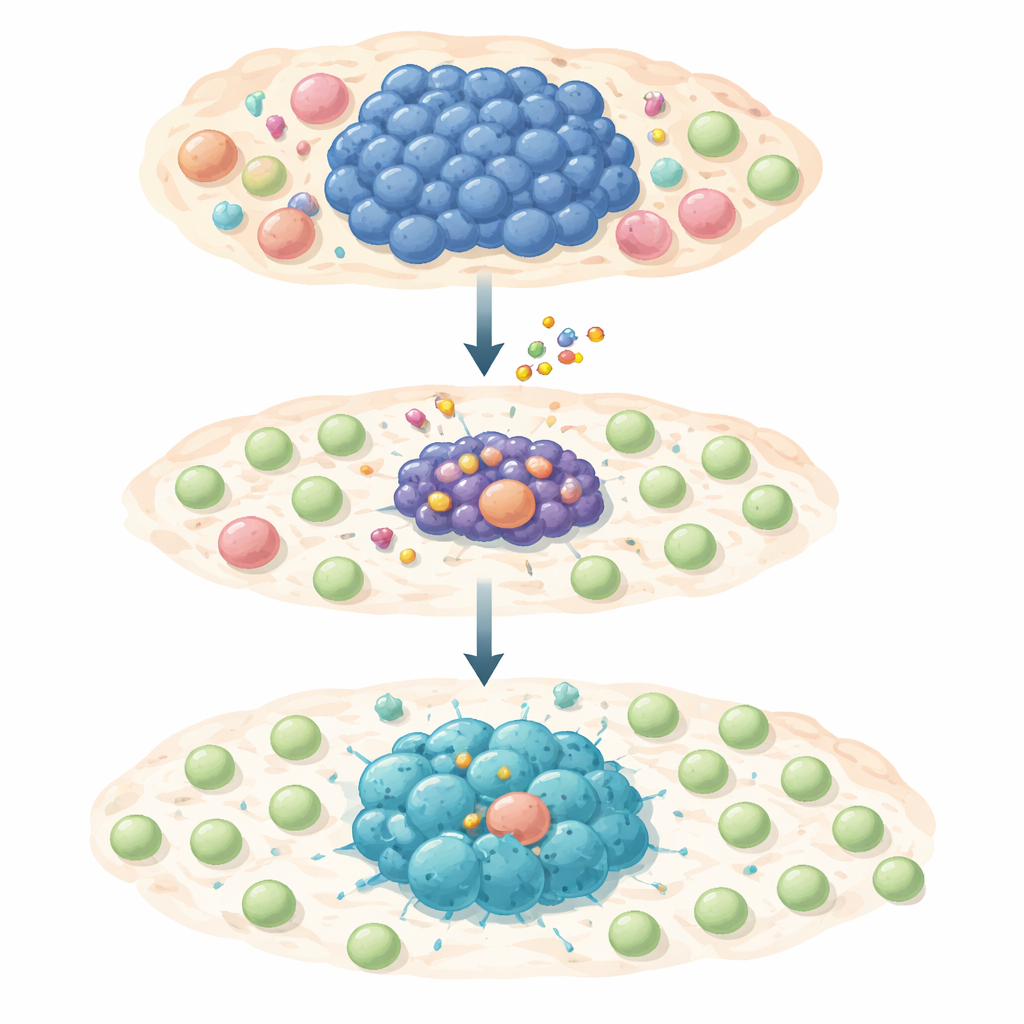
Dwustopniowy atak na przeżycie guza i jego ukrywanie
Zespół przetestował selektywny inhibitor MCL‑1, S63845, na dużej serii ludzkich linii komórkowych chłoniaka zależnych od MYC. Większość tych komórek nowotworowych była wysoce wrażliwa na lek i ulegała zaprogramowanej śmierci po zablokowaniu MCL‑1. Jednak niewielka ich część przetrwała krótkotrwałą lub długotrwałą ekspozycję i stała się tolerancyjna na lek lub w pełni oporna. Po dokładnym zbadaniu tych ocalonych komórek stwierdzono, że aktywność MYC była przytłumiona, podczas gdy inne białko, STAT1, oraz związana z nim ścieżka alarmowa interferonów zostały włączone. Ta zmiana uruchamiała geny napędzające sygnały zapalne i chemokiny — molekularne „sygnały świetlne”, które mogą przyciągać limfocyty T do obszaru guza.
Przywrócenie aktywności sąsiedztwa odpornościowego
Aby sprawdzić, jak to działa in vivo, autorzy lecili myszy z chłoniakami napędzanymi przez MYC niską dawką inhibitora MCL‑1. Lek zmniejszył masę guza przy oszczędzaniu normalnych komórek B, ale jego wpływ wykraczał poza zwykłe zmniejszenie objętości. Leczone guzy miały więcej limfocytów T CD4 i CD8, mniej limfocytów T w stanie wyczerpania, mniej komórek regulatorowych T oraz mniej supresyjnych komórek mieloidalnych — wszystkie te zmiany świadczyły o bardziej przyjaznym dla odporności mikrośrodowisku. Sekwencjonowanie RNA pojedynczych komórek guza i komórek otaczających potwierdziło, że pozostające komórki chłoniaka miały obniżone MYC, zwiększone STAT1 oraz silniejsze sygnały interferonowe i zapalne, podczas gdy otaczające tkanki zostały zreperowane przez aktywne komórki T i komórki NK zamiast komórek supresyjnych.
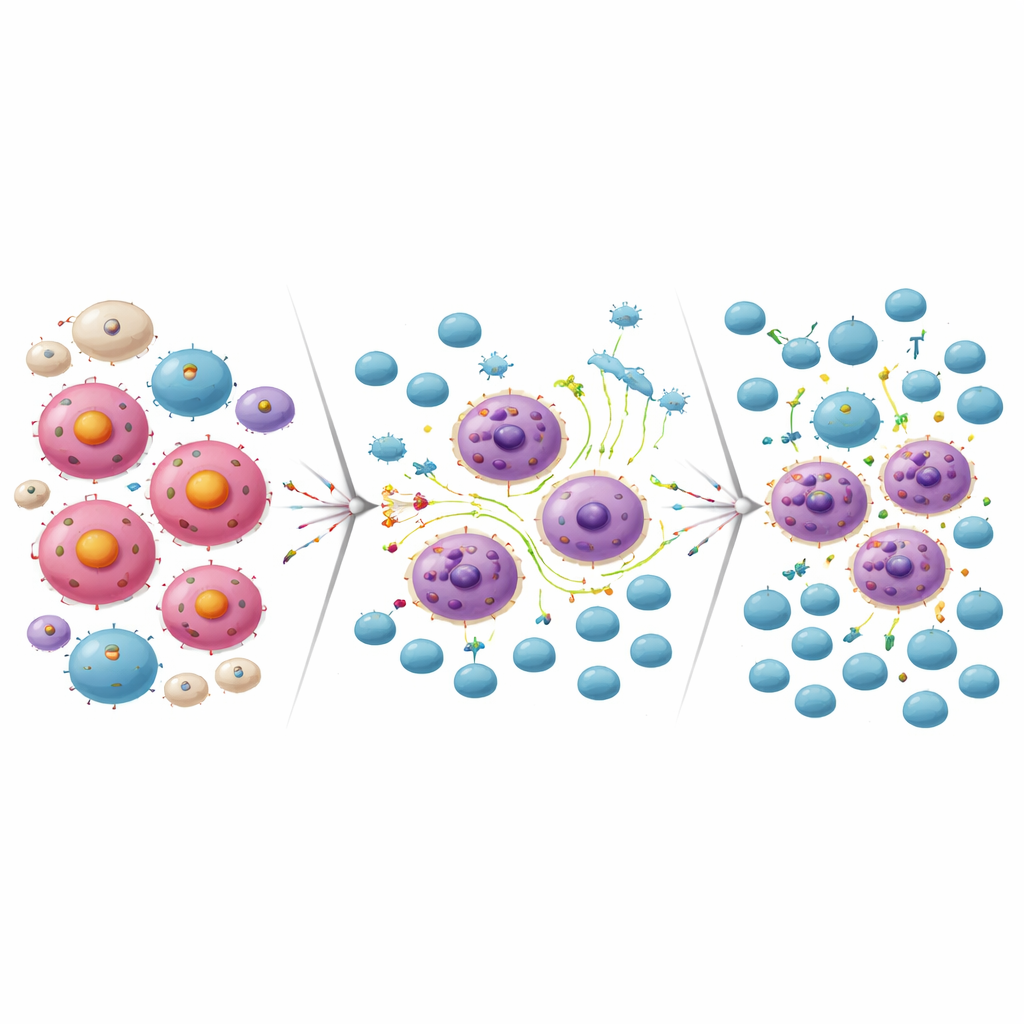
Przekształcenie oporności w okazję dla komórek CAR‑T
Ta sama reprogramacja zapalna, która pomogła niektórym komórkom chłoniaka przetrwać blokadę MCL‑1, jednocześnie uczyniła je bardziej podatnymi na atak immunologiczny. W warunkach laboratoryjnych komórki CAR‑T ukierunkowane na CD19 efektywnie zabijały komórki chłoniaka, które stały się oporne na lek MCL‑1. Odwrotnie, komórki chłoniaka oporne na terapię CAR‑T przeciw CD19 były wysoce wrażliwe na inhibitor MCL‑1. Gdy badacze połączyli subletalną dawkę inhibitora MCL‑1 z komórkami CAR‑T w hodowli komórkowej, oba zabiegi razem zniszczyły znacznie więcej komórek chłoniaka niż każdy z nich osobno. W modelach mysich podanie inhibitora MCL‑1, a następnie komórek CAR‑T przeciw CD19, doprowadziło do niemal całkowitego oczyszczenia guza i istotnie wydłużyło przeżycie w porównaniu z monoterapiami.
Celujący cios z potencjałem leczniczym
Mówiąc krótko, badanie sugeruje strategię „jeden‑dwa”. Najpierw lek blokujący MCL‑1 redukuje większość chłoniaka i zmusza przetrwałe komórki nowotworowe do stanu zapalnego, w którym stają się wyraźnie widoczne i tracą ochronne tarcze immunologiczne. Następnie komórki CAR‑T przeciw CD19 wykorzystują tę odsłoniętą słabość, aby wykorzenić pozostałą chorobę. Uderzając zarówno w wewnętrzne mechanizmy przeżycia guza, jak i jego ochronne mikrośrodowisko, połączone podejście może zmniejszyć liczbę nawrotów i przybliżyć agresywne chłoniaki B‑komórkowe do długotrwałej remisji.
Cytowanie: Gao, J., Zhao, X., Yin, Q. et al. Synthetic lethality of MCL-1 inhibition and CAR-T therapy in aggressive B-cell lymphoma. Leukemia 40, 638–648 (2026). https://doi.org/10.1038/s41375-026-02884-8
Słowa kluczowe: chłoniak B-komórkowy, terapia CAR-T, inhibicja MCL-1, mikrośrodowisko guza, oporność na leki