Clear Sky Science · pl
Tłumienie miR-29 przez MYC prowadzi do zwiększonego sygnału CD40 w zmetamorfizowanym chłoniaku grudkowym
Kiedy rozmowa między komórkami staje się niebezpieczna
Chłoniak grudkowy to powoli rosnący nowotwór krwi, który może tlić się przez lata, lecz u niektórych pacjentów nagle przyspiesza i staje się agresywną, zagrażającą życiu chorobą. W tym badaniu postawiono proste, lecz kluczowe pytanie: co zmienia się wewnątrz tych komórek nowotworowych i w ich komórkowym sąsiedztwie, by przełączyć ten tryb? Śledząc zarówno geny komórek nowotworowych, jak i maleńkie regulatory RNA podczas tej przemiany, badacze odkryli ukrytą pętlę regulacyjną, która dopasowuje, jak silnie komórki nowotworowe odpowiadają na pomoc pobliskich komórek odpornościowych — i pokazali, że gdy ten układ zawodzi, rak staje się trudniejszy do leczenia.
Cichy rak, który czasem przyspiesza
Chłoniak grudkowy wywodzi się z komórek B, komórek układu odpornościowego, które normalnie produkują przeciwciała. U większości pacjentów choroba ma przebieg indolentny, czyli powolny, jednak niewielka część przypadków każdego roku przechodzi transformację w agresywny chłoniak, który zachowuje się bardziej jak rozlany chłoniak z dużych komórek B. Mutacje genetyczne powiązano z tą zmianą, lecz nie wyjaśniały one całej historii. Komórki nowotworowe żyją w bogatym mikrośrodowisku pełnym pomocniczych komórek T i innych partnerów odpornościowych, nieustannie wymieniając sygnały. Autorzy przypuszczali, że małe cząsteczki regulacyjne zwane mikroRNA, które precyzyjnie modulują wykorzystanie genów, mogą być kluczowe dla tego, jak komórki nowotworowe przystosowują się do zmieniającego się sąsiedztwa i dokonują skoku w kierunku bardziej niebezpiecznego stanu.
Małe hamulce RNA znikają
Aby sprawdzić ten pomysł, zespół przeprowadził pierwsze dopasowane profilowanie zarówno informacyjnych RNA (mRNA), jak i mikroRNA w parach próbek pobranych od tych samych pacjentów przed i po transformacji. Porównując 11 próbek chłoniaka grudkowego z ich 11 zmetamorfizowanymi odpowiednikami, znaleźli ponad tysiąc genów i 19 mikroRNA, które uległy zmianie. Wyróżniła się jedna rodzina: wszystkie trzy członkinie rodziny miR‑29 były konsekwentnie obniżone w zmetamorfizowanych guzach. W wcześniejszych pracach w innych nowotworach krwi miR‑29 pełniło rolę hamulca wzrostu i przeżycia komórek. Tutaj jego utrata wyłoniła się jako cecha charakterystyczna transformacji, sugerując, że stłumienie tej rodziny mikroRNA może uwolnić szlaki sprzyjające wzrostowi w komórkach chłoniaka.
Wzmocniony sygnał od komórek pomocniczych
Zgłębiając dane o ekspresji genów, badacze odkryli, że zmetamorfizowane guzy wykazywały silny wzrost aktywności szlaku CD40, czyli drogi sygnałowej uruchamianej, gdy komórka T pomocnicza łączy się z komórką B. W zdrowych węzłach chłonnych i w indolentnym chłoniaku grudkowym ta interakcja pomaga komórkom B rosnąć i przeżywać w kontrolowany sposób. Co zaskakujące, w zmetamorfizowanych próbkach geny związane z CD40 były włączone w około 90 procent przypadków, mimo że ogólna liczba komórek T w obszarach guza była w rzeczywistości niższa. Analizy pojedynczych komórek potwierdziły, że podzbiór komórek T nadal dostarczał sygnału aktywującego CD40, ale same komórki chłoniaka wydawały się stać znacznie bardziej wrażliwe na ten sygnał.
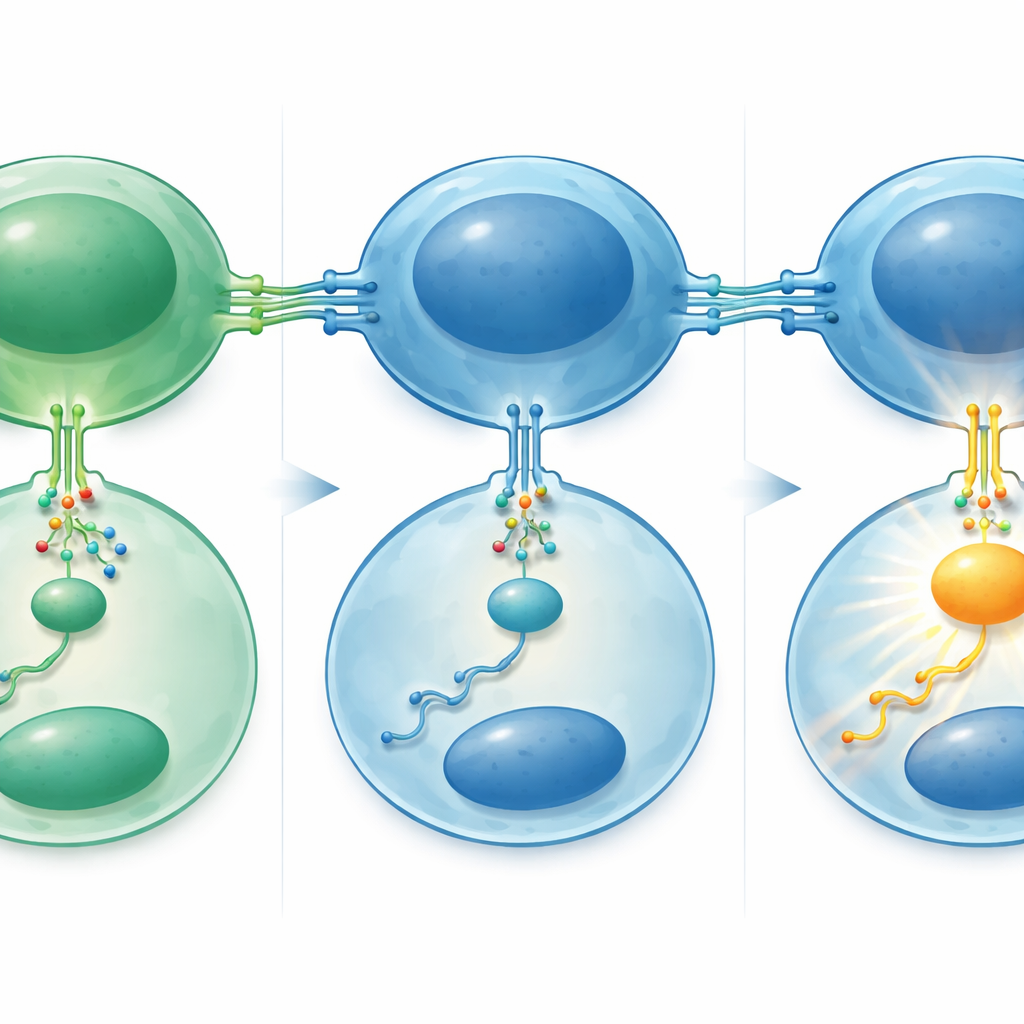
Jak trzystopniowy układ wzmacnia wzrost
Autorzy następnie złożyli w całość molekularny układ leżący u podstaw tej zwiększonej wrażliwości. Eksperymenty laboratoryjne wykazały, że miR‑29 normalnie utrzymuje poziomy białka zwanego TRAF4 pod kontrolą w komórkach B; TRAF4 jest wewnętrznym adaptorowym białkiem, które pomaga przekazać sygnał CD40 głębiej do komórki. Gdy poziomy miR‑29 były eksperymentalnie podnoszone w liniach komórkowych chłoniaka, poziomy TRAF4 spadały, a komórki słabiej reagowały na stymulację CD40, z mniejszą aktywacją dalszych elementów sygnalizacji i wolniejszą proliferacją. W próbkach pacjentów zaobserwowano odwrotny wzorzec: zmetamorfizowane guzy i chłoniaki grudkowe o wyższym stopniu złośliwości miały więcej TRAF4 i wyższe tempo podziałów komórkowych. Kolejny główny gracz, dobrze znane białko sprzyjające nowotworom MYC, znajdował się powyżej tego układu. Poziomy i aktywność MYC wzrastały podczas transformacji, a wykazano, że MYC wiąże się bezpośrednio z regionami DNA kontrolującymi miR‑29, działając jako przełącznik, który wycisza tę rodzinę mikroRNA.
Co to oznacza dla pacjentów
Składając te elementy razem, badanie opisuje trzystopniowy łańcuch: aktywacja MYC tłumi miR‑29, utrata miR‑29 usuwa hamulec dla TRAF4, a dodatkowy TRAF4 sprawia, że komórki chłoniaka stają się nadmiernie wrażliwe na sygnały CD40 od kilku pozostałych komórek T pomocniczych. To wzmocnione „wsparcie” napędza silniejszy wzrost i przeżycie, przyczyniając się do transformacji. Klinicznie pacjenci, których guzy miały niższe poziomy miR‑29 — szczególnie członka miR‑29c — mieli tendencję do krótszego przeżycia i szybszych nawrotów, co potwierdzono w niezależnym badaniu terapeutycznym. Ponieważ miR‑29 można mierzyć wiarygodnie nawet w starych, zachowanych próbkach biopsji, a leki naśladujące miR‑29 lub blokujące sygnalizację CD40 są już badane, ta praca wskazuje nowe sposoby identyfikacji pacjentów z chłoniakiem grudkowym o wysokim ryzyku oraz projektowania terapii, które przerwą groźną rozmowę między komórkami nowotworowymi a ich sąsiadami odpornościowymi.
Cytowanie: Filip, D., Litzmanova, K., Michaelou, A. et al. Repression of miR-29 via MYC leads to increased CD40 signaling in transformed follicular lymphoma. Leukemia 40, 759–772 (2026). https://doi.org/10.1038/s41375-026-02868-8
Słowa kluczowe: chłoniak grudkowy, mikroRNA, sygnalizacja CD40, MYC, mikrośrodowisko nowotworu