Clear Sky Science · pl
Alnuctamab, dwuwartościowy engager limfocytów T skierowany przeciwko antygenowi dojrzewania komórek B (BCMA) dla pacjentów z nawrotowym lub opornym szpiczakiem mnogim: wyniki badania fazy 1, pierwszego badania w populacji ludzkiej
Dlaczego ten nowy lek przeciwnowotworowy ma znaczenie
Dla osób żyjących ze szpiczakiem mnogim, nowotworem krwi, który niemal zawsze nawraca po leczeniu, każda nowa opcja może oznaczać więcej czasu i lepszą jakość życia. To badanie sprawdza terapię immunologiczną następnej generacji o nazwie alnuctamab, zaprojektowaną tak, aby pomóc własnym komórkom obronnym organizmu odnaleźć i zniszczyć komórki szpiczaka. Badanie stawia praktyczne pytanie ważne dla pacjentów i lekarzy: czy tę silną terapię można podać jako prostą zastrzyk podskórny, osiągając mocne działanie przeciwnowotworowe przy mniejszej liczbie groźnych działań niepożądanych?
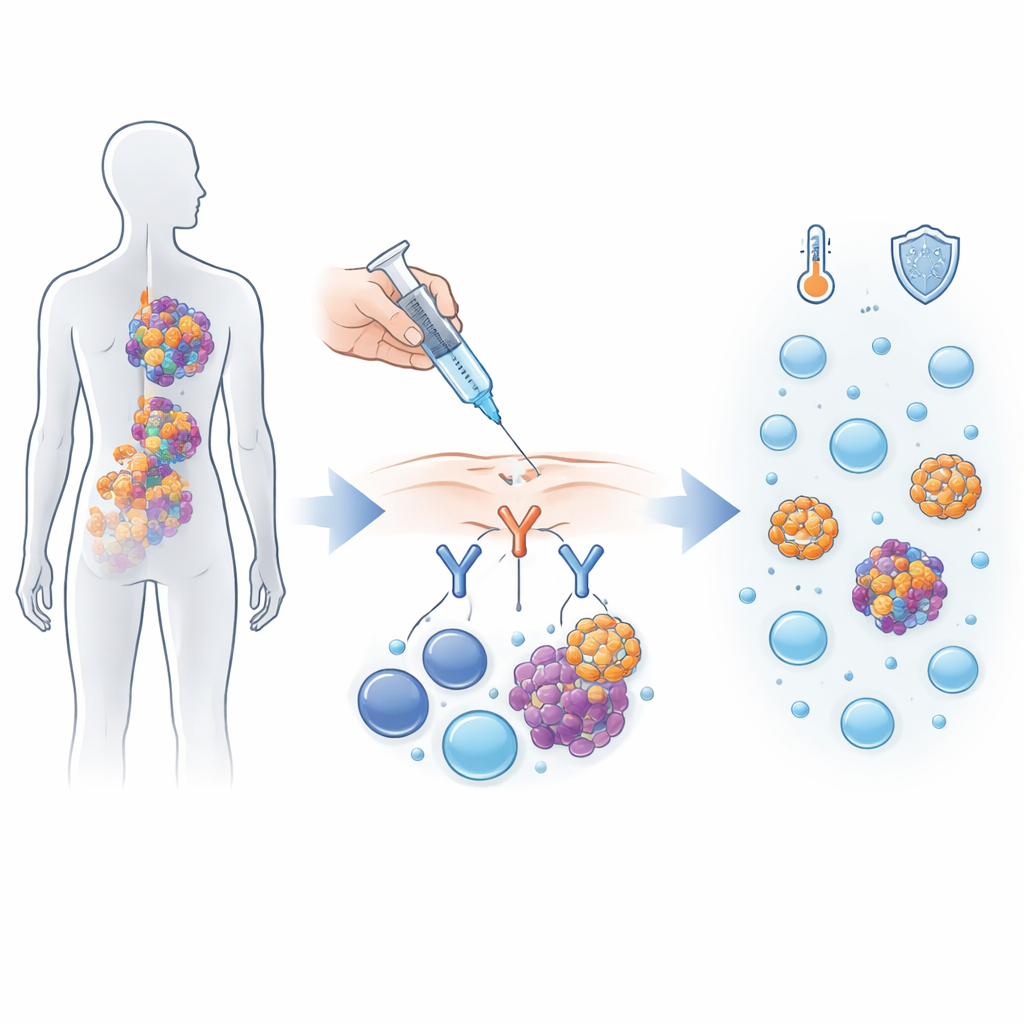
Sprytna metoda przekierowania układu odpornościowego
Alnuctamab należy do nowej klasy leków działających jak molekularni swatowie między komórkami nowotworowymi a komórkami układu odpornościowego. Komórki szpiczaka na swojej powierzchni noszą marker zwany BCMA, podczas gdy limfocyty T mają inny marker, CD3. Alnuctamab zbudowany jest z dwóch „ramion”, które wiążą BCMA, i jednego ramienia wiążącego CD3, przyciągając komórki T w bliski kontakt z komórkami szpiczaka, by mogły je zaatakować. W tym pierwszym badaniu u ludzi 165 osób ze szpiczakiem, który nawrocił po co najmniej trzech różnych rodzajach terapii, otrzymało alnuctamab dożylnie lub podskórnie.
Od wlewu do zastrzyku
Początkowo lek podawano dożylnie, ale to podejście powodowało bardziej intensywne reakcje układu odpornościowego, w tym zagrażający życiu epizod zespołu uwalniania cytokin (cytokine release syndrome), gdy układ odpornościowy nagle wyrzuca duże ilości sygnałów zapalnych. Z powodu tych obaw bezpieczeństwa i jedynie umiarkowanego efektu, badanie przeszło na podawanie podskórne, które uwalnia lek wolniej. Dziewięćdziesięciu pięciu pacjentów leczono w ten sposób według schematu „step-up”: małe dawki początkowe, po których następują wyższe dawki docelowe, a częstotliwość zastrzyków była stopniowo zmniejszana w czasie z tygodniowych do raz na cztery tygodnie, jeśli leczenie było kontynuowane.
Jak pacjenci reagowali i z czym się mierzyli
Wśród wszystkich pacjentów, którzy otrzymali podskórne zastrzyki, około 59% doświadczyło zmniejszenia guza o co najmniej połowę, a niemal połowa uzyskała status „minimalnej choroby resztkowej ujemnej” (MRD–), co oznacza, że bardzo czułe testy nie wykrywały już komórek szpiczaka w szpiku kostnym. Przy zalecanej dawce 30 miligramów odpowiedzi były jeszcze silniejsze: około 71% pacjentów zareagowało, a ponad połowa osiągnęła MRD–. Wielu pacjentów utrzymało kontrolę choroby przez blisko rok lub dłużej, nawet gdy schemat dawkowania stawał się mniej intensywny. Działania niepożądane były częste, ale w większości dały się kontrolować. Reakcje przypominające gorączkę wystąpiły u około trzech na pięciu pacjentów, ale wszystkie były łagodne lub umiarkowane. Wystąpiły także obniżenia liczby białych krwinek i infekcje, co odzwierciedla zarówno siłę leku, jak i osłabiony układ odpornościowy pacjentów, jednak ciężkie infekcje były rzadsze niż raportowano przy kilku podobnych lekach.
Dlaczego droga podskórna była bezpieczniejsza
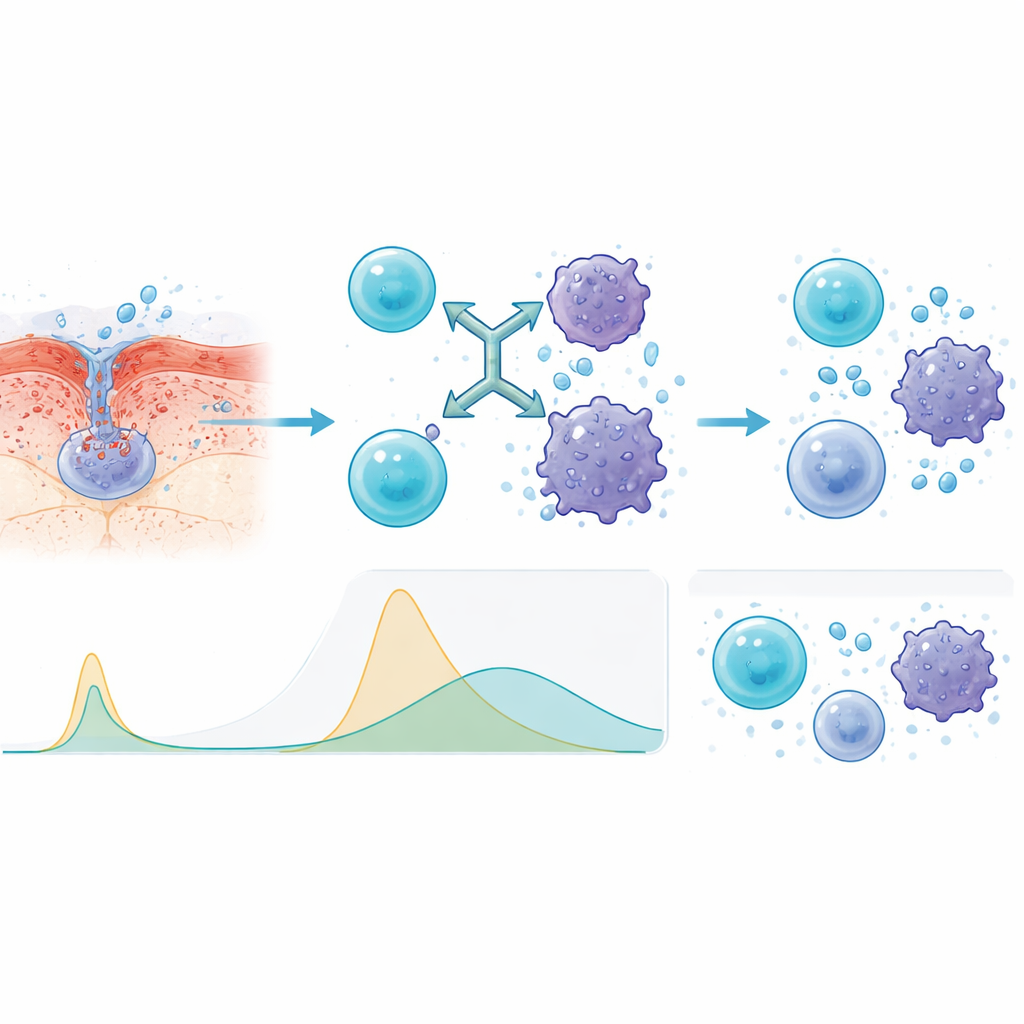
Aby zrozumieć, dlaczego metoda podskórna zachowywała się lepiej, badacze mierzyli we krwi molekuły sygnalizujące stan zapalny. W porównaniu z podaniem dożylnym, zastrzyki wywoływały wolniejsze i niższe szczyty kluczowych sygnałów zapalnych, takich jak interleukiny i czynnik martwicy nowotworu (TNF). Taki spłaszczony profil oznacza, że układ immunologiczny nadal jest aktywowany przeciwko rakowi, ale bez nagłego wyrzutu, który może doprowadzić pacjentów do stanu zagrażającego życiu. Zespół zauważył również, że osoby, których krew na początku wykazywała niższe poziomy odciętego (shed) BCMA — znak mniej agresywnej lub mniej zaawansowanej choroby — miały tendencję do lepszych odpowiedzi i dłuższego utrzymania remisji.
Co to oznacza dla przyszłej opieki nad chorymi na szpiczaka
Chociaż firma później zdecydowała nie kontynuować rozwoju alnuctamabu z powodów strategicznych, wnioski z tego badania są istotne. Pokazano, że starannie zaprojektowany engager immunologiczny można podać jako prosty zastrzyk na schemacie, który z czasem staje się mniej wymagający, a jednocześnie daje głębokie i trwałe odpowiedzi u wielu osób z trudnym do leczenia szpiczakiem. Wyniki sugerują także, że stopniowe zwiększanie dawki i unikanie ostrych szczytów aktywacji układu odpornościowego może ograniczyć poważne reakcje bez osłabiania działania przeciwnowotworowego. Te obserwacje prawdopodobnie będą kierować projektowaniem przyszłych terapii opartych na układzie odpornościowym, dając nadzieję, że więcej pacjentów z nawrotowym szpiczakiem otrzyma skuteczne terapie, które są nie tylko potężne, ale też bezpieczniejsze i łatwiejsze do zniesienia.
Cytowanie: Bar, N., Martin, T., Hofmeister, C.C. et al. Alnuctamab, a bivalent B-cell maturation antigen-targeting T cell engager for patients with relapsed or refractory multiple myeloma: results from a phase 1, first-in-human study. Leukemia 40, 481–490 (2026). https://doi.org/10.1038/s41375-025-02841-x
Słowa kluczowe: szpiczak mnogi, immunoterapia, przeciwciało dwuspecyficzne, BCMA, engager limfocytów T