Clear Sky Science · pl
Rozpuszczalny agonista Notch umożliwia dojrzewanie ludzkich ameloblastów i tworzenie tkanek przypominających szkliwo w celu regeneracji zęba
Dlaczego naprawa szkliwa jest tak trudna
Szkliwo, szklista biała powłoka pokrywająca nasze zęby, jest najtwardszym materiałem w ludzkim ciele — ale gdy zniknie, nie odrasta. Ponad 90 procent dorosłych ma ubytki lub uszkodzenia szkliwa, a nasze zęby nie mają naturalnej zdolności do jego odbudowy. To badanie opisuje sposób hodowli ludzkich komórek produkujących szkliwo w laboratorium, doprowadzania ich do pełnego dojrzewania i nawet skłaniania ich do tworzenia zmineralizowanej tkanki przypominającej szkliwo u zwierząt. Praca otwiera drogę do przyszłych terapii, które mogłyby pewnego dnia naprawiać zęby żywą tkanką zamiast wypełnień i koron.
Budowanie szkliwa z komórek macierzystych
Szkliwo tworzą wyspecjalizowane komórki zwane ameloblastami, które obumierają po wyrznięciu się zęba przez dziąsła. Bez nich zęby dorosłych nie potrafią wytworzyć nowego szkliwa. Badacze wykorzystują ludzkie indukowane pluripotencjalne komórki macierzyste — komórki dorosłe przeprogramowane do elastycznego, embrionalnego stanu — aby stworzyć „indukowane ameloblasty”. W wcześniejszych pracach te hodowane w laboratorium komórki potrafiły zacząć przypominać naturalne komórki wytwarzające szkliwo, ale zatrzymywały się przed osiągnięciem pełnej dojrzałości i funkcjonowały prawidłowo tylko wtedy, gdy rosły w bliskim kontakcie z odontoblastami, komórkami tworzącymi leżące poniżej zębiny. To postawiło kluczowe pytanie: co dokładnie odontoblasty dostarczają ameloblastom, aby mogły dokończyć rozwój?
Brakująca rozmowa między komórkami zębowymi
Aby rozszyfrować ten komórkowy dialog, zespół przeanalizował mapy ekspresji genów na poziomie pojedynczych komórek z rozwijających się ludzkich i mysich zębów. Szukali szlaków sygnałowych, które wydawały się działać specyficznie od odontoblastów do ameloblastów w kluczowym oknie, gdy formuje się szkliwo. Jeden szlak wyróżniał się szczególnie: Notch, bezpośredni system komunikacji komórka–komórka szeroko wykorzystywany w rozwoju embrionalnym. W tych mapach zębowych ligandy typu Delta (zwłaszcza DLL1 i DLL4) występowały głównie na odontoblastach, podczas gdy receptory Notch koncentrowały się na dojrzewających ameloblastach. Gdy badacze zablokowali aktywność Notch lekiem w systemie współhodowli, ameloblasty znacząco zmniejszyły produkcję enameliny, głównego białka szkliwa — to mocny dowód, że sygnalizacja Notch jest niezbędna, by komórki wytwarzające szkliwo mogły dojrzeć. 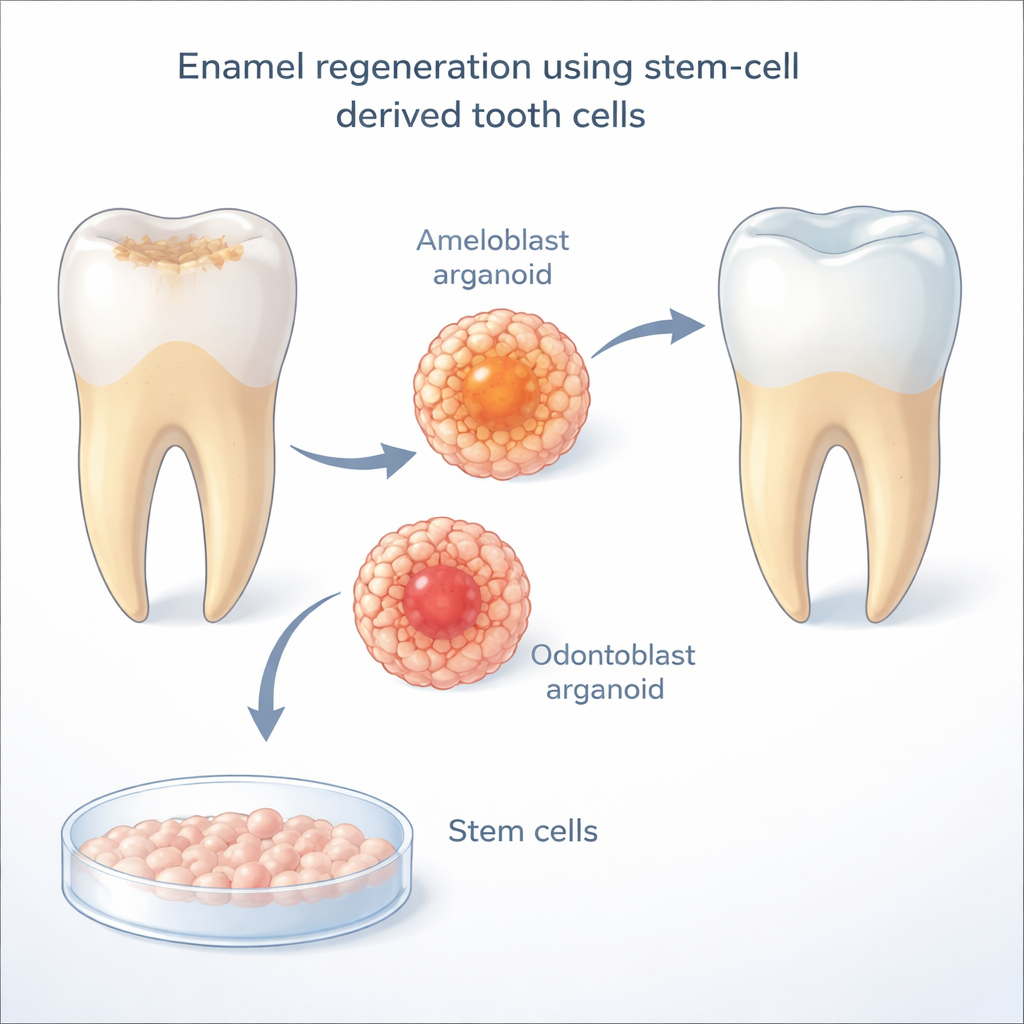
Sztucznie zaprojektowany przełącznik białkowy dla komórek szkliwa
Aby pójść dalej, zespół chciał precyzyjnie i kontrolowanie włączyć Notch, bez polegania na prawdziwych odontoblastach. Użyli sztucznego białka nazwanego C3‑DLL4, zaprojektowanego przy użyciu narzędzi obliczeniowych. Ta rozpuszczalna cząsteczka układa trzy kopie domeny sygnałowej DLL4 w sztywnym, trójramiennym rusztowaniu, co pozwala jej skupiać i aktywować receptory Notch na pobliskich komórkach podobnie jak naturalna sąsiednia komórka. W liniach reporterowych C3‑DLL4 silnie włączał geny zależne od Notch. Dodany do wczesnych organoidów ameloblastów — maleńkich trójwymiarowych skupisk komórek wyhodowanych z komórek macierzystych — wywołał gwałtowną zmianę aktywności genów. Organoidy przeszły z profilu niedojrzałego w kierunku odpowiadającemu ameloblastom sekrecyjnym i w pełni dojrzałym, uruchamiając charakterystyczne geny takie jak AMELX, ENAM, MMP20, ODAM, KLK4, TUFT1 i WDR72. Usunięcie aktywności Notch miało odwrotny efekt, zatrzymując dojrzewanie i zaburzając produkcję białek szkliwa.
Z organoidów do tkanki przypominającej szkliwo
Co uderzające, gdy te aktywowane przez Notch organoidy ameloblastów przeszczepiono pod torebkę nerkową myszy z niedoborem odporności — bezpieczną, dobrze ukrwioną niszę często używaną do testowania ludzkich tkanek — zaczęły odkładać gęsty, zmineralizowany materiał. Wysokorozdzielcze skany mikro‑CT i klasyczne techniki barwienia potwierdziły obecność zwapniałych guzków tam, gdzie normalnie taka tkanka nie występuje. Mikroskopia ujawniła zorganizowane, spolaryzowane warstwy ludzkich komórek eksprymujących kluczowe białka szkliwa i WDR72, czynnik związany z prawidłową mineralizacją szkliwa. Chociaż ten materiał lepiej opisać jako „przypominający szkliwo” niż w pełni naturalne szkliwo, wykazuje, że inżynierowane ludzkie ameloblasty mogą w zasadzie odkładać twardy minerał w żywym organizmie. 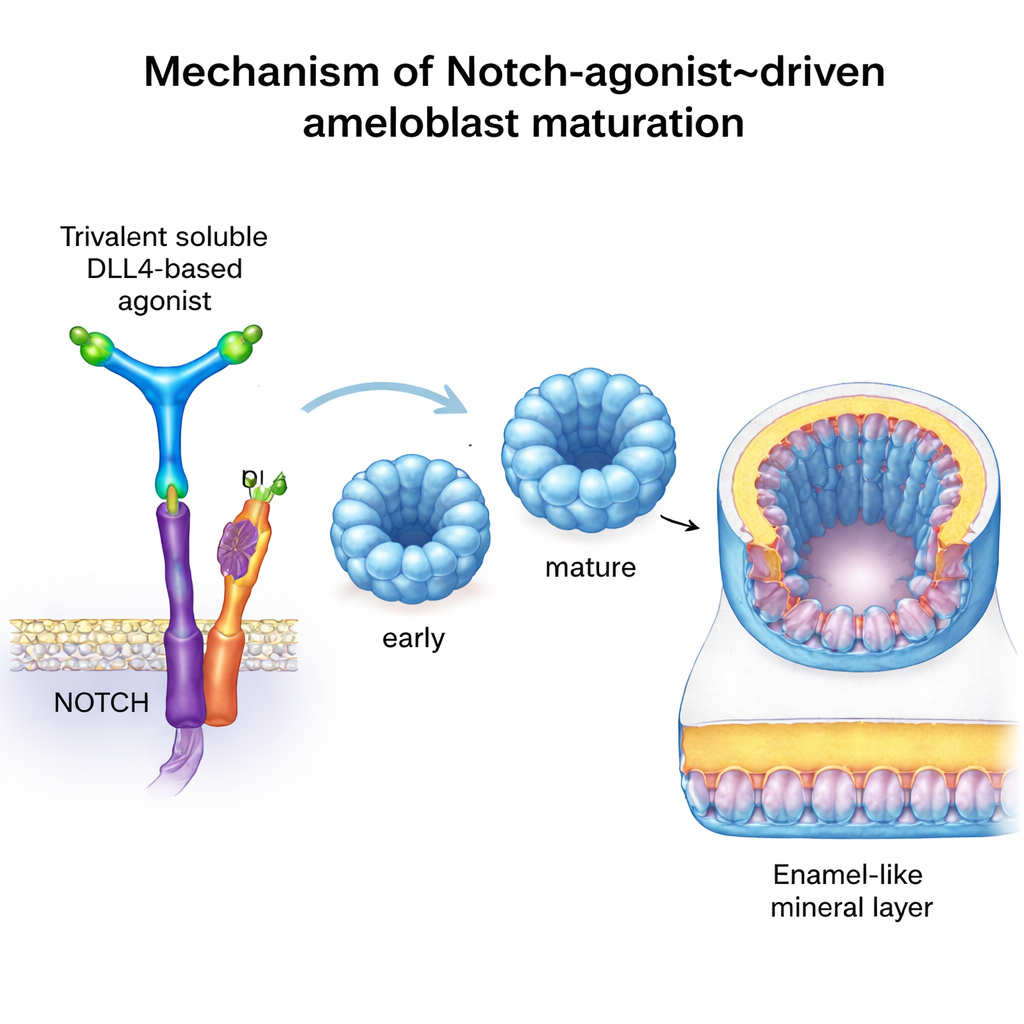
Rozwiązanie genetycznej zagadki słabego szkliwa
Badanie zajmuje się także długo nierozwiązanym problemem związanym z genem DLX3, którego mutacje powodują niektóre dziedziczne wady szkliwa i zwiększają ryzyko próchnicy. DLX3 jest aktywny zarówno w ameloblastach, jak i odontoblastach, co utrudnia określenie, która populacja komórek jest najbardziej dotknięta, gdy coś idzie nie tak. Korzystając z systemu organoidów pozbawionego odontoblastów i edycji genów metodą CRISPR, badacze usunęli DLX3 specyficznie w linii ameloblastów. Wczesne etapy formowania ameloblastów wciąż zachodziły, ale końcowa faza dojrzewania załamała się: kluczowe białka szkliwa, takie jak enamelina, AMELX, MMP20, KLK4, TUFT1 i WDR72, zostały drastycznie zredukowane zarówno na poziomie RNA, jak i białka. To pokazuje, że DLX3 jest bezpośrednio wymagany wewnątrz ludzkich ameloblastów do ukończenia programu wytwarzania szkliwa, co pomaga wyjaśnić, dlaczego warianty w pobliżu tego genu wiążą się z kruchymi zębami podatnymi na próchnicę.
Co to może znaczyć dla przyszłej opieki stomatologicznej
Razem te odkrycia przedstawiają krok po kroku drogowskaz od komórek macierzystych do organoidów produkujących szkliwo i dalej do tkanki przypominającej szkliwo in vivo, kontrolowany przez regulowany „włącznik” Notch i gen DLX3. Chociaż kliniczna regeneracja zębów jest nadal odległa, praca ta dostarcza potężnego pola doświadczalnego do badania genetycznych chorób zębów, przesiewania nowych terapii i dopracowywania strategii odbudowy utraconego szkliwa za pomocą żywych komórek zamiast materiałów obojętnych. Dla pacjentów długoterminowa nadzieja jest taka, że wizyty u dentysty mogą kiedyś polegać na naprawie startego lub zepsutego zęba bioinżynieryjnym szkliwem, które zachowuje się znacznie bardziej jak prawdziwe szkliwo.
Cytowanie: Patni, A.P., Mout, R., Alghadeer, A. et al. Soluble Notch agonist enables human ameloblast maturation and enamel-like tissue formation for tooth regeneration. Int J Oral Sci 18, 25 (2026). https://doi.org/10.1038/s41368-026-00429-4
Słowa kluczowe: regeneracja szkliwa, organoidy ameloblastów, szlak sygnałowy Notch, DLX3, komórki macierzyste zębów