Clear Sky Science · pl
Gli2 i Gli3 synergistycznie pośredniczą w sprzężeniu HH–TGF-β w mezenchymalnych komórkach progenitorowych, aby zorganizować morfogenezę korzenia zęba
Dlaczego korzenie zębów są ważniejsze, niż myślisz
Większość z nas myśli o zębach tylko wtedy, gdy bolą lub gdy widzimy je w lustrze. Jednak to, co osadza każdy ząb w szczęce — korzeń — jest równie istotne jak widoczna korona. Zdrowe korzenie utrzymują zęby stabilnie podczas żucia i mówienia przez całe życie. W tym badaniu zbadano, jak maleńkie sygnały w tkankach szczęki mówią niedojrzałym komórkom, jak zbudować mocne korzenie zębów — prace, które pewnego dnia mogą pomóc zapobiegać lub naprawiać wady korzeni prowadzące do rozchwianych zębów i ich utraty.
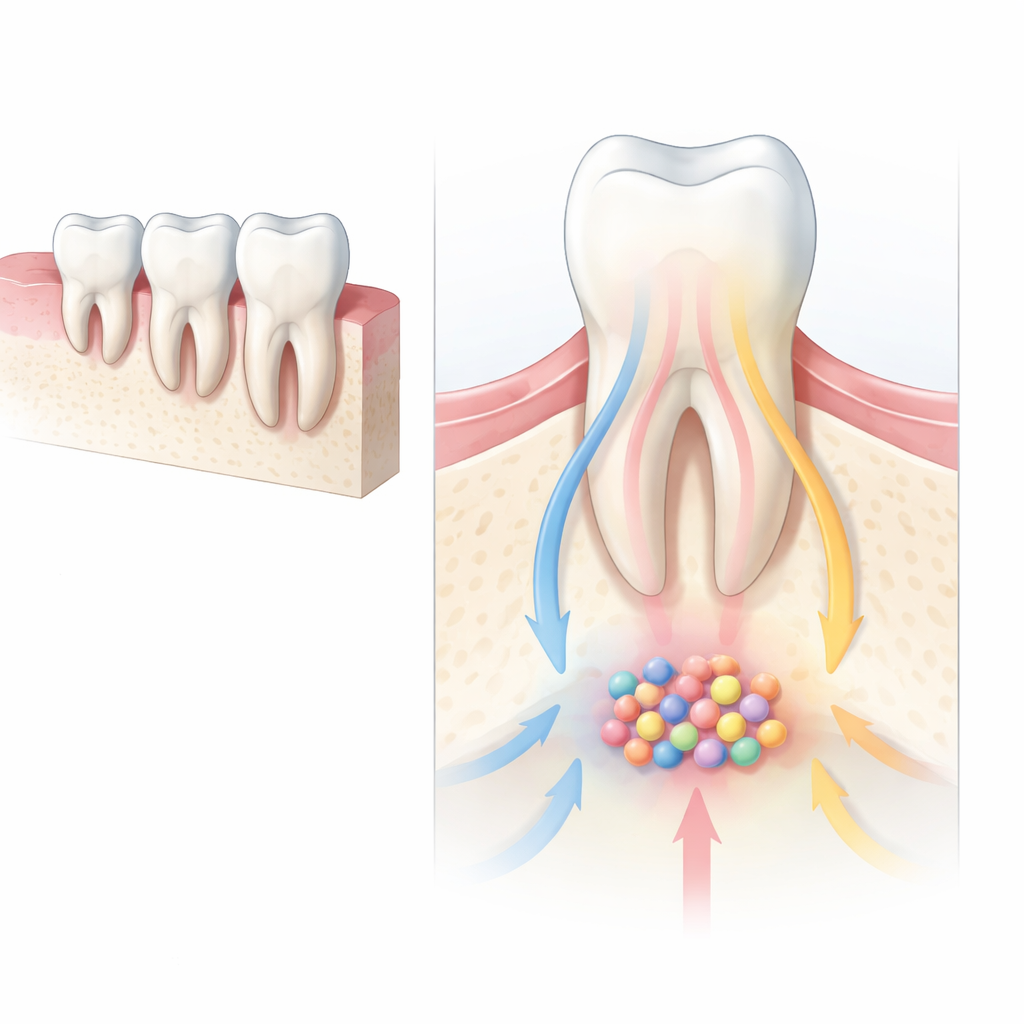
Wędrujące komórki, które budują nasze twarze
We wczesnym etapie rozwoju specjalna populacja komórek zwana czaszkowymi komórkami grzebieniowymi migruje do formującej się twarzy i szczęk, gdzie przekształca się w kość, chrząstkę i tkanki wspierające zęby. Gdy ta przemiana przebiega nieprawidłowo, noworodki mogą rodzić się z poważnymi wadami twarzowo‑zgryzowymi i stomatologicznymi. Kluczowy sygnał kierujący tymi komórkami to szlak Hedgehog, działający jak molekularny GPS, pomagający komórkom zdecydować, dokąd iść i czym się stać. Autorzy skupili się na dwóch białkach pomocniczych kontrolowanych przez Hedgehog — Gli2 i Gli3 — aby sprawdzić, jak wspólnie kierują komórkami, które ostatecznie budują korzenie trzonowców u myszy.
Dwa genowe przełączniki działające zespołowo
Wykorzystując precyzyjnie zaprojektowane modele myszy, badacze selektywnie wyłączali Gli2, Gli3 lub oba w populacji progenitorów tworzących korzeń, położonej w pobliżu rosnących końcówek korzeni. Usunięcie samego Gli2 niemal nie wpłynęło na formowanie korzenia, natomiast brak Gli3 spowodował wyraźnie krótsze korzenie, opóźnione wyrzynanie się zębów i mniejszą ilość kości podporowej wokół zębów. Gdy usunięto zarówno Gli2, jak i Gli3, problemy stały się znacznie poważniejsze: korzenie miały około połowy normalnej długości, wyrzynanie było opóźnione, a kość otaczająca korzenie była znacznie zredukowana. Te eksperymenty pokazują, że Gli2 i Gli3 nie działają w izolacji; współpracują, kształtując korzeń i otaczające go struktury podporowe.
Ukierunkowywanie komórek do właściwych zadań
Aby zrozumieć, dlaczego korzenie zawodziły, zespół dokładnie przyjrzał się, w co normalnie przekształcają się progenitory korzenia. W zdrowych zębach komórki te dają początek odontoblastom produkującym zębiny we wnętrzu korzenia, włóknistym komórkom więzadła przyczepiającego korzeń do kości oraz komórkom tworzącym kość w zębodole. Gdy brakowało Gli3, a zwłaszcza obu Gli2 i Gli3, te linie różnicowania zostały zaburzone: kluczowe markery tożsamości zębiny i więzadła były znacznie zmniejszone, a w pobliżu korzeni pojawiło się mniej komórek kościotwórczych. Śledzenie potomków komórek progenitorowych wykazało, że zamiast zasiedlać korzeń i jego więzadło, wiele z tych komórek pozostawało wyżej w obrębie zęba, co wskazuje, że ich normalne „ścieżki kariery” zostały wykolejone. Jednocześnie spadła liczba dzielących się komórek w rejonie korzenia, więc było mniej elementów budulcowych potrzebnych do skonstruowania korzenia.
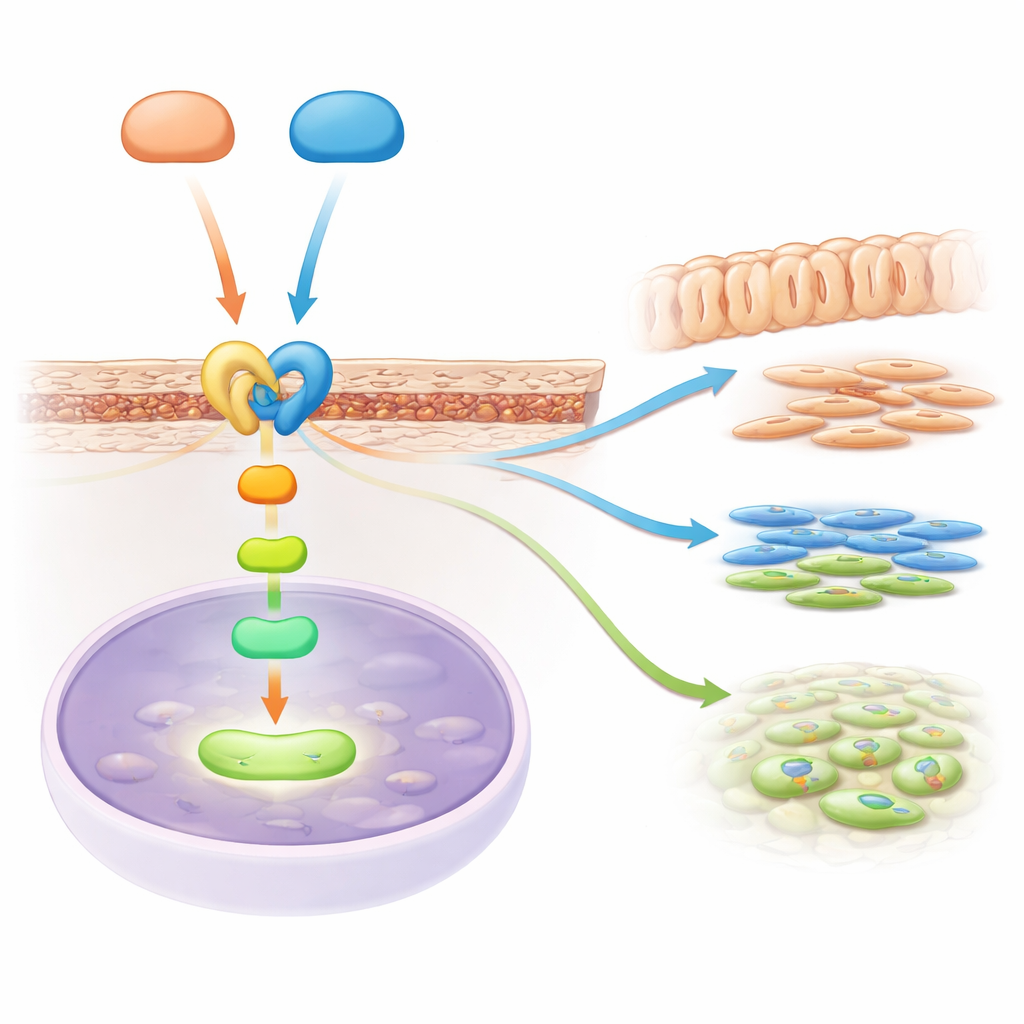
Przekaźnik sygnałowy łączący dwa główne szlaki
Historia nie zakończyła się na sygnalizacji Hedgehog. Analizując, które geny były włączone lub wyłączone, naukowcy odkryli, że inny ważny szlak, sygnalizacja TGF‑beta, był stłumiony po utracie Gli2 i Gli3. TGF‑beta jest dobrze znane z promowania tworzenia zębiny i kości. Zespół zidentyfikował kluczową cząsteczkę przekaźnikową — receptor o nazwie Acvr2b — który znajduje się na powierzchni progenitorów korzenia i pomaga przekazywać sygnały rodziny TGF‑beta do wnętrza komórki. Wykazali, że zarówno Gli2, jak i Gli3 fizycznie wiążą się z regionem kontrolnym genu Acvr2b, zwiększając jego aktywność. Bez tych pomocników poziomy Acvr2b w obrębie korzenia spadły, a wewnątrzkomórkowe przekaźniki TGF‑beta były mniej aktywne, osłabiając instrukcje napędzające wzrost i różnicowanie korzenia.
Częściowe przeprogramowanie wadliwego programu budowy korzenia
Aby sprawdzić, czy przywrócenie sygnalizacji TGF‑beta może pomóc, badacze leczyli myszy pozbawione obu Gli2 i Gli3 lekiem stymulującym ten szlak. Chociaż nie udało się w pełni odtworzyć normalnych korzeni, leczenie wydłużyło korzenie, zwiększyło ilość otaczającej kości i poprawiło tworzenie zębiny oraz tkanki więzadła w porównaniu z nieleczonymi mutantami. To częściowe „ocalenie” sugeruje, że łańcuch Gli2/Gli3–Acvr2b–TGF‑beta jest główną drogą, dzięki której sygnały Hedgehog przekształcane są w strukturalny wzrost korzeni zębów.
Co to znaczy dla przyszłej opieki dentystycznej
Mówiąc prosto, praca ta pokazuje, że dwa genetyczne „przełączniki”, Gli2 i Gli3, współdziałają, aby pomóc młodym komórkom szczęki wyczuwać sygnały Hedgehog i, poprzez przekaźnik z udziałem TGF‑beta, decydować o przekształceniu się w wyspecjalizowane komórki budujące i wspierające korzenie zębów. Gdy ta komunikacja zawodząc, korzenie są krótkie, zęby wyrzynają się słabo, a kość podporowa jest cienka. Zrozumienie tej sieci sygnałowej nie tylko wyjaśnia, jak powstają normalne korzenie zębów, lecz także wskazuje nowe strategie kierowania komórkami macierzystymi lub progenitorowymi w celu naprawy uszkodzonych korzeni lub ich regeneracji w przyszłych terapiach dentystycznych.
Cytowanie: Zhou, T., Huang, L., Xie, Y. et al. Gli2 and Gli3 synergistically mediate HH-TGF-β crosstalk in mesenchymal progenitor cells to orchestrate tooth root morphogenesis. Int J Oral Sci 18, 30 (2026). https://doi.org/10.1038/s41368-026-00427-6
Słowa kluczowe: rozwój korzenia zęba, czaszkowe komórki grzebieniowe, sygnalizacja Hedgehog, szlak TGF-beta, komórki macierzyste zębowe