Clear Sky Science · pl
Atlas transkrypcyjny pojedynczych komórek ujawnia odrębne mechanizmy komunikacji między układem odpornościowym a chondrocytami w zwyrodnieniu stawu skroniowo‑żuchwowego wywołanym różnymi rodzajami zaburzeń zwarcia
Dlaczego ważny jest staw żuchwowy
Małe stawy przed uszami, zwane stawami skroniowo‑żuchwowymi (TMJ), umożliwiają mówienie, żucie, ziewanie i śmiech. Gdy rozwija się w nich choroba zwyrodnieniowa, codzienne czynności mogą stać się bolesne i utrudnione. Niniejsze badanie wykorzystuje nowoczesną analizę genów na poziomie pojedynczych komórek u myszy, by przyjrzeć się tym stawom komórka po komórce, ujawniając, jak różne problemy z zwarciem prowadzą do odmiennych typów uszkodzeń — i jak to może wpłynąć na bardziej precyzyjne terapie.
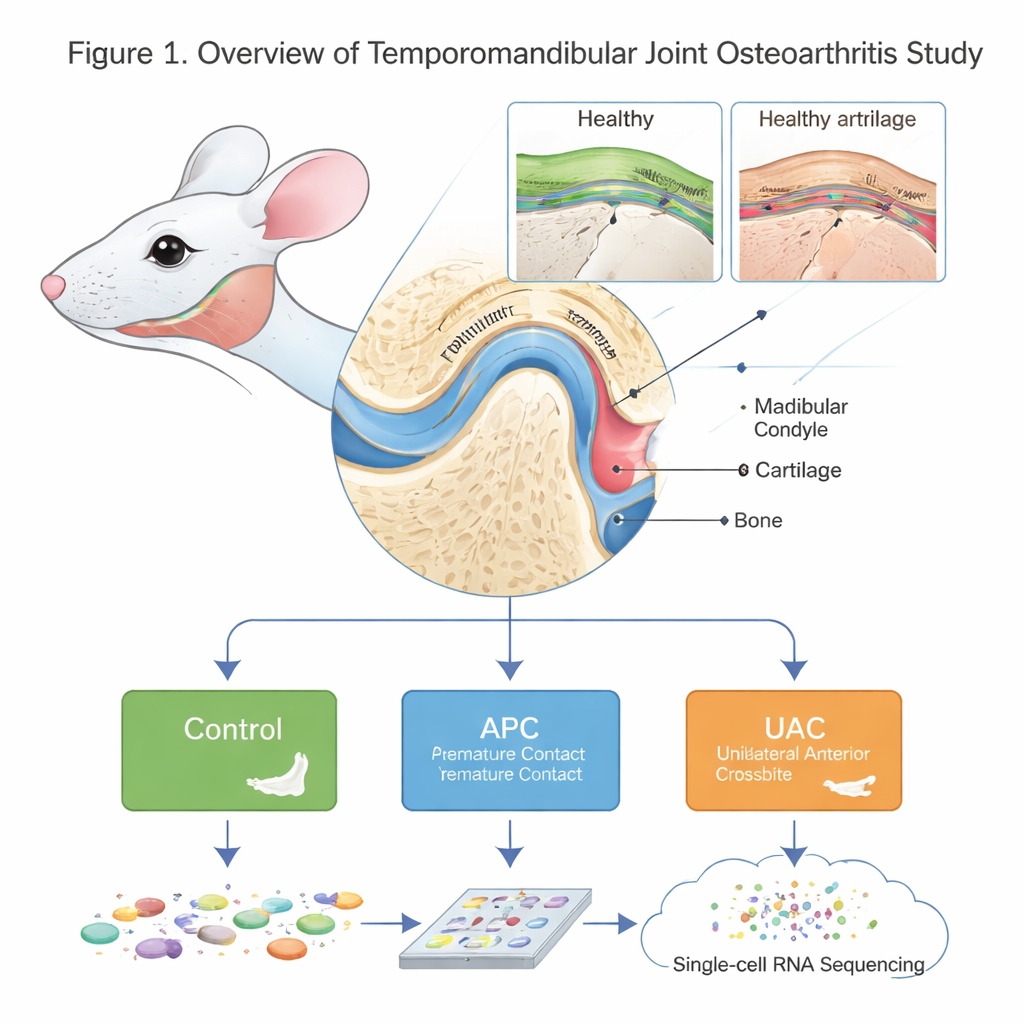
Dokładne spojrzenie na mały, lecz złożony staw
TMJ to nie prosty zawias. Jego zaokrąglony koniec, kłykieć żuchwy, jest pokryty specjalnym rodzajem chrząstki i podparty przez leżącą poniżej kość. Zwyrodnienie tego stawu (TMJOA) powoduje ból, sztywność i utratę funkcji, ale jego mikroskopowe i molekularne przyczyny trudno było rozplątać. Autorzy stworzyli szczegółowy „atlas komórkowy” kłykcia myszy w zdrowiu i chorobie, używając sekwencjonowania RNA pojedynczych komórek — techniki pozwalającej odczytać, które geny są aktywne w tysiącach pojedynczych komórek. Porównali zdrowe myszy z dwoma modelami zaburzeń zwarcia — przednim przedwczesnym kontaktem (APC), gdy przednie zęby stykają się zbyt wcześnie, oraz jednostronnym przednim zgryzem krzyżowym (UAC), gdy jedna strona przednich zębów gryzie nieprawidłowo — oboma znanymi z nadmiernego obciążania stawu żuchwowego.
Wiele rodzajów komórek chrząstki, nie tylko jeden
Tradycyjnie chrząstkę kłykcia opisywano w szerokich warstwach — komórki proliferujące, dojrzałe i hipertroficzne. To badanie pokazuje, że rzeczywistość jest znacznie bardziej zróżnicowana. Zespół zidentyfikował wiele podtypów chondrocytów, z których każdy ma własny profil ekspresji genów i prawdopodobną rolę. Stwierdzono komórki progenitorowe blisko powierzchni zachowujące się jak pula naprawcza, chondrocyty włókniste związane z macierzą przypominającą bliznę i gojeniem, chondrocyty związane z zapaleniem produkujące sygnały zapalne, chondrocyty związane z mineralizacją i hipertroficzne uczestniczące w przekształcaniu chrząstki w kość oraz komórki naprawcze tłumiące stres i zapalenie. W zdrowych stawach te podtypy układają się w uporządkowany układ przestrzenny i podążają płynną „trajektorią” rozwojową od progenitorów do stanów bardziej dojrzałych.
Gdy problemy z zwarciem zaburzają porządek komórkowy stawu
Oba modele APC i UAC prowadziły do cieńszej chrząstki, chropowatości powierzchni i typowych zmian przypominających chorobę zwyrodnieniową w kłykciu. Na poziomie komórkowym odsetek chondrocytów spadł, a liczba komórek odpornościowych wzrosła. W APC nastąpił napływ określonych chondrocytów mineralizujących i hipertroficznych oraz zaburzenie normalnego przejścia od komórek progenitorowych do komórek dojrzałych. W UAC zaobserwowano również wzrost chondrocytów włóknistych i naprawczych, co sugeruje silniejszą próbę regeneracji i przebudowy. Mikroskopia potwierdziła, że komórki straciły uporządkowane warstwy i stały się zwarte oraz zdezorganizowane w chorobowo zmienionej chrząstce, zgodnie ze zakłóconymi ścieżkami rozwojowymi wywnioskowanymi z danych o ekspresji genów.
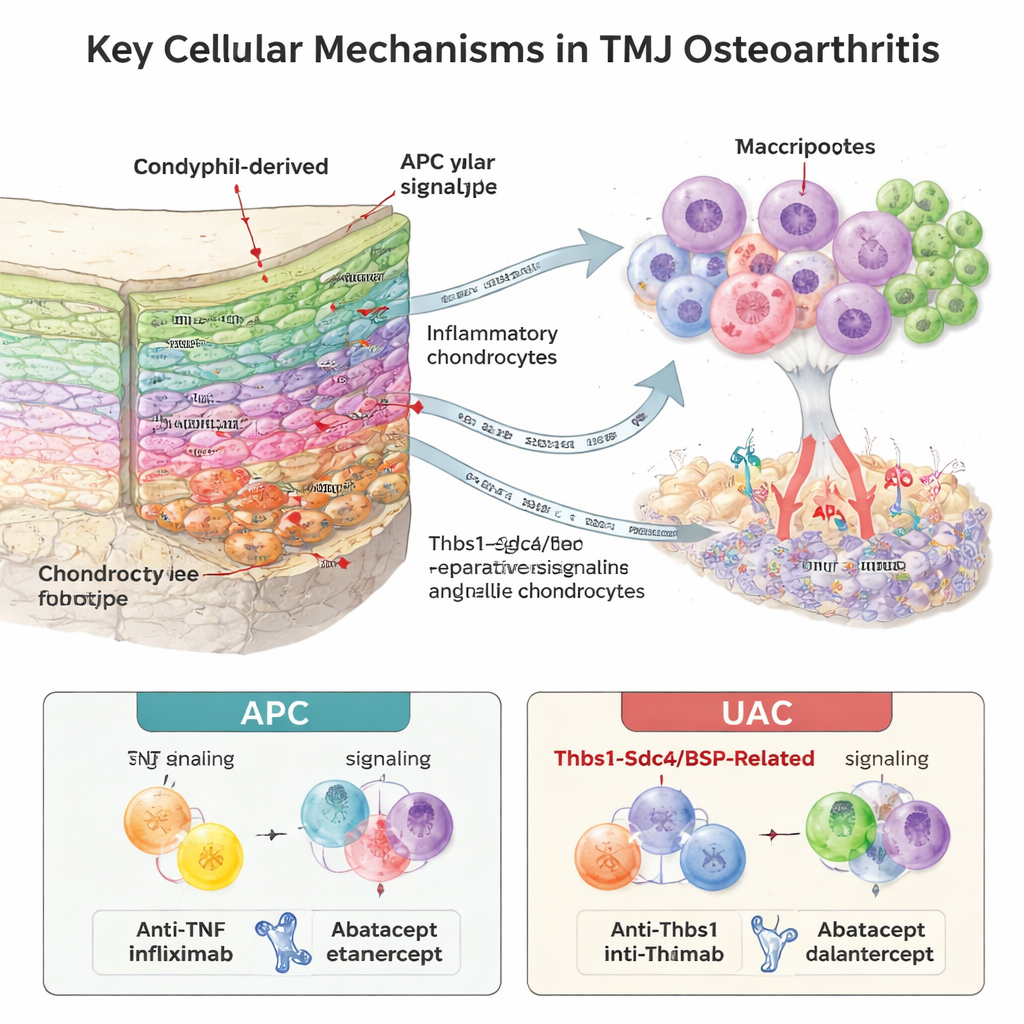
Komunikacja między komórkami odpornościowymi, naczyniami krwionośnymi i chrząstką
Kość i szpik wspierające kłykieć kryły zaskakująco bogate „mikrośrodowisko” odpornościowe. Badacze wykryli dziewięć typów komórek odpornościowych, przy czym neutrofile (szybko reagujące krwinki białe) silnie rozrosły się w chorych stawach, szczególnie na określonym etapie dojrzewania. Analizując, które cząsteczki sygnałowe i receptory współwystępują, wnioskowali o intensywnej „rozmowie” między komórkami odpornościowymi a chondrocytami. W modelu APC neutrofile stały się głównym źródłem TNF‑alfa, silnego sygnału zapalnego, wysyłającego mocne, uszkadzające komunikaty do komórek chrząstki. W modelu UAC ujawnił się inny wzorzec: sygnały związane z kością i chrząstką obejmujące sialoproteinę kostną (BSP) oraz szlak Thbs1–Sdc4 były bardziej wyraziste i silnie powiązane z nowym wzrostem naczyń krwionośnych na granicy chrząstka–kość. Obszary bogate w BSP pokrywały się z markerami angiogenezy, co sugeruje, że naciekające naczynia i rekrutowane komórki odpornościowe wspólnie napędzają erozję chrząstki.
Dopasowane terapie do różnych obciążeń stawu
Aby sprawdzić, czy te odrębne sygnały mają rzeczywiste znaczenie, zespół leczył myszy w trakcie rozwoju choroby lekami blokującymi konkretne szlaki. W TMJOA wywołanym APC blokada TNF‑alfa lekiem etanerceptem wyraźnie chroniła chrząstkę, podczas gdy lek celujący receptory przyciągające neutrofile (Navarixin) nie przyniósł większej różnicy. W przeciwieństwie do tego, w TMJOA wywołanym UAC Navarixin znacząco złagodził uszkodzenie chrząstki, co zgadza się z procesem chorobowym bardziej zależnym od inwazji naczyń prowokowanej przez neutrofile i przebudowy, podczas gdy etanercept miał słabszy efekt. Te wyniki sugerują, że zwyrodnienie stawu skroniowo‑żuchwowego to nie jedna choroba, lecz zbiór powiązanych schorzeń kształtowanych przez sposób obciążenia stawu, i że skuteczne terapie mogą wymagać dopasowania do konkretnych mechanicznych i komórkowych wzorców u danego pacjenta.
Co to oznacza dla osób z bólem żuchwy
Dla osoby borykającej się z trzeszczeniem stawu, bólem czy ograniczonym otwieraniem ust badanie to podkreśla dwie kluczowe idee. Po pierwsze, staw żuchwowy jest utrzymywany przez zróżnicowaną społeczność komórek chrząstki i odpornościowych, które w zależności od sposobu aktywacji mogą chronić lub szkodzić tkance. Po drugie, różne problemy z zwarciem mogą przesunąć tę społeczność w stronę odmiennych szkodliwych ścieżek — jedna napędzana klasycznym zapaleniem, druga przez nieprawidłowy wzrost naczyń i przebudowę kości‑chrząstki. W dłuższej perspektywie tego typu mapowanie na poziomie pojedynczych komórek może pomóc stomatologom i lekarzom wyjść poza uniwersalne podejścia terapeutyczne i przejść do strategii łączących korekcję zwarcia z dobranymi lekami, wybranymi według specyficznego wzorca uszkodzeń stawu u pacjenta.
Cytowanie: Wang, K., Li, Y., Xiang, S. et al. Single-cell transcriptional atlas reveals distinct immune-chondrocyte crosstalk mechanisms in temporomandibular joint osteoarthritis induced by different types of occlusal disorder. Int J Oral Sci 18, 22 (2026). https://doi.org/10.1038/s41368-025-00424-1
Słowa kluczowe: zwyrodnienie stawu skroniowo‑żuchwowego, sekwencjonowanie RNA pojedynczych komórek, chondrocyty, neutrofile, zaburzenie zwarcia