Clear Sky Science · pl
Implantacja uaktywnia okołoprotezowy potencjał osteogeniczny poprzez mechanotransdukcję osi Snx5–EGFR
Dlaczego zachowanie kości szczęki po utracie zęba ma znaczenie
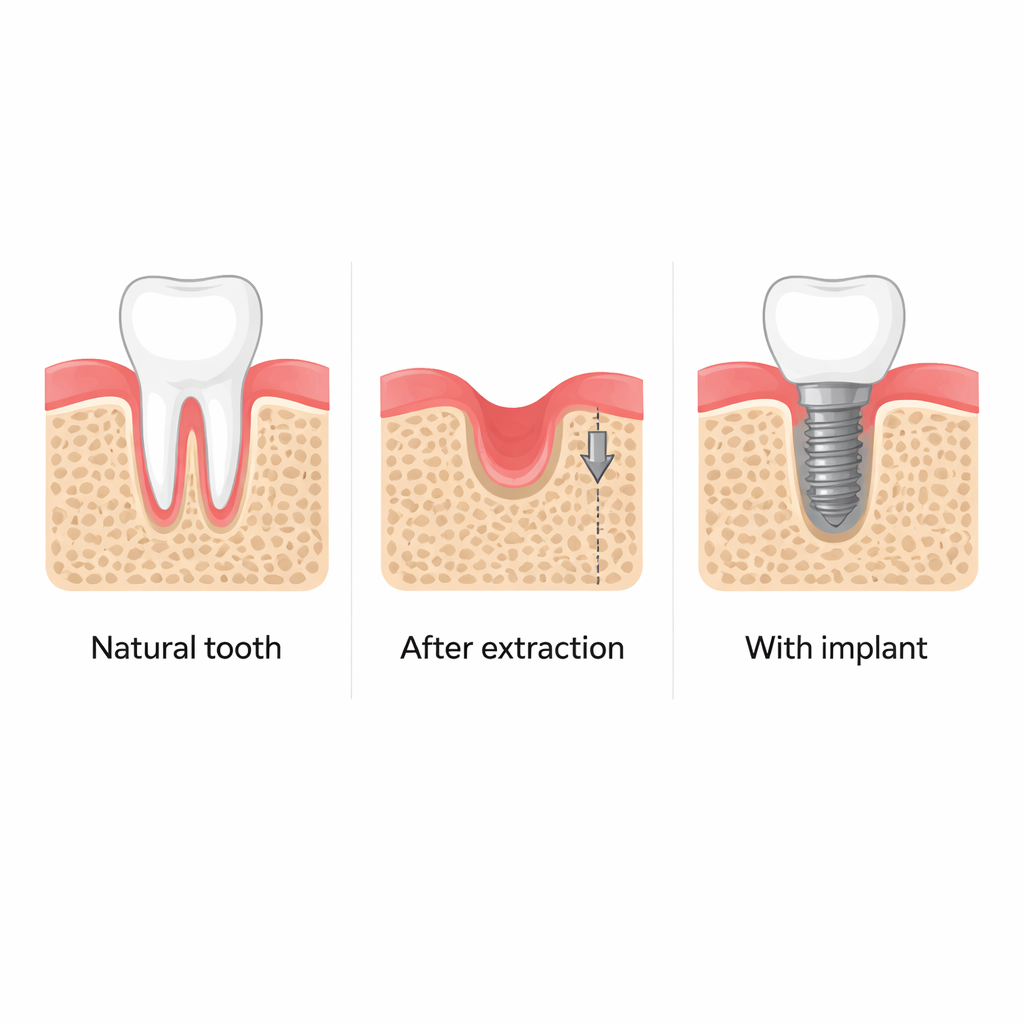
Po usunięciu zęba otaczająca kość szczęki często ulega zanikowi, co utrudnia późniejsze umieszczenie stabilnych implantów i wpływa na wygląd twarzy. Stomatolodzy od dawna zauważają, że samo osadzenie implantu w świeżym zębodole wydaje się chronić tę kość, nawet zanim implant zacznie służyć do żucia. Badanie stawia proste, lecz istotne pytanie: w jaki sposób sam akt wkręcania implantu „budzi” system naprawczy kości i czy można wykorzystać ten proces do poprawy regeneracji szczęki?
Implanty jako dyskretni ochroniarze kości
Skany kliniczne od pacjentów oraz szczegółowe eksperymenty na myszach potwierdzają, że wstawienie implantu niedługo po ekstrakcji pomaga zachować wysokość i grubość otaczającej kości szczęki. Natomiast zębodole pozostawione do samoistnego gojenia tracą znaczną część kości w ciągu kilku miesięcy. Wokół implantów badacze znaleźli więcej niezróżnicowanych komórek tworzących kość (osteoprogenitorów), co wskazuje, że tkanka przy metalowym trzpieniu jest biologicznie bardziej aktywna. Ta zwiększona aktywność wydaje się być napędzana nie przez siły żucia, lecz przez nietypowe naprężenia mechaniczne powstające, gdy ciasny implant jest wkręcany w nieco za mały otwór w kości.
Ukryty przełącznik w komórkach macierzystych kości
Zespół skupił się na szczególnej populacji komórek macierzystych szpiku kostnego oznaczonych białkiem LepR, znanych jako kluczowi dostawcy nowej kości u dorosłych. Porównując aktywność genów w tych komórkach pochodzących z normalnej kości, z kości sąsiadującej z implantem oraz z komórek poddanych stresowi w warunkach laboratoryjnych, wyodrębnili jedną cząsteczkę — sorting nexin 5 (Snx5) — której poziomy konsekwentnie spadały w obecności sygnałów mechanicznych. W obrębie przyimplantacyjnej tkanki komórki LepR z niskim poziomem Snx5 częściej wykazywały markery wczesnych komórek kostnych, co sugeruje, że obniżenie Snx5 pomaga pchnąć te „uciszone” komórki macierzyste w stronę aktywnego stanu budowania kości.
Gdy przełącznik zawodzi, kość nie odczuwa siły prawidłowo
Aby sprawdzić funkcję Snx5, badacze użyli myszy i komórek macierzystych pozbawionych tego białka. Bez Snx5 komórki macierzyste wykazywały silną wrodzoną skłonność do tworzenia kości, nawet bez dodatkowej stymulacji. Jednak po zastosowaniu rozciągania mechanicznego — naśladującego naprężenia wokół implantu — komórki normalne zwiększały aktywność osteogeniczną, podczas gdy komórki pozbawione Snx5 praktycznie nie reagowały. U żywych myszy implanty w normalnych osobnikach indukowały wyraźny przyrost nowej kości wokół tytanowego trzpienia. Natomiast myszy bez Snx5 nie zyskiwały dodatkowej kości po implantacji, co ujawniło, że Snx5 jest kluczowy dla przekształcania sygnałów mechanicznych w dodatkową naprawę kostną, a nie dla samego podstawowego tworzenia kości.
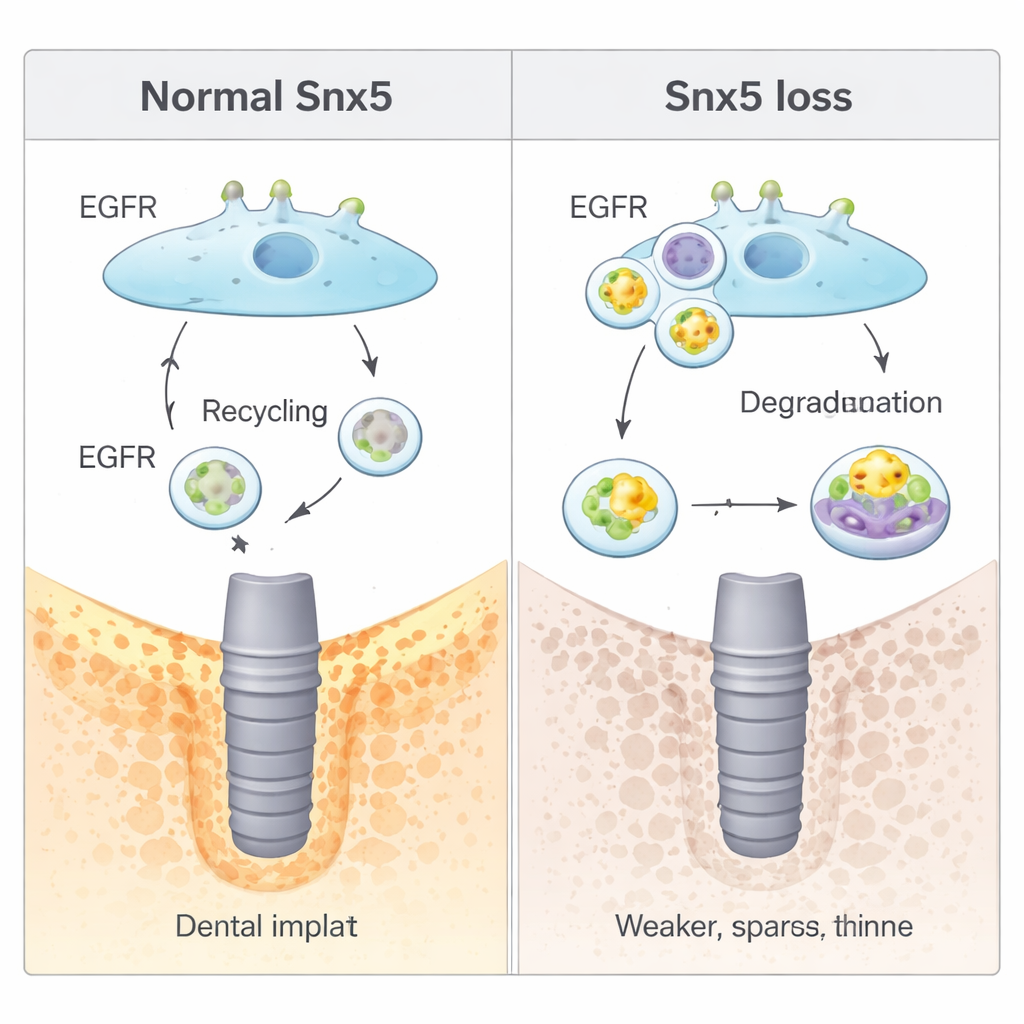
Jak szlak recyklingu kontroluje sygnały kostne
Badanie następnie ujawniło mechanizm działania Snx5 na poziomie molekularnym. Wiele sygnałów wzrostowych w komórkach przechodzi przez receptory na powierzchni komórki, które są nieustannie wciągane do wnętrza i albo recyklingowane, albo degradowane. Snx5 należy do rodziny białek „sortujących”, które kierują tym ruchem. Tutaj pokazano, że Snx5 steruje receptorami czynnika wzrostu naskórka (EGFR) — kluczowego regulatora wzrostu komórek i różnicowania kostnego — kierując je z powrotem na błonę komórkową po internalizacji. Gdy Snx5 brakowało, więcej EGFR było kierowane do „trawiennych” przedziałów komórkowych (lizosomów) i ulegało degradacji. To osłabienie sygnalizacji EGFR niespodziewanie zwiększało bazowe tworzenie kości, ale pozostawiało komórki mniej zdolne do dostosowania się, gdy zmieniały się siły mechaniczne. Leki sztucznie aktywujące EGFR osłabiły nadmierne tworzenie kości obserwowane przy braku Snx5, podczas gdy inhibitory degradacji lizosomalnej przywracały sygnał EGFR i ponownie zmniejszały osteogenezę.
Co to oznacza dla przyszłych pacjentów z implantami
Dla laika wyniki te sugerują, że kość szczęki ma wbudowany system potrafiący wyczuć subtelne pociągnięcia i naciski powstające podczas osadzania implantu i przetłumaczyć je na dodatkowy wzrost kości. Snx5 działa jak kontroler ruchu, który utrzymuje kluczowy receptor wzrostu, EGFR, w cyklu na właściwym poziomie, dzięki czemu komórki macierzyste kości mogą „usłyszeć” i odpowiedzieć na te mechaniczne sygnały. Gdy ten kontroler jest zmieniony, kość może tworzyć się łatwiej w spoczynku, ale traci precyzyjną reakcję na siłę. Zrozumienie osi Snx5–EGFR otwiera drogę do nowych terapii — leków lub powłok na implantach — które mogłyby regulować mechanyczną czułość kości, pomagając zachować strukturę szczęki i poprawić powodzenie implantów w trudnych przypadkach klinicznych.
Cytowanie: Jiang, X., Weng, Y., Feng, Y. et al. Implantation awakens peri-implant osteogenic potential via Snx5-EGFR axis-mediated mechanical transduction. Int J Oral Sci 18, 18 (2026). https://doi.org/10.1038/s41368-025-00423-2
Słowa kluczowe: implanty dentystyczne, regeneracja kości szczęki, mechanotransdukcja, komórki macierzyste kości, szlak sygnalizacji EGFR