Clear Sky Science · pl
KDM6B/Pdk1 napędzana przez glikolizę laktylacja ZEB2 wspomaga tworzenie cementum komórkowego
Dlaczego ochrona korzeni zębów ma znaczenie
Choroba dziąseł, czyli zapalenie przyzębia, jest jedną z głównych przyczyn utraty zębów u dorosłych. W miarę postępu choroba stopniowo niszczy tkanki kotwiczące zęby w szczęce. Jedną z najważniejszych jest cementum — cienka, przypominająca kość warstwa pokrywająca powierzchnię korzenia, dzięki której ząb „wiąże się” z otaczającymi więzadłem i kością. Gdy cementum zostaje utracone, zęby stają się luźne i mogą w końcu wypaść. W badaniu postawiono proste, ale istotne pytanie: czy możemy zrozumieć na poziomie molekularnym, jak powstaje cementum, aby pewnego dnia pomóc organizmowi je odbudować i utrzymać zęby przez całe życie?
Od komórek podpierających ząb do celu leczniczego
Cementum powstaje dzięki wyspecjalizowanym komórkom zwanym cementoblastami, które osiadają na powierzchni korzenia i odkładają nowy materiał zmineralizowany. Komórki te zachowują się podobnie do osteoblastów, komórek tworzących kość, ale sygnały kierujące tym, kiedy i jak budują cementum, były słabo poznane. Badacze skupili się na cząsteczce zwanej KDM6B — enzymie modyfikującym chemiczne znaczniki na białkach związanych z DNA, co może uruchamiać geny. Analizując zęby myszy w różnych wieku oraz cementoblasty hodowane w laboratorium, stwierdzili, że poziom KDM6B rośnie w aktywnej fazie tworzenia cementum, a spada, gdy wzrost ustaje. Zablokowanie KDM6B w komórkach lub u myszy obniżało aktywność cementoblastów, a część „komórkowa” cementum — grubszy, żywy fragment przy wierzchołku korzenia — ulegała ścieńczeniu, co sugeruje, że KDM6B jest kluczowym promotorem zdrowego wzrostu cementum.
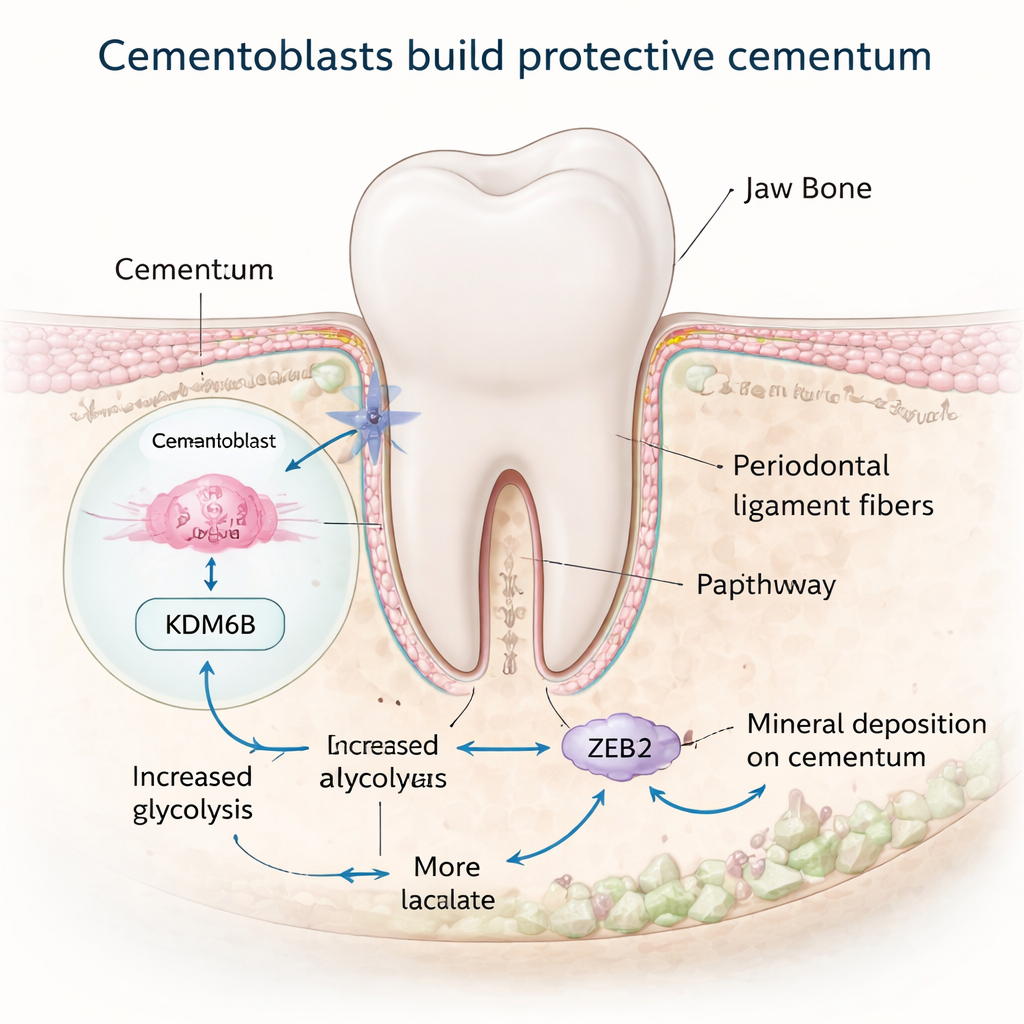
Przeprogramowanie metabolizmu komórek, by budować mineral
Tworzenie tkanki zmineralizowanej wymaga dużo energii, i wiele komórek przełącza swój metabolizm na wydajniejszy tryb podczas tego procesu. Zespół odkrył, że KDM6B pomaga cementoblastom zmienić sposób wykorzystywania cukru. Normalnie te komórki preferują ścieżkę zwaną glikolizą, która szybko rozkłada glukozę i wytwarza laktonian (mlekowy). Gdy KDM6B był zmniejszony, geny zaangażowane w glikolizę ulegały wyciszeniu, podczas gdy te związane z wolniejszą, zależną od tlenu produkcją energii były mieszane lub podwyższone, a komórki wytwarzały mniej energii ogółem. Centralną rolę w tym przesunięciu odgrywał enzym PDK1. Dzięki narzędziom mapowania genomu badacze wykazali, że KDM6B fizycznie usuwa represyjny znacznik z regionu DNA kontrolującego gen Pdk1, co pozwala na wzrost poziomu PDK1. Przywrócenie PDK1 w komórkach pozbawionych KDM6B odnowiło wiele markerów tworzenia minerału, ujawniając metaboliczny przełącznik KDM6B–PDK1, który napędza cementoblasty.
Przemiana mleczanu z odpadu w użyteczny sygnał
Mleczan bywa postrzegany jako produkt uboczny ciężko pracujących mięśni, ale ostatnie badania pokazują, że może też pełnić rolę sygnałową modyfikując białka. Tutaj wyższa glikoliza napędzana przez KDM6B i PDK1 zwiększała produkcję mleczanu w cementoblastach. Naukowcy następnie śledzili nowy rodzaj modyfikacji białek zwany laktylacją, w której pochodne mleczanu przyłączają się do określonych miejsc białek. Stwierdzili, że poziomy laktylacji w cementoblastach rosły w okresach aktywnego tworzenia cementum, a spadały u starszych myszy i w komórkach pozbawionych KDM6B. Dodanie prostego chlorku sodu mleczanu podniosło laktylację, ożywiło geny związane z mineralizacją i przywróciło powstawanie grudek mineralnych zarówno w hodowlach komórkowych, jak i w modelu myszy, nawet gdy KDM6B był zablokowany. To sugeruje, że sam mleczan może pomóc uratować osłabioną aktywność budowania cementum.
Molekularny impuls dla kluczowego regulatora cementum
Zespół zapytał następnie, które białka są „ozdabiane” przez laktylację w sposób istotny dla cementum. Skoncentrowali się na ZEB2, białku regulującym geny, znanym już z promowania mineralizacji cementoblastów. Przy użyciu technik mapowania białek zidentyfikowali konkretne miejsca na ZEB2 noszące znaki laktylacji i pokazali, że zmiana jednego krytycznego miejsca osłabia zdolność komórki do uruchamiania genów mineralizacyjnych. Dalsze eksperymenty wykazały, że szlak KDM6B–PDK1 zwiększa laktylację ZEB2, a dostarczenie dodatkowego mleczanu może przywrócić aktywność ZEB2, gdy poziom PDK1 jest niski. W istocie metabolizm i kontrola genów są powiązane: rozkład cukru zasila produkcję mleczanu, który następnie dopracowuje ZEB2, utrzymując programy budowy cementum w sile.
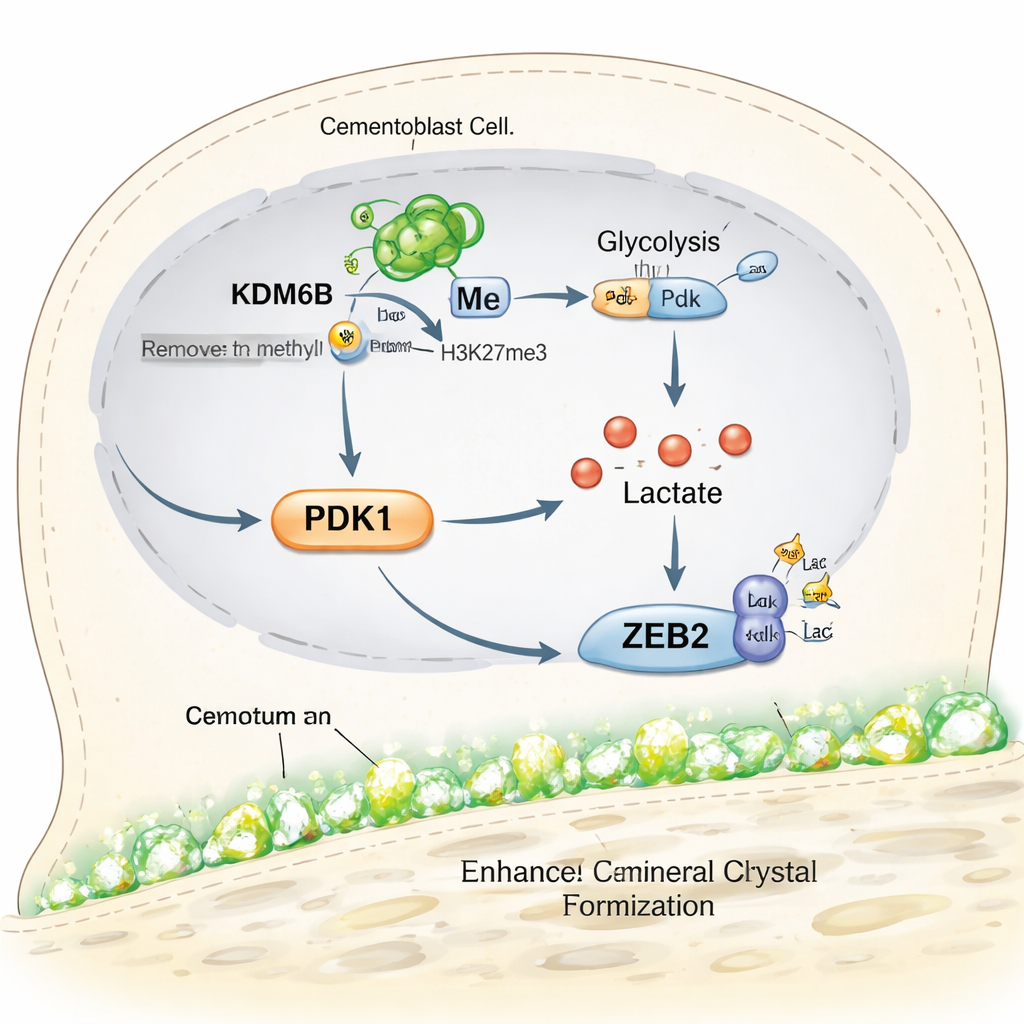
Co to oznacza dla przyszłych terapii ratujących zęby
Mówiąc krótko, badanie ujawnia łańcuch zdarzeń w komórkach tworzących cementum: enzym KDM6B otwiera gen Pdk1, PDK1 przesuwa komórki w kierunku szybkiego wykorzystania cukru, ten metabolizm generuje mleczan, a mleczan chemicznie reguluje białko ZEB2, aby napędzać odkładanie minerału. Gdy którykolwiek krok tego łańcucha zostanie zablokowany, wzrost cementum słabnie, ale ostrożne dodanie mleczanu może częściowo go przywrócić. Dla pacjentów praca ta nie przekłada się jeszcze na terapię kliniczną, ale wskazuje nowe, precyzyjne cele dla leków lub biomateriałów zaprojektowanych do regeneracji cementum i stabilizacji zębów w zaawansowanym zapaleniu przyzębia. Sugeruje też, że podobne metaboliczne „przełączniki” można wykorzystać do wspierania gojenia kości w innych częściach ciała.
Cytowanie: Yang, Z., Wang, H., Xiao, J. et al. KDM6B/Pdk1 glycolytic pathway-driven ZEB2 lactylation promotes cellular cementum formation. Int J Oral Sci 18, 21 (2026). https://doi.org/10.1038/s41368-025-00420-5
Słowa kluczowe: regeneracja cementum, zapalenie przyzębia, metabolizm cementoblastów, demetylaza histonowa KDM6B, laktylacja białek