Clear Sky Science · pl
Wgląd strukturalny w mutacje związane z chorobami w maszynerii przetwarzania mikroRNA
Jak drobne nożyczki RNA kształtują zdrowie i choroby
W każdej komórce działa ukryty system edycyjny, który przycina komunikaty genetyczne zanim zostaną odczytane. System ten opiera się na maleńkich fragmentach RNA zwanych mikroRNA, które działają jak precyzyjne regulatory tysięcy genów jednocześnie. Gdy molekularne „maszyny” wytwarzające mikroRNA funkcjonują prawidłowo, komórki rosną, dzielą się i specjalizują w sposób kontrolowany. Gdy jednak te maszyny ulegają uszkodzeniu na skutek mutacji, równowaga aktywności genów może przesunąć się w stronę nowotworów, zaburzeń krwi lub problemów w rozwoju mózgu. Artykuł wyjaśnia, jak zrozumienie trójwymiarowych kształtów tych maszyn pomaga naukowcom wskazać, co idzie nie tak i jak można to potencjalnie naprawić.
Komórkowe narzędzie do przyciszania genów
MikroRNA to krótkie fragmenty RNA, liczące około 22 nukleotydów, które same w sobie nie kodują białek. Zamiast tego przyczepiają się do dłuższych matryc mRNA i albo oznaczają je do zniszczenia, albo blokują ich translację, skutecznie przyciszając geny zamiast je całkowicie wyłączać. Aby wytworzyć mikroRNA, komórka przepuszcza dłuższe prekursory RNA przez wieloetapową linię montażową. Najpierw enzym DROSHA przycina masywne pierwotne transkrypty w jądrze komórkowym do krótszych fragmentów o kształcie pętelki. Te fragmenty przemieszczają się następnie do cytoplazmy, gdzie inny enzym, DICER, mierzy i tnie je na dupleksy o wielkości mikroRNA. W końcu jedna nić każdego dupleksu jest wczytywana do białka Argonaute 2 (AGO2), które wykorzystuje mikroRNA jako przewodnik do odnajdywania pasujących komunikatów i ich wyciszania. 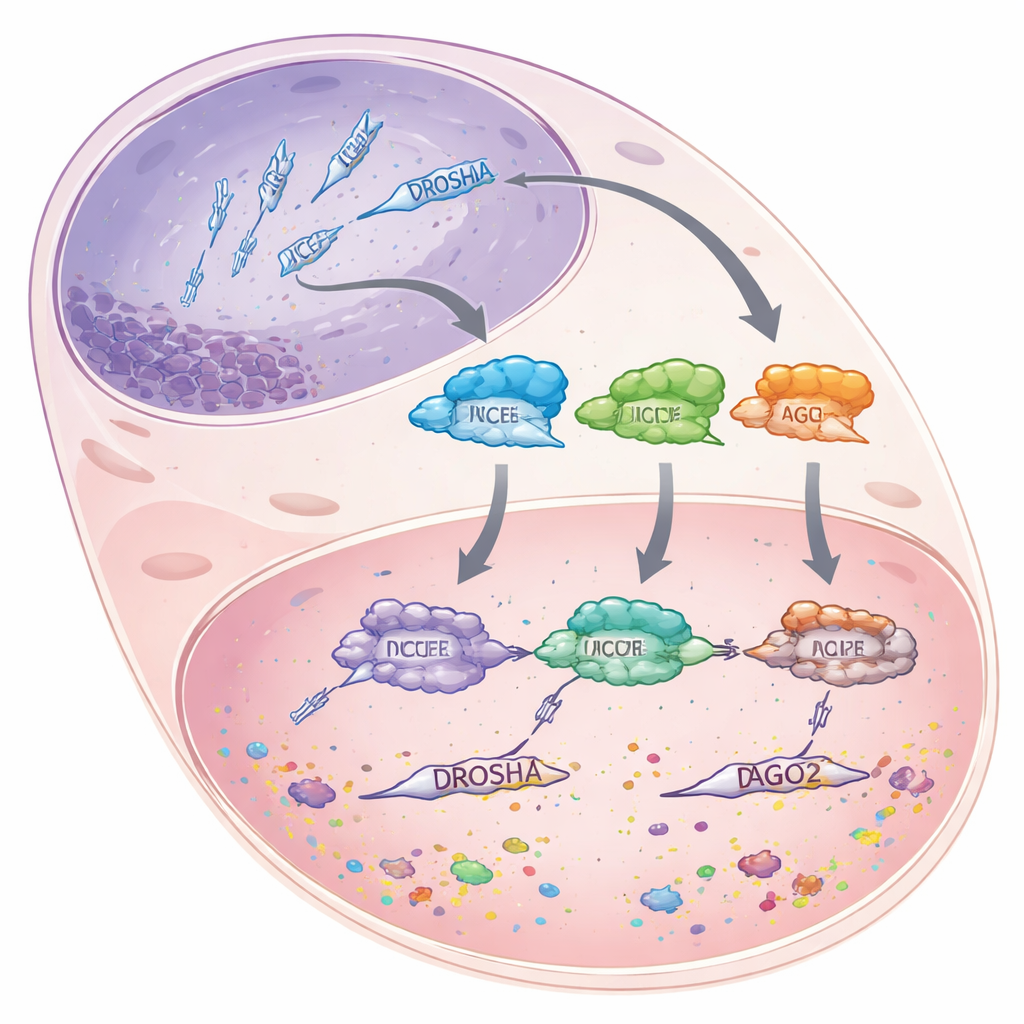
Delikatne kształty o precyzyjnych zadaniach
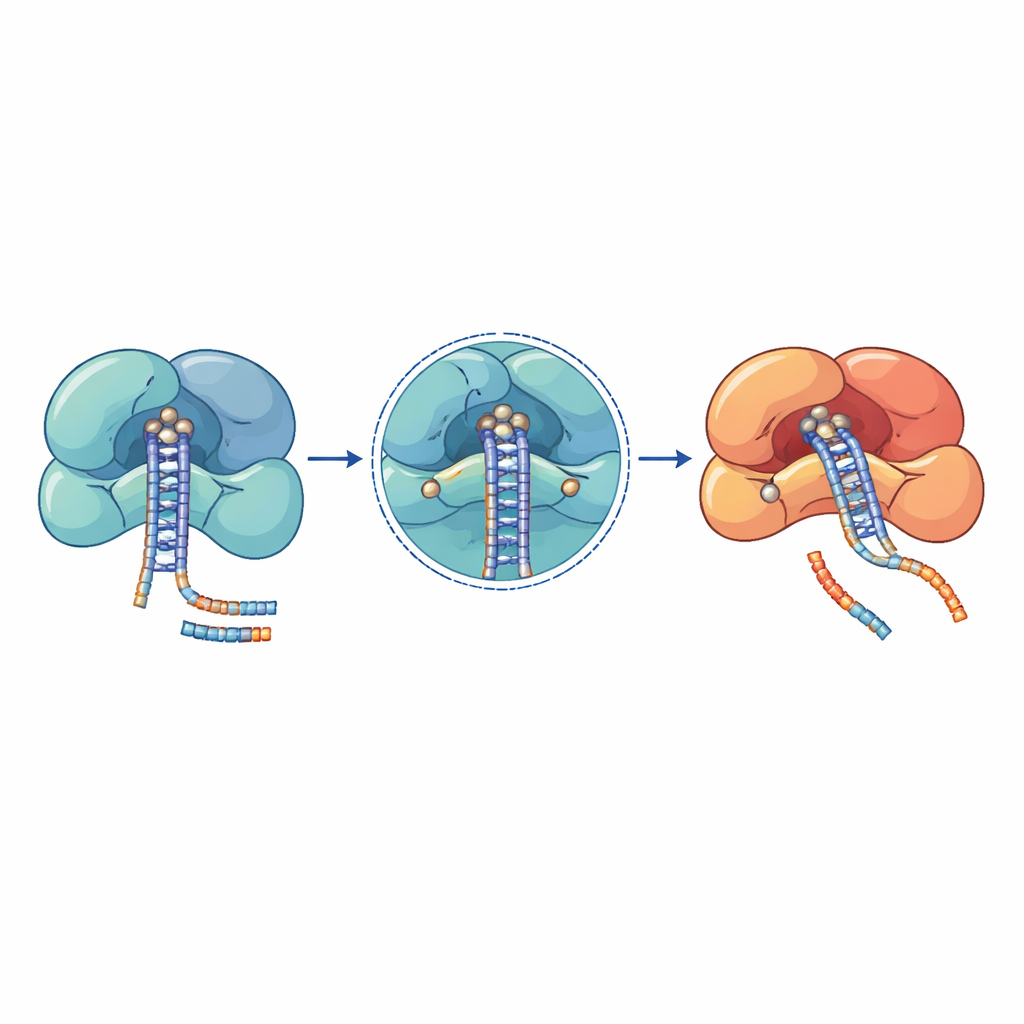
DROSHA, DICER i AGO2 nie są prostymi nożyczkami; każdy z nich zbudowany jest z kilku współdziałających części, które muszą poruszać się w skoordynowany sposób. DROSHA współdziała z białkiem towarzyszącym DGCR8, aby chwycić końce pierwotnej pętelki mikroRNA i ocenić dokładnie, gdzie przeciąć. DICER używa swego rodzaju wbudowanej miarki utworzonej przez swoje domeny, by ustawić stałą odległość między miejscem, gdzie trzyma koniec pętelki, a miejscem, gdzie jego centrum katalityczne wykonuje cięcie. AGO2 owija się wokół pojedynczej nici mikroRNA tak, aby jej region „seed” był idealnie wystawiony do rozpoznawania celów, podczas gdy jony metali i kluczowe aminokwasy w jego rdzeniu ustawiają się do przecinania tych celów, gdy dopasowanie jest wystarczająco silne. We wszystkich trzech białkach dodatnio naładowane rowki i elastyczne łączniki prowadzą nici RNA na swoje miejsce, podczas gdy kieszenie wiążące metale i reszty katalityczne przeprowadzają chemiczne cięcia.
Gdy nożyczki są zgięte lub tępe
Badania genetyczne pacjentów z nowotworami, chorobami krwi i zespołami neurorozwojowymi ujawniły skupiska mutacji w tych maszynach przetwarzających mikroRNA. Wiele najbardziej uszkadzających zmian leży bezpośrednio w centrach katalitycznych lub na ciasnych powierzchniach chwytających RNA. W DROSHA, na przykład, substytucje takie jak E1147K i D1219G znajdują się w sercu miejsca cięcia i zaburzają zdolność wiązania niezbędnych jonów metali, przez co enzym nie jest w stanie przetwarzać pierwotnych mikroRNA. Inne mutacje DROSHA, takie jak skrócenia usuwające region tnący lub zmiany destabilizujące jego helisy podporowe, osłabiają cały kompleks i powodują globalny spadek poziomów mikroRNA w guzie Wilmsa, zaburzeniach szpiku kostnego i chorobach układu nerwowego. W DICER powtarzające się mutacje skupiają się w jednej z jego dwóch domen tnących, zniekształcając produkcję tak, że jedna ramka dupleksu mikroRNA zostaje utracona, co przesuwa równowagę między sygnałami promującymi wzrost i hamującymi go.
Nieprawidłowo ustawione przewodniki w mózgu i poza nim
Mutacje w AGO2 opowiadają inną, lecz pokrewną historię. Bezpośrednie uderzenia w jego rdzeń katalityczny są rzadkie, prawdopodobnie dlatego, że byłyby letalne we wczesnym rozwoju. Zamiast tego warianty związane z chorobami zwykle pojawiają się w elastycznych łącznikach i na złączeniach domen utrzymujących kształt AGO2. W zespole Lessel–Kreienkamp, schorzeniu neurorozwojowym, mutacje w tych łącznikach i otaczających powierzchniach subtelnie skręcają sposób, w jaki części PAZ, MID i PIWI AGO2 się układają i poruszają. Może to źle wyrównać przewodnikowe mikroRNA lub osłabić jego chwyt na docelowych RNA, rozmazując precyzję wyciszania genów podczas rozwoju mózgu. Podobne zmiany strukturalne w dowolnym miejscu ścieżki mikroRNA — czy to w DROSHA, DICER czy AGO2 — mogą rozlać się dalej, zmieniając całe sieci genów zaangażowanych w wzrost komórek, tworzenie krwi czy okablowanie neuronalne.
Przekształcanie wskazówek strukturalnych w przyszłe terapie
Przez nakładanie mutacji chorobowych na mapy 3D o wysokiej rozdzielczości tych białek, badacze mogą dokładnie sklasyfikować, jak każda zmiana powoduje problemy — czy przez stępienie krawędzi tnącej, rozluźnienie krytycznych kontaktów z partnerami białkowymi, czy wygięcie kluczowych helis z osi. Te wnioski strukturalne otwierają drogę do ukierunkowanych interwencji: małe cząsteczki stabilizujące osłabione interfejsy, zaprojektowane RNA, które kierują częściowo funkcjonalne enzymy z powrotem na właściwe substraty, albo związki allosteryczne, które popychają zmutowane białka w bardziej aktywne kształty. Dla laika najważniejsze przesłanie jest takie, że drobne poprawki strukturalne w komórkowych nożyczkach RNA mogą mieć ogromne konsekwencje dla zdrowia, ale jednocześnie dają precyzyjne uchwyty do projektowania nowej generacji terapii uwzględniających mutacje.
Cytowanie: Lee, H., Lee, J. & Roh, SH. Structural insights into disease-associated mutations in the microRNA processing machinery. Exp Mol Med 58, 639–649 (2026). https://doi.org/10.1038/s12276-026-01669-4
Słowa kluczowe: microRNA, interferencja RNA, DROSHA DICER AGO2, genetyka nowotworów, zaburzenia neurorozwojowe